우연히 발견된 후복막강 신경절신경종
A Case of Incidental Retroperitoneal Ganglioneuroma
Article information
Trans Abstract
Ganglioneuroma is a rare benign tumor originating from the neural crest cells. It occurs most commonly in the retroperitoneum and posterior mediastinum and is often found in the neck or pelvis. It may be detected incidentally or detected by pressure effects on the adjacent structures due to its slow growth. However, some functional tumors may secrete catecholamines and present with some clinical symptoms. Complete surgical excision is the treatment of choice. We describe here a case of a retroperitoneal ganglioneuroma which was removed completely by surgery. We review the literature and discuss the clinical features of a ganglioneuroma.
서 론
신경절신경종(ganglioneuroma)은 배아 발달 중 부신수질과 교감신경계를 형성하는 신경배(neural crest)에서 유래한 세포에서 발생하는 양성 종양이다[1]. 보고된 신경절신경종의 발생률은 100만 명당 1명 정도이며, 일차성 후복막강 종양에 있어서는 0.7~1.6% 정도만을 차지하는 정도로 드물게 발생하는 것으로 알려져 있다[2]. 일반적으로 교감신경 줄기를 따라 발달하게 되어 후복막강이나 종격동에서 대부분 발견되며, 경부나 골반강에서도 드물게 발견된다[3]. 저자들은 후복막강에 위치한 신경절신경종을 경험하여 문헌 고찰과 함께 보고하는 바이다.
증 례
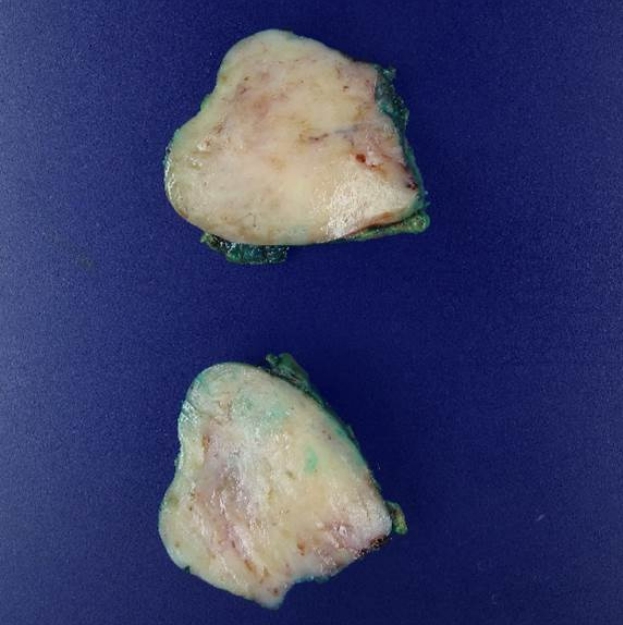
특별한 증상이 없는 40세 남자가 건강 검진에서 시행한 복부 초음파에서 복강 내 종괴가 관찰되었다. 감별진단을 위하여 복부 전산화단층촬영을 시행하였고, 우측 신정맥과 십이지장 2부의 외벽 사이에 약 4.4×2.4 cm 가량 크기의 비교적 균일한 저음영의 타원형의 종괴가 관찰되어 본원 외래를 방문하였다. 과거력에서 특이 소견은 없었고, 사회력에서는 약 8갑년의 흡연력과 1회당 소주 1병 가량, 주 3~4회 정도의 음주력이 있었다. 전신 상태는 양호하였으며, 계통 문진과 신체 검진에서도 특이소견은 없었다. 내원일에 시행한 혈액 검사에서 백혈구 8,060/mm3, 혈색소 14.3 g/dL, 혈소판 423,000/mm3였고, AST 35 IU/L, ALT 25 IU/L, 총 빌리루빈 0.42 mg/dL, 혈액요소질소 10.1 mg/dL, 크레아티닌 0.74 mg/dL로 확인되었다. 감별진단을 위한 자기공명영상 검사(magnetic resonance imaging, MRI)에서 십이지장 2부와 우측신장 사이에 경계가 뚜렷한 약 5.4×4.8 cm 종괴가 관찰되었고 림프절 비대는 없었으며, 주변 장기나 조직으로 침윤은 동반되지 않았다. T1과 T2 강조영상에서 모두 저신호 강도를 띄는 균질한 양상을 보였으며, 조영제를 사용한 역동학적 검사에서 경한 후기 지연증강이 T1 강조영상에서 관찰되었다(Fig. 1). MRI에서 진단이 명확하지 않고 종괴의 위치가 십이지장 2부의 바깥에 위치하고 있어, 내시경 초음파(endoscopic ultrasonography, EUS)를 통한 미세 침 생검(fine needle biopsy)을 시행하였다. 색도플러 영상을 이용하여 혈관을 확인한 뒤, 20게이지(gauge)의 세침바늘(EchoTip ProCore®; Cook Medical, Bloomington, IN, USA)을 이용하여 세침흡입과 조직 생검을 시도하였으나 조직이 매우 단단하여 바늘이 종괴를 충분히 통과하지 못하였고, 획득한 검체에서는 정상적인 소장 점막만 확인되었다. 비록 증상은 없었지만 환자의 나이가 비교적 젊고 종괴의 크기가 5.4 cm 가량으로 컸기에 수술적 제거를 위하여 전신 마취 하에 개복 종괴 적출술을 시행하였다. 적출된 종괴는 4.7×4.3×2.5 cm 크기로, 주변 조직과의 유착이나 침윤 소견은 없었다(Fig. 2). H&E 염색에서 난원형의 신경절세포 주변으로 길게 연장된 핵과 섬유성 세포질을 가지는 슈반세포가 다수 관찰되었고, 미성숙한 신경아세포(neuroblast)는 관찰되지 않았다. 면역조직화학염색에서 S-100과 neuron specific enolase에서 양성 소견을 보였으며, 점액 기질(myxoid stroma)은 관찰되지 않아 신경절신경종으로 진단되었다(Fig. 3). 환자는 수술 후 7일째 특별한 합병증 없이 퇴원하였고, 수술 후 12개월째인 현재, 재발 소견 없이 외래 경과 관찰 중이다.

Magnetic resonance imaging finding. (A) A 5.4×4.8 cm-sized well-defined tumor mass in the retroperitoneum is found with a low signal intensity at T1 weighted image and (B) a low signal intensity at T2 weighted image (arrow).
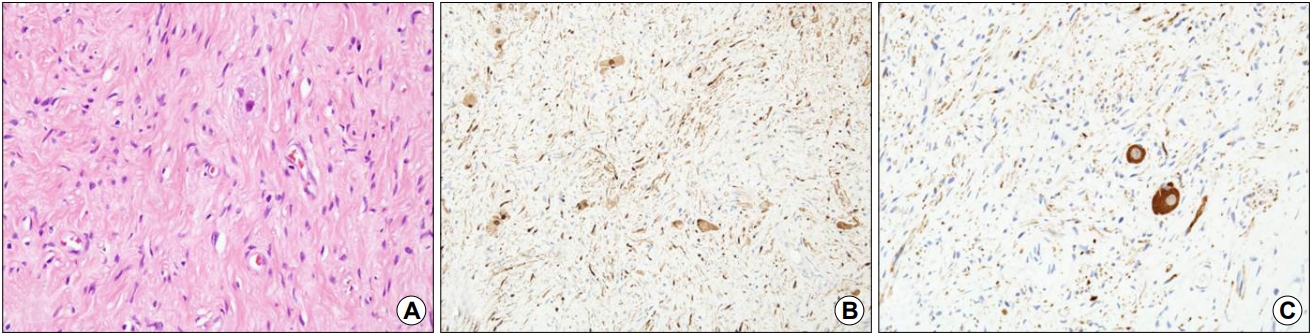
Microscopic findings of the resected specimen. (A) Many Schwann cells with fibrous cytoplasm are observed around the mature ganglion cells (H&E, ×400). (B) Schwann cells are positively stained with S-100 protein (S-100, ×200). (C) The ganglion cells are positively stained with neuron specific enolase (neuron specific enolase, ×200).
고 찰
교감신경계에서 기원하는 종양은 교감신경모세포(sympatheticoblast)의 성숙 정도에 따라 높은 악성도를 보이는 신경모세포종(neuroblastoma), 잘 분화된 성숙 신경절세포로 구성된 신경절신경종과 그 중간 형태를 보이는 신경절모세포종(gaglioneuroblastoma)으로 구분할 수 있다. 그중 신경절신경종은 조직학적으로는 슈반세포, 신경절세포와 신경섬유로 구성된 양성종양이다[3,4].
모든 연령에서 보일 수 있지만 소아와 젊은 성인(42~60%)에서 흔히 발견되며, 남녀 간의 비율은 1:1.13~1:1.5 정도로 여성에서 약간 더 호발한다고 보고된다[2,4,5]. 척추 교감신경절(paravertebral sympathetic ganglia)을 따라 어디든지 발생할 수 있으나 주로 후복막강(32~52%)이나 종격동(39~43%)에 흔히 발생하며, 드물게 소화기계, 뼈, 쇄골 주변, 부신에서도 보고되는 경우가 있다[6].
신경절신경종은 증상이 없는 경우가 대부분으로, 병변이 커지면서 주변 조직 압박으로 인하여 복부 통증, 정맥순환 장애, 변비, 복부 팽만감, 요로 및 위장관계의 기능 장애가 발생할 수 있다. 드물게 카테콜라민, 장내 혈관 펩티드(vasointestinal peptide)와 안드로겐과 같은 호르몬을 생산하여 설사, 발한, 고혈압, 안면홍조 등을 야기할 수 있으며, 이러한 경우 갈색세포종과의 감별이 어려울 수 있다[4]. 호르몬 분비와 관련된 증상들은 종양을 제거하면 대부분 호전된다.
초음파 검사에서 주변 조직과는 경계가 뚜렷한 비교적 균일한 저에코의 종양으로 관찰되며, 전산화단층촬영에서는 근육보다 저음영으로 확인되고, 지방이나 낭성 성분이 없으며 조영증강은 대개 잘 되지 않는다[6]. 보고에 따르면 신경절신경종의 약 10~25%에서 석회화가 관찰될 수 있는데, 산재된 반점 양상(scattered spotty)이거나 알갱이 양상의 석회화(grain like calcification)는 양성 병변을 시사하고, 반면 거대반(large patchy) 또는 불규칙한 석회화를 보이는 경우에는 악성 경향을 시사하여 감별진단에 도움이 된다[7]. 자기공명영상에서는 T1 강조영상에서 균질한 저신호 강도를 보이고, T2 강조영상에서는 이질성의 고신호 강도 또는 등신호 강도를 보이는 것으로 알려져 있다. T2 강조영상의 강도와 조직학적 소견은 연관성을 보이는데, 종양의 점액 기질이 풍부하고 상대적으로 세포충실성(cellularity)이 떨어지며, 아교섬유(collagen fiber)가 적을 때는 고신호 강도로 나타날 수 있는 반면, 세포충실성과 아교섬유가 풍부하고, 점액 기질의 양이 적을 때는 반대의 경우에 비하여 낮은 신호 강도를 보이게 된다. 즉 조직학적 구성 성분의 비에 따라 자기공명영상의 T2 강조영상에서 신호 강도가 달라질 수 있다[8]. 본 증례의 경우 T2 강조영상에서 낮은 신호 강도를 보였는데, 조직에서 아교섬유가 풍부하였던 반면 점액 기질은 관찰되지 않았기에 신호 강도가 낮게 나왔던 것으로 생각된다.
신경절신결종은 수술적 제거를 통하여 완치가 가능하며, 국내의 한 연구에서 35명의 신경절신경종 환자들을 수술적 절제 후 추적 관찰하였을 때 재발 없이 양호한 예후를 보이는 것을 확인하였다[9]. 하지만 종양이 대동맥, 대정맥 또는 신경과 같은 조직을 침범하거나 유착하는 경향이 있어 주의가 필요하다. 42명의 신경절신경종 수술을 받은 환자를 후향적으로 분석한 연구에서 장기 생존율은 훌륭하였지만 약 21%에서 수술 연관 합병증이 보고되었다. 이 중 1명은 사망하였고, 6명에서 호너 증후군(Horner syndrome), 대동맥의 파열(rupture of aorta), 감각이상(paresthesia) 등이 보고되었다[10]. 신경절신경종에 대하여 불완전 절제를 할 경우 항암 치료나 방사선 치료를 시행하지 않더라도 전체 생존율(overall survival)이나 재발에는 큰 차이가 없는 것으로 알려져 있다[11,12]. 그러나 신경절신경종은 약 25%에서 악성화 병변과 함께 있는 경우가 있어[13] 불완전 절제를 시행할 경우에는 여러 부위에서 동결 절편 검사를 시행하여 종양이 양성임을 충분히 확인하는 것이 필요하다. 수술적 치료 이후 추적 관찰의 기간이나 방법에 대하여는 정립된 내용은 없는 실정이다. 일부 연구에서 매년 신경학적 검사를 포함한 신체검진과 MRI를 이용하여 국소 재발 여부를 확인하는 것을 추천하고 있으며, 종양의 자연 경과를 고려하였을 때 불완전 절제시에도 1년 간격의 추적 검사로 재발 여부를 확인할 수 있다고 언급하고 있다[14,15]. 따라서 신경절신경종의 완전 절제를 할 경우 완치가 가능하며, 예후는 매우 좋은 것으로 알려져 있다. 하지만 인접 장기나 신경조직에 손상을 주거나 수술 합병증의 가능성이 높다면 부분 절제술이나 면밀한 경과 관찰을 하며 잔존 종양의 성장 및 합병증 발생 여부를 추적 관찰하는 방법도 고려해볼 수 있을 것이다. 요약하면 이번 증례는 우연히 발견된 후복막강에 위치한 종괴가 수술적 치료를 통하여 신경절신경종으로 확진된 증례로, 문헌 고찰과 함께 보고하는 바이다.
Notes
No potential conflict of interest relevant to this article was reported.