 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 20(3); 2020 > Article |
|
Abstract
Achalasia is a rare primary esophageal motility disorder characterized by the loss of enteric neurons leading to an absence of peristalsis and impaired relaxation of the lower esophageal sphincter. The subsequent stasis of ingested food not only leads to symptoms of dysphagia, regurgitation, chest pain, and weight loss, but also results in an increased risk of esophageal carcinoma. Structural or functional pulmonary abnormalities occur in more than half of patients and may be due to recurrent aspiration or tracheal compression from a dilated esophagus. Delayed diagnosis or ineffective intervention may lead to progressive dilation of the esophagus and the development of a megaesophagus. Respiratory distress and cardiopulmonary arrest from tracheal or left atrial compression secondary to a megaesophagus are rare complications of achalasia. There is only limited evidence that pneumatic dilation may be used as a first-line therapy for a megaesophagus. The choice of definitive treatment will depend on many factors including achalasia type, patient wishes, performance status, and surgical expertise.
ěëě´ěëśëĽěŚ(achalasia)ě ě°íě ěë 체ëśě ě°ëě´ë ěě¤ęłź íëśěëę´ě˝ęˇźě ëśěě í ě´ěě ëł´ě´ë ěëě´ë ě§íě´ë¤[1]. íëśěëę´ě˝ęˇźě íěëĄ ěěëŹźě´ ěë ë´ę°ě ě§ěě ěźëĄ ě 체ëě´ ěźí´ęł¤ë, ěíëě§ ěě ěě돟ě ěëĽ, íĄě¸ěą 기욨, ííľ, ě˛´ě¤ ę°ě ëąě ěŚěě ě ë°íë¤[2]. ě§ë¨ě´ ě§ě°ëęą°ë ěšëŁę° ëśěśŠëśí ę˛˝ě° ěë íěĽě´ ě§íëě´ ęą°ë ěë(megaesophagus)ëĄ ëłíëë ë§ę¸° ěëě´ěëśëĽěŚ(end-stage achalasia)ěźëĄ ë°ííë¤[3]. íěĽë ęą°ë ěëë íę° ë° ěŁźëł ě˘
겊ë ěĽę¸°ëĽź ěë°íěŹ ě¤ěŚ íŠëłěŚě ě ë°í ě ěë¤. ë°ëłľě ě¸ ëŻ¸ě¸ íĄě¸ě´ë íěĽë ěëě ěí 기ë ěë°ěźëĄ 꾏쥰ě ëë 기ëĽě í ě´ěě ě´ëí ě ěěźëŠ°[4], ę¸ěą ě기ë íěě ę°ě í¸íĄę¸° íŠëłěŚ ë°ěě´ ę°ëĽíë¤[5]. ëí ěŁźëł íę´ ěë°ěźëĄ ě¸í ěŹíę´ęł íí ë° ě˘ěŹë°Šě ěë°íěŹ ëśě 맼 ë° íěíě ëśěě ě ě ë°í ě ěěźë[6], ę¸ěą í¸íĄëśě ë° ěŹě ě§ě ě´ëĽ´ë 경ě°ë ë§¤ě° ë돟ë¤[7]. ě ěë¤ě ęą°ë ěëě ěí ě˘ěŹë°Š ěë°ěźëĄ ë°ěí ę¸ěą ěŹě ě§ëĽź ëë°í ë§ę¸° ěëě´ěëśëĽěŚ íě뼟 경ííęł íě íěĽě ëĄ ěšëŁíě기ě 돸í ęł ě°°ęłź í¨ęť ëł´ęł íë ë°ě´ë¤.
67ě¸ ë¨ěę° íëŹ ě ëśí° ë°ěí ěźí´ęł¤ë ë° ęľŹí 뼟 죟ěëĄ ë´ěíěë¤. ě˝ 8ë
ě ëśí° ę°íě ě¸ ęľŹí ěŚě¸ę° ěěěźë ěšëŁëĽź íě§ ěěěźëŠ° 2ë
ě ëśí° ěě돟 ěëĽ ěŚěěźëĄ ę°ě¸ëłěěě ěëĽěą ěëěźěźëĄ ě§ë¨ë°ęł ě˝ëŹź ěšëŁëĽź íěěźë ěŚěě ě
íě í¸ě ě ë°ëłľíěë¤. íëŹ ě ëśí° 돟곟 ęł íěě ěźí´ęł¤ë ë° ěěŹ ě§í 꾏í ěŚě¸ę° ě§ěëęł 1죟 ě ěë ě늴 ě¤ ęľŹí ę° ë°ěíěŹ ěí기ë´ęłź ě¸ëëĄ ë´ěíěë¤. ęłźęą°ë Ľěě 본íěą ęł íěěźëĄ 5ë
ę° ě˝ě 뼟 ëłľěŠíěěźëŠ°, 30ë
ě ěě˛ęłľ ěě ě íěë¤. ě 체 ę˛ěŹěě ë§ěą ëłěě´ěěźëŠ° ěĽěě ě ěě´ěęł , ꡸ ě¸ě íšě´ ě겏ě ę´ě°°ëě§ ěěë¤. ěŹě ë ë° íëś ë¨ě ě´Źěěě ě´ě ě겏ě ěěë¤. íëś ě ě°íë¨ě¸ľě´Źěěě ě ë°ě ě¸ ěëě íěĽęłź ěë ë´ę° ë´ ěĄě˛´ ě ëĽ ěę˛Źě´ ę´ě°°ëěë¤(Fig. 1).
ěëśěěĽę´ ë´ě경 ę˛ěŹěě ěë 체ëśě ëšě ěě ě¸ íěĽęłź ěě돟 ě ëĽę° ę´ě°°ëěěźëŠ° ěěëě íŠëśę° ëěŹěěěźëĄ ę°íę˛ ěěśëě´ ě˘ěě ¸ ěěë¤(Fig. 2A). ěë ě ë§ ěĄ°ě§ ę˛ěŹěě íšě´ ě겏ě ěěěźëŠ°, ěë쥰ěě ěě ěë 체ëśě íěĽ ë° ě°ëě´ë ěě¤ęłź ěŹí ěěëś ěëíě°ŠěźëĄ ě¸í íëś ěëě ěëśëŚŹ(birdâs beak) 모ěě´ ę´ě°°ëěęł (Fig. 2B), ěëë´ě ę˛ěŹěě ě°í ě íëśěëę´ě˝ęˇźě ëśě´ěęłź ěë 체ëśě ě°ëě´ëě ěě¤ ë° ëŽě ěë Ľě ëěěą ěěśě´ ę´ě°°ëěë¤(Fig. 2C). ęł íěě ě´ěŠí ëěěě ěëíľęłź ę˛ěŹěě ę˛ěŹ 10ëśě 55%, 20ëśě 57%ě ěëĽě¨ëĄ íě í íľęłź ěę°ě ě§ě°ě ëł´ěë¤(Fig. 2D). Eckardt ěŚě ě ěë 10ě (ěźí´ęł¤ë 3, ěëĽ 3, ííľ 1, ě˛´ě¤ ę°ě 3)ěźëĄ ěŹí ěëě´ěëśëĽěŚěźëĄ ě§ë¨íęł íě íěĽě ě ęśě íěěźë ěě íŠëłěŚě ëí ëë ¤ěěźëĄ íěę° ęą°ëśíěŹ í´ěíěë¤.
íěë 2죟 í í¸íĄęł¤ëęłź 기욨 ë° ëěą ę°ë´ěźëĄ ěę¸ě¤ëĄ ë¤ě ë´ěíěë¤. íë Ľě§íë íě 125/80 mmHg, 맼ë°ě 71í/ëś, í¸íĄě 26í/ëś, ě˛´ě¨ 38.6âěë¤. ę˛ěŹě¤ ě겏ě ë§ě´íěĄ ę˛ěŹěě ë°ąí꾏 10,990/mm3, íěě 15.0 g/dL, íěí 254,000/mm3ěë¤. íě˛ ěíí ę˛ěŹë ěëśëŻź 4.6 g/dL, ěěě§ě 14.0 mg/dL, íě˛ íŹë ěí°ë 0.95 mg/dL, ě´ ëšëŚŹëŁ¨ëš 0.55 mg/dL, AST/ALT 28/24 IU/LěěźëŠ°, íě˛ ě í´ě§ ę˛ěŹë ëí¸ëĽ¨ 137 mEq/L, 욟뼨 4.1 mEq/L, ěšźě 8.4 mg/dL, ë§ęˇ¸ë¤ě 2.1 mg/dLěěźëŠ°, C-ë°ěěą ë¨ë°ąě§ě 178 mg/LëĄ ěŚę°ëě´ ěěë¤. íëś ë¨ěě´Źěěě ě츥 íěźě ěěě´ ěŚę°ëě´ ěěěźëŠ°, ęł í´ěë íëś ë¨ě¸ľě´Źěěě ě츥 ííëś, ě°ě¤ě˝ ë° ě˘ěě˝ íë ´ ěę˛Źě´ ę´ě°°ëěěźëŠ° ěë íëśę° í˝ě°˝ë ě겏ě´ěë¤(Fig. 3).
ę¸ěą íë ´ěźëĄ ě§ë¨íęł ě
ěíěŹ 5ěźę° íěě ěšëŁ í ěě ěŚěęłź ë°ŠěŹě íě ę˛ěŹ ěę˛Źě´ í¸ě ëë ě¤, 욨ěěě ëëłě ëł´ęł ë ě§í ę¸ěě¤ë° í¸íĄęł¤ë ë° ěě ěě¤ě´ ë°ěíěěźëŠ°, ě꾏í¸ě(eyeball deviation) ě겏곟 경ë맼 ë° ěíëś ë§Ľë°ě´ ě´ě§ëě§ ěě ěŚě 기ëě˝ę´ ë° ěŹíěěě ě ěííěë¤. ě˝ 2ëśę°ě ěŹíěěě í íěë ěěě íëłľíęł ě체 ě§íę° ěě ëěěźëŠ°, ě§í ěíí ěŹě´ěí ę˛ěŹěě íěĽë ěëę° ě˘ěŹë°Šě ě¸ě¸Ąěě ěë°íë ěíěęł ě´ëĄ ě¸í ě˘ěŹë°Š íí ěę˛Źě´ ę´ě°°ëěë¤(Fig. 4). ëí ę˛ěŹ ë° ëëś ě ě°íë¨ě¸ľě´Źě ëąě ě ěě´ěęł , ěëě´ěëśëĽěŚě ěí ě˘ěŹë°Š ěë°ěźëĄ íë¨íęł ë¨źě ëšěę´ě íëś ěëě ě˝ě
íěŹ ę°ěě ěíí í ë¤ě ë íě íěĽě ě ěííěë¤. íëśěëę´ě˝ęˇź ëśěě 3.0 cm ě§ę˛˝ě RigiflexÂŽ íě ěě¤í
(Boston Scientific, Marlborough, MA, USA)ě ě´ěŠíěŹ 12 psiě ěë ĽěźëĄ 90ě´ ę° 2í íě íěĽě ě ěííěęł , ěě ë¤ě ë ěíí ěë 쥰ěě ěě 쥰ěě ę° ě íľęłźëë ę˛ě íě¸íěěźëŠ° ěě ěźěŁźěź í ěíí ěŹě´ěí ę˛ěŹěě ě˘ěŹë°Šě ěë°íë ě˘
ę´´ë ę´ě°°ëě§ ěěë¤(Fig. 5). ěě í ěŚěě í¸ě ëě´ ě ě ěě´ í í´ěíěěźëŠ°, 3ę°ě í ěśě ěŹě´ěí ę˛ěŹë ě ěě´ěęł Eckardt ěŚě ě ě 1ě (ěźí´ęł¤ë 0, ěëĽ 1, ííľ 0, ě˛´ě¤ ę°ě 0), ęł íěě ě´ěŠí ëěěě ěëíľęłź ę˛ěŹěě ę˛ěŹ 10ëśě 5.4%, 20ëśě 5.1%ě ěëĽě¨ëĄ ě´í 5ë
ę° ěŚě ěë ěíëĄ ě¸ë ěśě ě¤ě´ë¤.
ěëě´ěëśëĽěŚě ěě¸ě ě ě ěë íšë°ěąě¸ 경ě°ę° ëëśëśěźëĄ ěëě ě°ëě´ëęłź íëśěëę´ě˝ęˇźě ě´ěě 쥰ě íë ꡟěĄě 경ě (myenteric plexus)ě ě´ěě ěí´ ë°ěíë¤[2]. ě ě ë° ëŠ´ěíě ěě¸ě ę°ě§ ěŹëěě ë¨ěíŹě§ë°ě´ëŹě¤ ëąě ę°ěźë늴 ě´ě 늴ěë°ěě´ ě ë°ëě´ ęˇźěĄě 경ě ě ěźěŚě ěźěźí¤ëë°, ě¸íŹë
ěą ëŠ´ěë°ěě´ ě§ěë늴 ě ě°¨ě ěźëĄ ě 경ě¸íŹë¤ě´ ę°ěíěŹ ę˛°ęľ ěě¤ëęą°ë ě 경 기ëĽě ěĽě 뼟 ěźěźí¤ë ę˛ěźëĄ ěśě íë¤. íěě ěěę˛˝ęłźę° ë¤ěí ę˛ě 늴ěë°ěě ě˘
ëĽě ě¸íŹë
ěą ëŠ´ěë°ěě ě ëě ë°ëź ě§íěëě íííě´ ë¤ëĽ´ę¸° ë돸ě´ë¤[8].
ěëě´ěëśëĽěŚě ě§íě´ ě ě§ě ěźëĄ ě´ëŁ¨ě´ě§ëŻëĄ ě§ë¨ ěęšě§ ěë
ę° ěŚěě 경ííë¤[9]. Adams ëą[10]ě ěŚěě 3ë¨ęłëĄ ëśëĽíěëë°, 1ë¨ęłë ěźí´ęł¤ë, ííľ ë° ěëĽ ěŚěě´ ěě§ë§ ě ě ěë ě§ę˛˝ě ëł´ě´ë 경ě°, 2ë¨ęłë ěë ě§ę˛˝ě´ ěŚę°ë늴ě ěźí´ęł¤ë ë° ííľě´ ěźěě ěźëĄ ę°ěëë 경ě°, 3ë¨ęłë ěëę° ë§¤ě° ěŹíę˛ íěĽëě´ ěŚěě´ ě§ěě ěźëĄ ě
íëęł ě˛´ě¤ę°ěę° ëł´ě´ë 경ě°ě´ë¤. ěëę° íě í íěĽëě´ ěë ë§ę¸° ěëě´ěëśëĽěŚ ë¨ęłě íěë¤ě ëę° í¸íĄę¸° ěŚěě ě죟 í¸ěíëë°, ě ëĽë ěě ë° ëśëšëŹźëĄ ě¸í ěźę° 기욨곟 경ëě í¸íĄęł¤ë, íĄě¸ěą íë ´ ë° íëě, ëëŹźę˛ íěĽë ěëě ěí´ ę¸°ę´ě´ ěë°ë ę˛˝ě° ę¸ěą í¸íĄëśě ě´ ë°ěí ě ěë¤[11]. ë§ę¸° ěëě´ěëśëĽěŚěźëĄ ě¸í ęą°ë ěëěě ěŹě ě§ ë° ę¸ěŹě ę´ë ¨ë 기ě ěźëĄë ěě돟 íĄě¸, ę¸°ę´ ë° ěŹěĽ ěë°, ěěě ěëíľęłźëĽź ěí ë°ě´ë° 쥰ěě ě ë°ë ëśě 맼, ěëꜤě ěśí, ěëě˛ęłľ ëąě´ ę°ëĽíë¤[12]. 본 ěŚëĄěěë íěĽë ěëě ěí´ ě˘ěŹë°Šě´ ěë°ëě´ ę¸ěą ěŹě ě§ę° ë°ěí ę˛ěźëĄ ěśě ë늰, ě˘ěŹë°Šě ěŹěĽě íë°Šě ěěšíěŹ ěë ë° ííëë맼곟 ꡟě íęł ë˛˝ě´ ëšęľě ěęł ë´ëś ěë Ľě´ ëŽě 죟ě 꾏쥰돟ě ěí´ ěë°ë ě ěë¤. D'Cruz ëą[13]ě ě˘ěŹë°Š ěęľ(impression)ě ëí´ í´ëśíě ëłíě ěŹí ě ë ë° íěíě 결곟뼟 í ëëĄ ęˇźě (proximity), 욨ë˛(encroachment), ěë°(compression)ěźëĄ ě¸ëśíěëë°, ę°ěĽ ěŹí ííě¸ ě˘ěŹë°Š ěë°ě ě˘ěŹë°Š ěŠě ë° ěŹë°ěśëě ę°ěěěź í¸íĄęł¤ë, ě´ë ë´ěą ę°ě, íěíě ëśěě ě ěźěźí¤ëŠ°, ě˘ěŹë°Š ěë Ľ ěěšěźëĄ ěŚę°ë íě 맼ěěźëĄ ě¸í´ íëśě˘
ě ě ë°í ě ěë¤[6]. 본 íěë ë°°ëł ě ë°ě´ë° 쥰ěěźëĄ íę° ë´ ěë Ľě´ ěěšíěŹ íěĽë ěëě ěí ě˘ěŹë°Š ěë°ě´ ěźěě ěźëĄ ěŚę°íęł ě 맼íëĽę° ę°ěí늴ě ěŹě ě§ę° ë°ěíěě ě ěěźëŠ°, ë°ě´ë° 쥰ěěźëĄ ě ë°ë ëśě ë§Ľě´ ěě¸ěź ę°ëĽěąë ěë¤.
ěëě´ěëśëĽěŚęłź ëë°ë ę¸ěą í¸íĄëśě ë° ěŹě ě§ë ë§¤ě° ë돸 ěŹę°í íŠëłěŚěźëĄ ěěě ěŚëĄę° ëł´ęł ëěęł ę° ěŚëĄ ë§ë¤ ěë ě´ěëśëĽěŚě ëí´ ë¤ëĽ¸ ěšëŁ ë°Šë˛ě ě ěŠíěë¤[7]. Bruijnsęłź Hicks [14]ë 79ě¸ ěŹě íěę° ěí í¸íĄě ě§ëĄ ë´ěíěŹ ę¸°ëě˝ę´ ë° ě¸ęłľí기 ěíěě ěëě´ěëśëĽěŚ ě§ë¨ íě ëšěę´ě íľí ěë ę°ě í ëł´í¤ëŚŹë ë
ě 죟ě
ěšëŁëĽź íěŹ ěšëŁí ěŚëĄëĽź ëł´ęł íěěźë ě´í íěě ěśě ę˛ěŹę° ě´ëŁ¨ě´ě§ě§ ěě ěĽę¸° ěí뼟 ě ě ěěë¤. Altintoprak ëą[15]ě 18ë
ě ëśí° ěźí´ęł¤ëě´ ěë 35ě¸ ěŹě íěę° ěí ěŹě ě§ëĄ ë´ěíěŹ ěŹíěěě ě ěííěěźëŠ° ě ě°íë¨ě¸ľě´Źěěě íěĽë ěëëĄ ě¸í ěŹěĽ ë° ę¸°ę´ ěë° ěę˛Źě´ ę´ě°°ëě´ ëšěę´ě íľí ěë ę°ě í ëłľę°ę˛˝ íŹëŹ ꡟě ě ě ëĄ ěšëŁí í 18ę°ěęšě§ ěśě ę´ě°°í ěŚëĄëĽź ëł´ęł íěë¤. ꡸ëŹë 본 ěŚëĄě íěěěë ęł ë š ë° ę¸ěą íë ´ ëąě ě ě ěíę° ě˘ě§ 몝íěŹ ěě ě ěšëŁëĽź ě íí기 ě´ë ¤ě ë¤. Hifumi ëą[5]ě 13ë
ě ëśí° ěźí´ęł¤ëě´ ěë 53ě¸ ěŹě íěěě ě´ěĄ ě¤ ë ě°¨ëĄě ěŹíě ě§ëĄ íëśěë° í 기ëě˝ę´ ë° ě ě˛´ě¨ ěšëŁëĽź ëłíí늴ě ěëë´ě ę˛ěŹ ë° ě ě°íë¨ě¸ľě´Źěěě ęą°ë ěëëĄ ě¸í ę¸°ę´ ěë° ěę˛Źě´ ę´ě°°ëě´ ëšěę´ě íľí ěë ę°ě í íě íěĽě ëĄ ěšëŁí ěŚëĄëĽź ëł´ęł íěěźë ěšëŁ í íëŹ ě´í ěśě ę˛°ęłźę° ěě´ ěĽę¸°ěí뼟 ě ě ěěë¤. íší, Mabvuure ëą[7]ě 결ě ěą ę˛˝íěŚ ë° ę°ě§ ëłë Ľě´ ěë 40ě¸ ë¨ěę° ěí ę¸°ę´ íě°ŠěěźëĄ ë´ěíěŹ ěëě´ěëśëĽěŚěźëĄ ě¸í´ íěĽë ěëę° ę¸°ę´ě ěë°íěŹ íě íěĽě ëĄ ěšëŁíěěźë ěë íěĽě´ ěŹë° ë° ě§íëě´ 2ę°ě í ë¤ě ěŹíě ě§ę° ë°ěíěŹ ěëě ě ě ëĄ ěšëŁí ěŚëĄëĽź ëł´ęł íěë¤.
본 ěŚëĄěěë íë ´ ë° íěě ě ě ěíę° ě ě ë§ěˇ¨ě ěě ě´ ě´ë ¤ě´ ěíěě ěŹě ě§ě ě¤ěŚ íŠëłěŚě ëë°í 경ě°ëĄ, ěśí ěŹë°ě´ ěěźëŠ´ě ę°ëĽí ěľě 욨ěľě ěšëŁë˛ě ęł ë ¤í´ěź íë¤. ěëě´ěëśëĽěŚě´ ě§íë늴 ěëę° íŹę˛ í˝ě°˝íę˛ ë늴ě ěśí¸ě ë° ëší댟ěźëĄ Sěí ěëëĄ ëłíë늰[16], ě´ ę˛˝ě° ěëě ě ě ě´ ęˇźëł¸ě ě¸ ěšëŁëĄ ęł ë ¤ëě§ë§ íŠëłěŚęłź ěě ę´ë ¨ ěŹë§ëĽ ě´ ëë¤. Inoue ëą[17]ě ęł ë š, ě´ě ěšëŁ ęłźęą°ë Ľ, 6 cm ě´ěě ěë íěĽ, Sěí ěë뼟 íŹí¨í 500ëŞ
ě ěë ě´ěëśëĽěŚ íěěę˛ ę˛˝ęľŹ ë´ě경ě ꡟě ę°ě ě ě ěŠíěŹ ěšëŁ í¨ęłźę° ě˘ęł ěě ę´ë ¨ íŠëłěŚě 3.2%ëĄ ěě íë¤ęł ëł´ęł íěěźë ě ě ěíę° ě˘ě§ ěě ě ě ë§ěˇ¨ëĽź í ě ěë íěë ě ě¸íěë¤. Sěí ěëěě ëłľę°ę˛˝ íŹëŹ ꡟě ě ě ë° ę˛˝ęľŹ ë´ě경 ěë ꡟě ę°ě ěšëŁ ě ě˘ě 결곟뼟 ëł´ěŹěŁźë ě°ęľŹë¤ě´ ěě§ë§ ěĽę¸°ě ě¸ í¨ęłźě ëí´ěë ěśę° ě°ęľŹę° íěíë¤[18]. Khan ëą[19]ě 9ëŞ
ě ęą°ë ěë(7 cm ě´ěě ě§ę˛˝) íěěě íě íěĽě ě ěííěŹ íŠëłěŚě´ ěě´ ěśŠëśíę˛ íěĽíěęł 12ę°ě ěśě ę´ě°°ěě ě§ěě ě¸ ěŚě í¸ě ě ëł´ęł í ë° ěë¤. ë°ëźě, 본 ěŚëĄě íěěěë íě íěĽě ě ěľě 욨ěľě ěšëŁë˛ěźëĄ íë¨íěŹ ěííěěźëŠ°, ě´ě ëł´ęł ěě ěĽę¸° ěśě ę˛°ęłźę° ěě´ ëł¸ íě뼟 5ë
ę° ěśě ę´ě°°íěěźë ěŚě¸ ë° ë´ě경, ëěěě ěëíľęłź ę˛ěŹ, ěë 쥰ěě , ěŹěĽ ě´ěí ę˛ěŹ ëąěě í¸ě ë ěíëĄ ě ě§ëęł ěě´ ěě ě´ ě´ë ¤ě´ íěěě ěĽę¸°ę° ěě í ěšëŁëĄ ęł ë ¤í´ ëłź ě ěë¤. ěľęˇź ęł í´ěë ěëë´ě ę˛ěŹëĽź íľí´ ěëě´ěëśëĽěŚě ěí ëśëĽę° ę°ëĽí´ěĄęł , IIíě íě íěĽě ęłź ëłľę°ę˛˝ íŹëŹ ꡟě ě ě ě ěšëŁ í¨ęłźę° ë ëęł IIIíě I, IIíě ëšíěŹ ěíę° ëěë¤[20]. ęł í´ěë ěëë´ě ę˛ěŹëĽź ěííě§ë 몝íěěźë 본 íěë 체ëśě ëě ěěśíę° ę´ě°°ëë IIíěźëĄ íě íěĽě ě ě˘ě ěĽę¸° ěšëŁ í¨ęłźëĽź ëł´ě¸ ę˛ěźëĄ ěśě í ě ěěźëŠ°, IIIíě 경ě°ëźëŠ´ ꡟě ę°ě ě ě ě¤í ęł ë ¤í´ěź íë¤.
ë§ę¸° ěëě´ěëśëĽěŚě ěšëŁë ě´ë ¤ě°ëŠ° ěŹíě ě§ě ę°ě ě¤ěŚ íŠëłěŚě ëë°í ęą°ë ěëě ę˛˝ě° Sěí ěë ě 돴, ěëë´ě ę˛ěŹě ěí ěí, ě´ě ěšëŁ ęłźęą°ë Ľ, íě ěí, ěě ěě ěë ¨ë, ěëŁę¸°ę´ě ěě¤, ě¸ęłźě ě 돸ěąě íŹí¨í ë§ě ěě뼟 ęł ë ¤íěŹ ěšëŁë°Šë˛ě 결ě íěŹěź íë¤. 본 ěŚëĄěě ěëě´ě ëśëĽěŚěźëĄ ě¸í ęą°ë ěëě ě˘ěŹë°Š ěë°ěźëĄ ë°ěí ę¸ěą ěŹě ě§ íěěě íě íěĽě ëĄ ěąęłľě ěźëĄ ěšëŁíęł ěĽę¸°ę° ěśě ę´ě°°ěě ě˘ě ěí뼟 ëł´ě기ě ëł´ęł íë ë°ě´ë¤.
Fig. 1.
(A) Chest contrast CT shows diffuse wall thickening and marked distension with fluid retention in the esophagus. (B) Transverse CT image shows the presence of a dilated esophagus abutting the left atrium.

Fig. 2.
(A) Upper endoscopy reveals abnormal esophageal dilatation and food material with a contracted gastroesophageal junction. (B) Barium esophagram shows the dilated esophagus (maximal transverse diameter: 54 mm) and bird beak appearance. (C) Esophageal manometry shows a low amplitude simultaneous contraction. (D) Radionuclide esophageal transit study shows an adynamic esophageal transit pattern with 57% retention after 20 minutes.

Fig. 3.
High resolution chest CT scan shows multifocal peribronchial distributed ill-defined small nodules and ground glass opacities in the left upper lobe, right middle lobe, and both lower lobes.
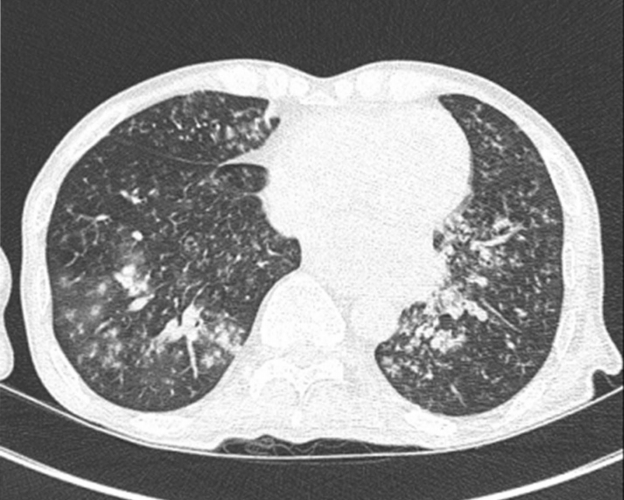
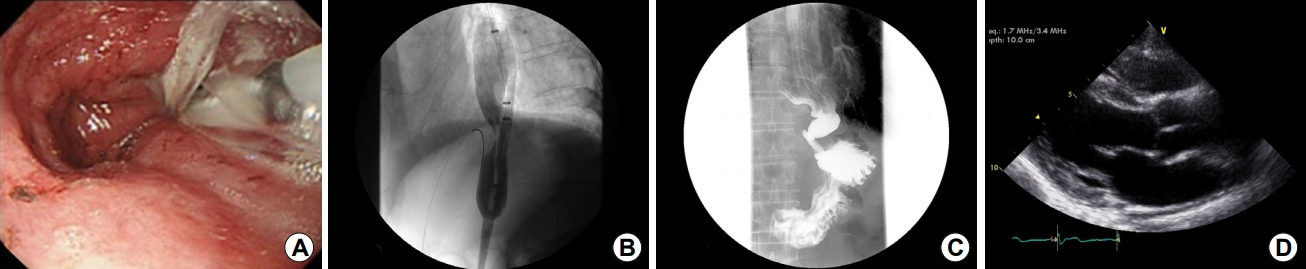
Fig. 4.
Transthoracic echocardiography shows a collapse of the left atrium by extrinsic compression due to an extracardiac mass lesion with heterogenous densities. The esophagus (*) is identified by echocardiographic appearance as a retrocardiac mass with air and a fluid level.

Fig. 5.
(A, B) After passage of a guidewire, a balloon is placed and inflated to dilate the narrowing of the esophagogastric junction (30 mm diameter) for 90 seconds. (C) After pneumatic dilatation, the contrast media shows good passage. (D) Transthoracic echocardiography shows a disappearance of the left atrial compression caused by the dilated esophagus.
REFERENCES
3. Eckardt VF, Hoischen T, Bernhard G. Life expectancy, complications, and causes of death in patients with achalasia: results of a 33-year follow-up investigation. Eur J Gastroenterol Hepatol 2008;20:956â960.


4. Makharia GK, Seith A, Sharma SK, et al. Structural and functional abnormalities in lungs in patients with achalasia. Neurogastroenterol Motil 2009;21:603âe20.


5. Hifumi T, Okada I, Inoue J, Koido Y. Cardiopulmonary arrest owing to oesophageal achalasia recovered completely with cardiopulmonary resuscitation followed by therapeutic hypothermia. BMJ Case Rep 2013;2013:bcr2012008378.



6. van Rooijen JM, van den Merkhof LF. Left atrial impression: a sign of extra-cardiac pathology. Eur J Echocardiogr 2008;9:661â664.



7. Mabvuure NT, Hey SY, Forshaw M. Recurrent respiratory distress and cardiopulmonary arrest caused by megaoesophagus secondary to achalasia. Int J Surg Case Rep 2014;5:628â632.



8. Kahrilas PJ, Boeckxstaens G. The spectrum of achalasia: lessons from studies of pathophysiology and high-resolution manometry. Gastroenterology 2013;145:954â965.


9. Jeon HH, Kim JH, Youn YH, Park H, Conklin JL. Clinical characteristics of patients with untreated achalasia. J Neurogastroenterol Motil 2017;23:378â384.




10. Adams CW, Brain RH, Ellis FG, Kauntze R, Trounce JR. Achalasia of the cardia. Guys Hosp Rep 1961;110:191â236.

11. Eckardt VF. Clinical presentations and complications of achalasia. Gastrointest Endosc Clin N Am 2001;11:281â292.


12. Schalinski S, Guddat SS, Tsokos M, Byard RW. Megaesophagus and possible mechanisms of sudden death. J Forensic Sci 2009;54:216â219.


13. D'Cruz IA, Feghali N, Gross CM. Echocardiographic manifestations of mediastinal masses compressing or encroaching on the heart. Echocardiography 1994;11:523â533.


14. Bruijns SR, Hicks A. Achalasia: an unusual cause of airway obstruction. Emerg Med J 2009;26:148.


15. Altintoprak F, Degirmenci B, Dikicier E, et al. A case of achalasia presented with cardiopulmonary arrest. Case Rep Surg 2012;2012:794858.




17. Inoue H, Sato H, Ikeda H, et al. Per-oral endoscopic myotomy: a series of 500 patients. J Am Coll Surg 2015;221:256â264.


18. Zaninotto G, Bennett C, Boeckxstaens G, et al. The 2018 ISDE achalasia guidelines. Dis Esophagus 2018;31:1â29.


-
METRICS

-
- 0 Crossref
- 2,814 View
- 63 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
A Case of Duodenal Volvulus Presenting with Recurrent Vomiting in Elderly2015 June;15(2)
A Case of Amyloidosis Presenting as Lymphadenopathy at the Porta Hepatis2018 September;18(3)






