한국인 헬리코박터 파일로리 감염 치료 근거 기반 임상진료지침 개정안 2020
Evidence-based Guidelines for the Treatment of Helicobacter pylori Infection in Korea: 2020 Revised Edition
Article information
Trans Abstract
Helicobacter pylori (H. pylori) infection is one of the most common infectious diseases worldwide. Although its incidence is gradually decreasing, about half of the world's population still get infected. H. pylori infection is responsible for substantial gastrointestinal morbidity worldwide. It is the most common cause of gastric and duodenal ulcers as well as gastric cancer. Since the revision of the H. pylori Clinical Practice Guidelines in 2013, the eradication rate of H. pylori has gradually decreased with the use of classical triple therapy, wherein amoxicillin, clarithromycin, and proton pump inhibitors are administered, for 7 days. According to a nationwide randomized controlled study conducted by the Korean College of Helicobacter and Upper Gastrointestinal Research released in 2018, the intention-to-treat eradication rate was only 63.9%, which was due to increased antimicrobial resistance induced by the use of antibiotics, especially clarithromycin. The update of clinical practice guideline for treatment of H. pylori was developed based on evidence-based medicine by conducting a meta-analysis. The draft recommendations were finalized after expert consensus on three recommendations regarding the indication for treatment and eight recommendations on the treatment itself. These guidelines are designed to provide patients, nurses, medical school students, policymakers, and clinicians with clinical evidence to guide primary care and treatment of H. pylori infection. These may differ from current medical insurance standards and will be revised further, if necessary, based on research-based evidence.
서 론
1. 배경
헬리코박터 파일로리(Helicobacter pylori, H. pylori) 감염은 전 세계적으로 가장 흔한 감염성 질환의 하나로 지역마다 유병률이 다양하여 북유럽에서는 11%, 캐나다와 미국에서는 각각 23.1%, 30%로 낮으나 남미 72~82%, 나이지리아에서는 91%를 육박하며[1] 국내 유병률도 50% 내외로 높다[2]. H. pylori는 만성 위염부터 소화성 궤양, 위축성 위염 및 장상피화생, 위 암까지 다양한 위장 질환을 유발한다. 특히 한국, 일본, 중국을 포함한 극동 아시아는 H. pylori 감염률이 높으면서 위암 발생률이 높은데, 2017년 국내 암등록 통계 자료에 의하면 위암 표준화 발생률이 인구 100,000명당 32명으로 갑상선암을 제외한 전체 암종 중에 가장 높았다[3]. 일본의 경우, H. pylori 양성 위염의 제균 치료를 건강보험 급여로 인정하면서 사실상 H. pylori 양성인 모든 대상자를 제균 치료하도록 권장하고 있다[4]. 그러나 전 인구의 절반 정도에서 감염되어 있으나 일부(<5%)에서만 위암이 발생하는 상황에서[5] H. pylori를 치료하기 위하여 여러 종류의 광범위 항생제를 투여하는 것에 대한 임상 근거가 확실치 않고, 높은 비용이 요구되며 항생제 내성 증가 가능성이 있어 위해(harm)에 비하여 확실한 이득(benefit)이 있다는 근거는 없다. 그러므로 국내 실정에 맞는 적절한 H. pylori 제균 치료의 적응증을 확립할 필요가 있다.
2013년에 발표된 H. pylori 진단 및 치료에 대한 임상진료 지침은 국외의 진료지침을 수용·개발하는 방법으로 국내 상황에 맞도록 제정하였으나, 그 개발 방법에 제한점이 있었다. 이번 개정안에서는 H. pylori 제균 치료가 필요한 환자 중 논란의 여지가 있던 철결핍성 빈혈, 위선종 제거 후, 위축성 위염 및 장상피화생에서 제균 치료가 필요한가에 대한 체계적 문헌 고찰을 시행하여 그 근거를 생성하고자 하였다.
H. pylori 제균 치료는 적절한 항생제와 산분비억제제의 조합을 이용하며, 제균율이 80% 이상 되어야 한다[6]. 최근 일차 치료로 사용되어 온 표준3제요법(양성자펌프억제제[proton pump inhibitors, PPIs]+amoxicillin+clarithromycin) 7일 치료는 제균율이 80% 미만으로 감소하였는데, 제균율 저하의 주요 원인은 clarithromycin 항생제 내성 때문이다[7]. Clarithromycin은 상기도 감염에 흔히 사용되는 광범위 항생제로서, 내성률이 15% 이상으로 높은 지역에서는 clarithromycin을 포함하는 3제 요법은 H. pylori 제균율이 낮아 권장되지 않는다[8]. 전 세계적으로 clarithromycin 내성률이 증가하고 있는데 북미 10%, 아시아 태평양 지역 17%, 유럽이 18%이며, 국내에서도 1995년 9%, 2003년 13.8%, 2005년 16.7%로 증가하는 추세이다[9-11]. 2018년 대한상부위장관·헬리코박터학회 주도 연구에서도 내성률이 17.8%였으나[2] 내성 검사를 시행하는 지역과 colony 수에 따라 30% 이상으로 측정되는 지역이 있어 clarithromycin 내성이 제균율 감소의 주 원인으로 뽑힌다[12]. 한편 metronidazole은 2000년대 초반까지 내성률이 60% 내외로 높은 양상을 보였으나[9], 2018년 대한상부위장관·헬리코박터학회 주도 연구에서는 29%로 낮아져 있었으며 내성이 있는 경우 기간을 늘리거나 높은 용량으로 사용 시 좋은 효과가 있다는 보고들이 있어 clarithromycin 내성률을 극복할 수 있는 대안이 될 수 있다[2].
표준3제요법의 제균율이 감소하면서 다양한 약제 조합과 약제 투여 기간이 다른 제균 치료법이 소개되었다. 이번 진료지침에서는 표준3제요법 7일 치료의 대안으로서 다양한 치료법에 대한 임상 근거를 알아보기 위하여 체계적 문헌 고찰과 메타분석을 시행하여 한국에 적절한 H. pylori 대상과 효과적 치료법을 제시하고자 한다.
2. 임상진료지침의 대상, 범위, 목적 및 사용자
본 진료지침은 H. pylori 감염이 있는 성인 남녀를 대상으로, H. pylori 감염과 연관되어 일상생활에 불편을 겪고 있거나 연관된 질환을 가지고 있는 환자들을 대상으로 한다. 본 지침의 목적은 제균 치료가 필요한 임상 적응증을 정의하고, H. pylori 제균 약제 투여로 인한 부작용 및 내성률 발현은 최소화하면서 제균율을 극대화할 수 있는 적절한 일차 치료법 및 구제 치료법을 제시하여, 궁극적으로 H. pylori와 연관된 위염, 소화성 궤양 및 악성 위장관 질환 등 상부위장관 질환을 치료하고 예방하는 것이다.
임상진료지침의 범위는 진료지침 개발 그룹에서 명목집단기법으로 Patient Intervention Comparatives Outcomes (PICO) 형식에 맞춘 핵심질문 도출을 통하여 결정하였고 그 구체적인 내용은 표에 정리하였다.
본 진료지침은 H. pylori 감염을 진단하고 치료하는 내과 의사, 가정의학과 의사 및 일차 진료의뿐만 아니라 약사, 간호사, 내시경 검사 인력 및 병리 기사 등 보건의료종사자가 임상에서 의사 결정을 수행할 때 사용할 수 있다. 또한 교육 목적으로 의과대학, 약학대학 및 간호대학 학생, 내과 및 가정의학과 수련의, 간호사 및 의료 기사도 사용할 수 있다. 또한 H. pylori 연관 질환의 진료 및 치료가 필요한 환자 및 일반인도 이용할 수 있으며, H. pylori 치료에 대한 임상 근거를 바탕으로 최적의 지침 개발을 통하여 건강보험 적용 등에 대한 정책 결정의 표준을 제시하고자 한다.
3. 임상진료지침 위원회 구성
임상진료지침 운영위원회는 대한상부위장관·헬리코박터학회 회장 및 임원진을 중심으로 구성하여 진료지침 개발과 관련된 개발전략을 수립하고 실무위원장을 선임하였으며, 사업과 연관된 예산을 검토하고 승인하였다. 본 지침은 대한상부위장관·헬리코박터학회에서 모든 예산을 지원받았으나 이외 별도의 재정 후원은 없었으며, 학회의 재정 후원이 지침 개발에 영향을 주지 않았다. 지침 개발 실무팀은 H. pylori 관련 전문가인 소화기내과 의사를 중심으로 지역적 안배를 고려하여 위원장(정혜경), 간사(강승주) 및 위원(양효준, 박선영, 신철민, 김성은, 임현철, 김지현, 남수연, 신운건, 박재명, 최일주)으로 구성하였고, 근거의 선택, 검색 및 등급화를 시행하고 최종 권고안을 도출하였다. 지침 개발의 방법론 확립을 위하여 방법론 전문가 2명(신인순, 최미영)과 대한의학회 임상진료지침 전문위원인 김수영 교수가 문헌 검색 및 문헌의 질 평가, 메타분석의 실제, 임상진료 지침 근거와 권고 등급 설정, 전문가 합의에 관한 4회의 워크숍을 시행하였다. 본 진료지침은 대한소화기학회, 대한병리학회 및 대한임상미생물학회 등 위원을 포함하여 다학제 위원회를 구성하여 지침 개발 과정을 수행하였다.
4. 환자나 일반인의 관점과 선호도
진료지침 적용 대상인 환자 혹은 일반인의 경험과 기대, 선호도를 반영하기 위하여 위장 질환과 연관된 최대 인터넷 커뮤니티를 통하여 구조화된 설문지로 H. pylori 치료에 관한 설문조사를 일반인들에게 실시하였다. 총 233명이 응답하였고, 응답자의 64.4%가 성인 여성이었으며 H. pylori 양성인 경우가 57.5%였다. H. pylori 양성인 경우 치료 의향이 있는 경우가 86.7%였고, 이 중 제균 치료를 하고 싶은 이유는 위암 예방 목적 44.6%, 위장 증상 호전 28.8%, 타인에게 전염 우려가 9.9%였다. H. pylori 제균 치료에 대하여 가장 걱정스러운 점은 약제 부작용이 80.3%였다. 이러한 점에 근거하여 H. pylori로 인한 위암 발생의 전구 병변인 위축성 위염과 장상피화생이 제균 치료의 적응이 되는지 및 약물 치료 부작용 부분을 개발 주제에 추가하였다.
5. 임상진료지침 초안에 대한 내외부 검토 및 자문
최종 도출된 권고안을 바탕으로 실무위원회에서 초안을 작성하여 실행위원회 및 운영위원회에서 내부 검토를 수행하였고, 환자의 가치와 선호도, 촉진 요인과 장애 요인에 대하여 비임상 전문가를 포함한 외부 검토를 수행하였다. 검토 과정에서 도출된 의견 및 검토 의견의 반영 결과를 정리하였다.
6. 임상진료지침 보급 및 확산
본 지침은 대한상부위장관·헬리코박터학회(http://www.hpylori.or.kr), 대한내과학회(http://www.kaim.or.kr)의 웹사이트에서 지침안을 볼 수 있도록 하였다. 또한 본 임상진료지침은 국내외 H. pylori 제균 치료와 연관된 주제에 대한 메타분석을 시행하여 아시아 및 전 세계적 근거를 요약한 것으로 학회지에 게재하여 지침안을 볼 수 있도록 하였고 학회 트위터, 페이스북 등 소셜미디어를 통하여 이용이 가능하도록 하였다.
7. 임상진료지침 갱신 계획
본 임상진료지침은 2013년 발표된 ‘한국인 헬리코박터 파일로리 감염의 진단과 치료 임상진료지침’의 개정안으로 H. pylori 진단과 치료에 영향을 줄 정도의 임상 근거가 축적되거나, 새로운 권고안의 추가나 기존 권고안의 수정과 보완이 필요하다고 판단되는 경우, 추후 5년 전후의 기간 간격으로 개정할 예정이고, 개정 작업은 대한상부위장관·헬리코박터학회를 중심으로 진행할 예정이다.
8. 지침 개발자의 이해 상충
지침 개발 실무위원에게 진료지침 개발이나 승인 과정에서 상업적으로 관련이 있는 조직에서 자문 혹은 고용 여부, 상업적 소유 지분이나 연구비, 사례비 등을 수용하여 이해관계에 상충되는 점은 없는지, 지침 개발 내용과 관련된 약제에 대한 지적재산권(예: 특허, 상표권, 라이센싱, 로열티 등) 소유 여부, 본인의 가족 또는 가족이 소속된 회사에서 위에 기술된 것과 같은 관계를 가지고 있는지에 대한 내용을 문건으로 서명하여 확인하였고 참여위원 전원이 이해상충이 없음을 확인하였다.
본 론
1. 헬리코박터 파일로리 치료에 대한 임상진료지침 개정 방법
최근 국내 H. pylori 감염 및 관련된 위장관 질환의 역학과 항생제 내성률이 급격히 변화하는 추세이기 때문에 최신의 근거가 필요하여 이번 지침의 개정은 신규 직접(de novo) 개발을 시행하였다.
1) 핵심질문 도출
핵심질문을 도출하기 위하여 지침 개발 실무팀에서 기존 진료지침을 검색하고 대면회의를 통하여 H. pylori 치료의 대상이 되는 적응증과 치료에 대한 주제를 선정하였다. 이후 담당 실무위원을 정한 뒤, 다음 대면회의에서 각 주제에 타당한 PICO를 정한 뒤 토론 과정을 통해 최종 12개를 선정하였다. 주제 선정에 있어 환자선호도를 반영하기 위하여 국내 위장관 질환 관련 인터넷 커뮤니티에서 H. pylori 감염 치료와 연관된 일반인의 의견, 지침의 범위 등에 관한 조사를 실시하여, 위암의 전구 병변, 즉, 위선종 및 위축성 위염/장상피화생에서 H. pylori 제균 치료의 효과와 H. pylori 제균 치료 부작용에 대한 권고안을 선정하였다.
2) 문헌 검색 및 문헌의 질 평가
지침의 근거가 되는 연구 문헌을 검색하기 위하여 각 주제별 체계적 문헌 고찰을 실시하였다. 한국보건의료원 최미영 박사와 각 주제별 실무위원이 적절한 검색어를 선정하여 Ovid-MEDLINE, EMBASE, Cochrane Library, KoreaMed 및 KMBASE에서 2018년 8월까지 출판된 문헌들을 주제별로 검색을 실시하였고 (Fig. 1) 검색의 공통된 선정기준은 1) 성인을 대상으로 한 연구, 2) 영어 혹은 한국어로 기술된 문헌, 3) 관찰 연구, 무작위 대조군 연구(randomized controlled trial, RCT), 체계적 문헌 고찰 및 메타분석, 4) 2008년부터 2018년까지 발행된 연구, 5) 적절한 결과(제균율, 부작용 빈도, 증상 호전, 위암 발생 등)가 보고된 경우로 하였다. 공통된 제외기준은 1) 소아나 청소년을 대상으로한 연구, 2) 적절한 결과(제균율, 부작용 빈도, 증상 호전, 위암 발생 등)가 보고되지 않은 연구, 3) 영어나 한국어 이외의 언어로 기술된 문헌, 4) 중복으로 게재된 경우(동일 내용으로 다른 저널에 게재 혹은 출판 형태만 차이가 있는 경우), 5) 원문 확보가 불가능한 경우, 6) 전문가 의견이나 증례보고, 종설, 진료지침 등이었다. 각 주제별로 위원 2인이 한 조가 되어 근거 문헌을 선택하였고, 포함 여부가 불분명할 때에는 지침개발그룹 회의에서 포함 여부를 논의하였다. 각 주제별로 Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA)에서 제시한 문헌 선택 흐름도를 사용하여 문헌 선택 과정을 정리하였다(Fig. 1).
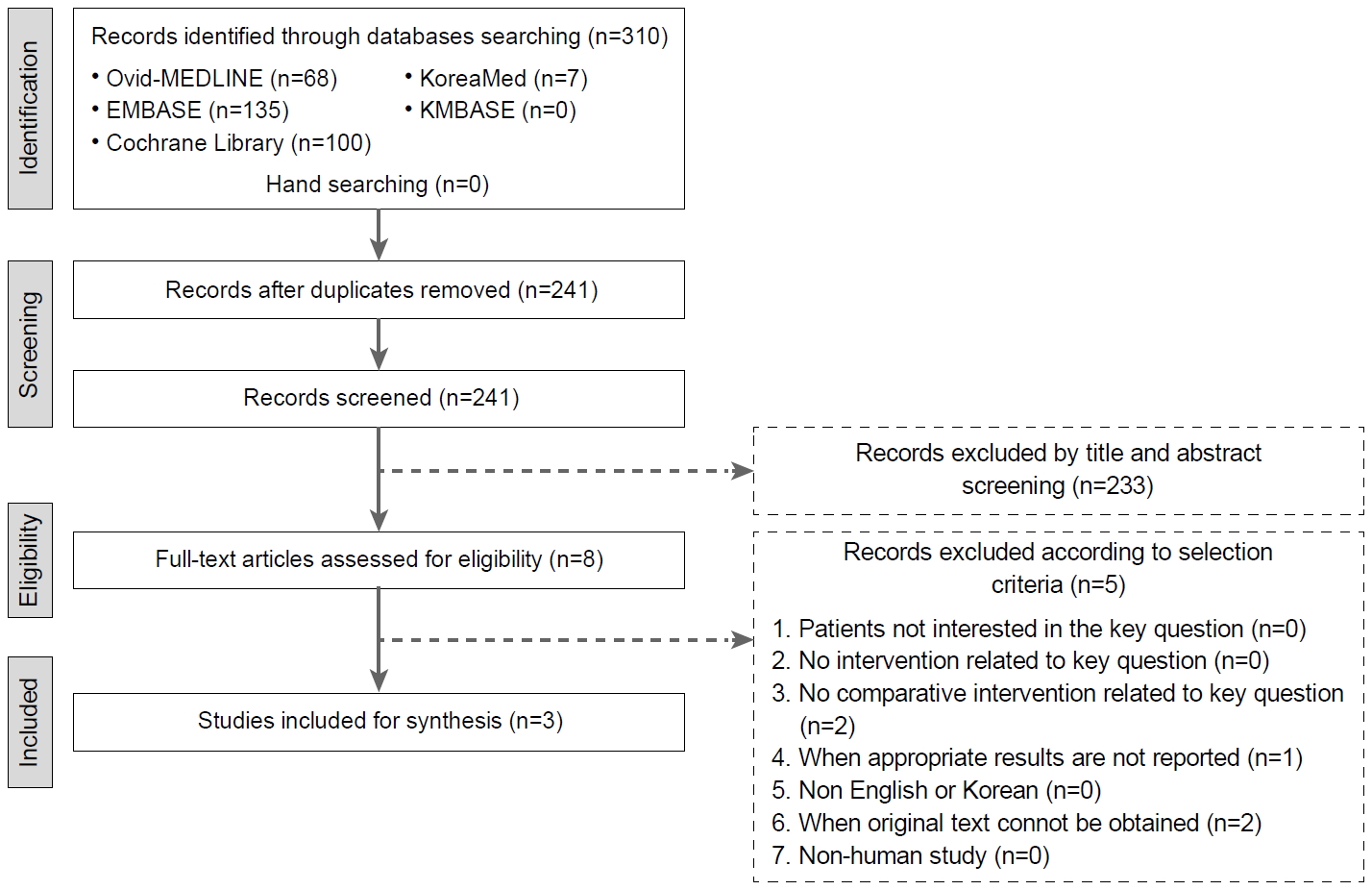
Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) flow chart shows the selection process for key question 1.
최종 선택된 문헌의 연구설계에 따라 무작위 배정 임상시험 연구는 Cochrane의 Risk of Bias (RoB) [13] 도구를 사용하였고, 비무작위 연구는 Risk of Bias Assessment tool for Non-randomised Study (RoBANS) [14]를 사용하여 평가하였다. 짝지어진 두 명의 실행위원이 1차 판정을 수행하여 결과가 일치하지 않는 경우 두 위원과 지침위원장이 논의하여 최종 평가를 시행하였다.
3) 권고안 도출: 근거 수준 및 권고 강도 결정
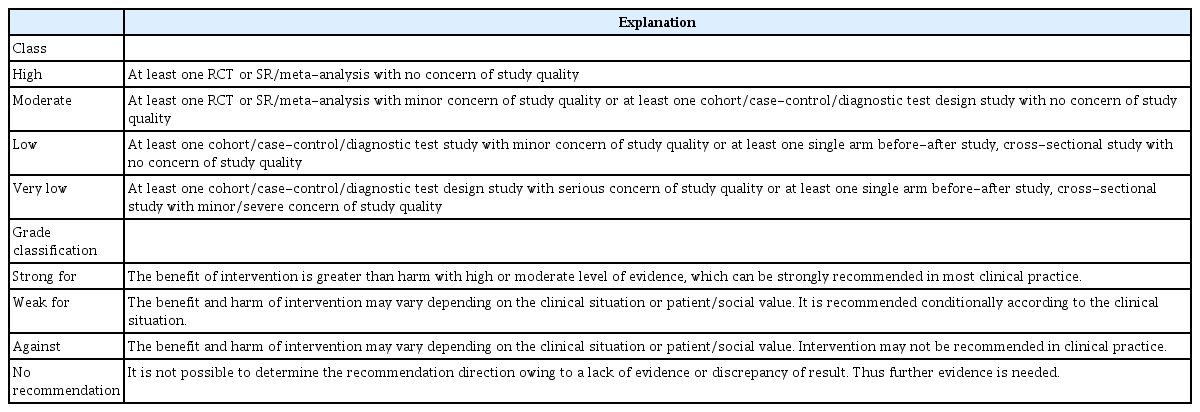
체계적 문헌 고찰을 통하여 최종 선택된 문헌을 바탕으로 사전에 작성된 근거표에 정리하였고, 이를 바탕으로 메타분석을 시행하였다. 근거 수준과 권고 강도(strength of recommendation)는 The Grading of Recommendations, Assessment, Development and Evaluation (GRADE) 방법론을 이용하였다(Table 1) [15]. 근거 수준은 4등급으로 세분하였는데, 연구 디자인과 근거의 질을 주로 평가하였고, 비뚤림 위험, 일관성, 직접성, 정밀성, 출판 비뚤림 등을 고려하였다. 권고 강도는 강한 권고, 약한 권고, 권고하지 않음, 미결정의 4단계로 분류하였다. 권고 강도는 대상자에게 해당 중재를 시행하였을 때 위해보다 이득이 더 클 것으로 혹은 작을 것으로 확신하는 정도를 의미하며, 권고 결정 고려요소로는 근거 수준, 효과 크기(이득과 위해의 정도 비교), 환자의 선호도와 가치, 자원 이용을 종합적으로 판단하였다[16]. 이 지침에서 제시되는 권고문들은 Table 2에 정리되어 있다.
자원 및 경제성 근거를 활용하기 위하여 문헌 검색을 실시하였고, 환자선호도를 반영하기 위하여 비용에 대한 설문을 실시하였다. H. pylori 제균 치료는 항생제 및 PPI를 7~14일 단기간 조합으로 사용하는데, 각 치료 방법 간의 비용의 차이는 크지 않다. 설문조사에서 환자에게 H. pylori 제균 치료에 드는 약제 비용이 부담되는지에 대하여 질문하였는데, 응답자의 8.2%에서만 비용이 부담이 된다고 응답하였다. H. pylori 맞춤 제균 치료법(tailored therapy based on antibiotics-susceptibility test)은 항생제 내성 여부를 제균 치료 전에 검사하는 방법으로 주로 clarithromycin 내성 검사를 시행하는데, 고비용이 드는 검사 방법이나 제균율이 75.3% 이하로 낮아지면 오히려 맞춤 치료가 비용-효과면에서 우월하다는 보고가 있다[17,18].
4) 전문가 합의
핵심 질문별 권고안의 합의를 위하여 합의 방법에 대한 워크숍을 실시한 후 수정 델파이 방법으로 합의안을 도출하였다. 1차 합의를 위하여 H. pylori 질환의 전문가 44명을 초대하였고 30명이 참여에 동의하여 이메일을 통해 조사하였다. 1차 설문은 각 권고안과 그 근거를 제시한 자료에 대하여 동의 정도를 묻는 9-Likert scale의 자가 보고형 설문지를 이용하여 조사하였다. 응답 척도는 1점이 ‘전혀 동의하지 않는다’에서 9점 ‘매우 동의한다’까지이며, 7~9점(고합의)의 비율이 2/3 이상이면서 비동의가 없는 경우를 동의로 간주하였다. 1차 합의에서 총 12개의 권고안에 대하여 8개가 합의되었고, 치료 적응증에서 빈혈 및 위축성 위염/장상피화생, 치료 방법에서 표준3제요법, 순차 치료가 동의에 이르지 못하여, 개발위원회에서 권고안을 수정하여 대면 합의로 2차 투표를 실시하였다(2019년 12월 14일). 수정된 2차 권고안의 근거에 대한 발표 후 무기명으로 2차 투표를 실시하였으며, 위축성 위염/장상피화생에 대한 권고안은 23명 중 48%의 찬성으로 기각되었고 나머지 권고안은 통과되어 최종적으로 11개의 권고안이 채택되었다.
5) 내외부 검토
전문가 합의 과정을 위한 2차 대면 투표에서 무기명 투표 후 초안에 대한 다양한 의견이 제시되었고 이를 바탕으로 가능한 범위에서 수정한 후 외부 전문가 검토를 시행하였다.
2. 헬리코박터 파일로리 제균 치료의 적응증
1) 철결핍성 빈혈(iron deficiency anemia)
헬리코박터 파일로리 제균 치료는 원인 미상의 철결핍성 빈혈 환자에서 혈색소를 증가시키는가?
지침 1. 헬리코박터 감염 제균 치료는 원인 미상의 철결핍성 빈혈을 가진 성인의 일부에서 도움이 될 수 있다.
∙ 권고 강도: 약함
∙ 근거 수준: 매우 낮음
∙ 전문가 합의: 76.0% (2차), 56.7% (1차)
빈혈은 유병률이 높고 다양한 전신 증상을 유발할 수 있는 질환으로 대부분이 철결핍성 빈혈이다[19,20]. 전 세계적으로 빈혈의 유병률은 24.8% (95% CI, 22.9~26.7%)로 약 16억 2천만명(95% CI, 15억 명~17억 4천만 명)에 해당하며[19], 미취학 어린이와 여성에서 호발한다. H. pylori는 만성 위염, 소화성 궤양 및 악성 질환 등 다양한 위장 질환을 유발하고, 특히 H. pylori 감염으로 인한 만성 위염은 철분 흡수에 반드시 필요한 위산 분비와 위 내 아스코르브산을 감소시킨다[6,21].
H. pylori와 철결핍성 빈혈과의 관련성에 대한 근거는 아래의 연구 결과에 토대를 두고있다. 최근 발표된 메타분석에서 H. pylori 감염이 있는 군은 없는 군에 비하여 철결핍성 빈혈이 동 반될 교차비(OR)가 1.72 (95% CI, 1.23~2.42)로 높았다[22]. 그러나 메타분석에 포함된 대부분의 연구가 소아와 청소년을 대상으로 한 연구였으며, 성인만을 대상으로 한 하위 분석에서는 OR 1.70 (95% CI, 1.01~2.85)으로 통계적인 유의성은 관찰되었으나 심한 이질성(heterogeneity)을 보였다[19]. 철결핍성 빈혈에서 H. pylori 제균 치료 후 빈혈이 교정되는가에 대한 연구는 많지 않고 이질성이 높으며, 연구 대상자가 소아이거나 청소년, 여성(임신 vs. 비임신)과 같은 특정군을 대상으로 한 연구여서 전체 성인에게 일반화하기 어려운 점이 있다. 또한, 제균 치료 후 빈혈의 호전 정도를 보는 연구 종료점이 ferritin이나 혈색소의 정량적 측정, 빈혈의 회복과 같은 정성적 측정 등 연구마다 다양하였다. 소아, 청소년 및 성인이 모두 포함되고 연구 종료점을 ferritin 상승으로 설정한 7개의 무작위 전향적 환자-대조군 연구를 바탕으로 한 메타분석에서 ferritin 상승의 표준화 평균 차이(standardized mean difference, SMD)는 0.53 (95% CI, 0.21~0.85)으로 의미 있는 상승을 보였으나 혈색소 상승의 SMD는 0.36 (95% CI, -0.07~0.78)으로 유의한 차이가 없었다[22].
본 지침에서 선정한 핵심 질문에 해당하는 성인 철결핍성 빈혈 환자에서 H. pylori 제균 치료 효과에 대한 연구는 매우 제한적이다. H. pylori 양성 만성 위염이 있으면서 철결핍성 빈혈이 있는 성인에서 제균 치료가 일반적인 빈혈 치료에 추가적인 빈혈 개선 효과가 있는지를 본 비무작위 대조군 연구가 있고 [23], H. pylori 감염이 있으면서 ferritin이 낮은 성인을 대상으로 제균 후 혈청 ferritin 상승을 본 전향적 관찰 연구가 있으나 연구 대상자수가 적었다는 제한점이 있다 [24]. 하지만 이 연구에서 H. pylori 감염군에서 유의하게 철결핍성 빈혈이 호발하였고, 제균 치료 후 ferritin이 상승하거나 빈혈이 소실되었다[24]. H. pylori 감염이 있는 88명의 환자에서 제균 치료 후 철결핍성 빈혈이 38.1%에서 소실되었고, 특히 남성과 폐경 후 여성에서 폐경 전 여성에 비하여 유의하게 빈혈 소실률이 높았다(75% vs. 23%, P<0.01) [25]. 근거 수준이 매우 낮음에도 불구하고, 단기간 H. pylori 제균 치료로 장기적으로 빈혈이 교정되는 이득의 가능성이 있고 위해가 크지 않아 ‘약한 권고’로 결정하였다.
2) 위선종 내시경 절제 후 상태
위선종의 내시경 절제 후 헬리코박터 제균 치료는 이시성 위암의 발생 예방에 도움이 되는가?
지침 2. 헬리코박터 양성 위선종 환자에서 내시경 절제 후 이시성 위암의 발생 예방을 위해 헬리코박터 제균 치료를 권고 할 수 있다.
∙ 권고 강도: 약함
∙ 근거 수준: 낮음
∙ 전문가 합의: 80.0% (1차)
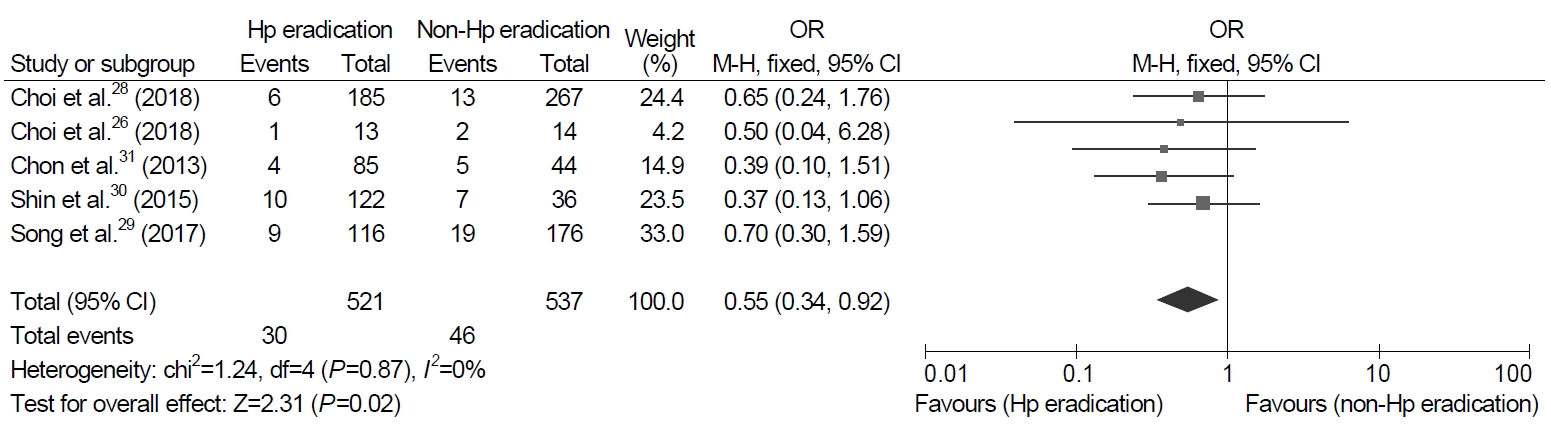
많은 연구들에 따르면 조기 위암의 내시경 절제술을 받은 환자에서 H. pylori 제균 치료 후 이시성 위암의 발생률이 감소하였다[26-28]. 따라서 조기 위암의 내시경 절제술 후 이시성 위암의 발생 감소를 위해 제균 치료는 시행되어야 한다. 그러나 위선종의 내시경 절제 후의 H. pylori 제균 치료에 대해서는 명확한 지침이 없다. 지금까지 조기 위암 및 선종을 포함한 위종양의 내시경 절제술 후 이시성 위암의 발생을 예방하기 위한 제균 치료에 관한 두 개의 RCT가 있었다[26,28]. 위선종의 내시경 절제 후 이시성 병변의 예방을 위한 H. pylori 제균 치료에 관한 후향적 연구는 3개가 있었는데, 이들 모두 국내에서 수행된 연구들이다(Supplementary Table 1) [29-31]. 이들 연구들에 따르면 H. pylori 제균 치료 후 이시성 위암의 발생률은 제균되지 않은 군 보다 낮았다(3.2% vs. 4.9%; 7.7% vs. 14.3%; 7.8% vs. 10.8%; 8.2% vs. 19.4%; 4.7% vs. 11.4%). 위의 5건의 연구를 포함한 메타분석에서 위선종의 내시경 절제 후 이시성 위암의 발생 예방에 대한 제균 치료의 효과는 통계적으로 유의하였다(OR, 0.55; 95% CI, 0.34~0.92) (Fig. 2). 이는 H. pylori 제균 치료는 위선종의 내시경 절제 후 이시성 위암의 발생을 예방하는 데에 도움이 됨을 시사한다. 따라서 H. pylori 양성 위선종 환자에서 내시경 절제 후 H. pylori 제균 치료가 권고된다. 하지만, 위선종 환자만을 대상으로 한 RCT가 아직 없어 이에 대한 연구가 필요하다.
3) 기능성 소화불량증
헬리코박터 파일로리 양성인 기능성 소화불량증 환자에서 제균 치료는 장기적인 증상 개선에 도움이 되는가?
지침 3. 헬리코박터 제균 치료는 기능성 소화불량증의 장기적인 증상 완화에 도움이 되기 때문에 권고할 수 있다.
∙ 권고 강도: 약함
∙ 근거 수준: 높음
∙ 전문가 합의: 70.0% (1차)
RCT들의 메타분석에서 기능성 소화불량증 환자에서 H. pylori를 제균하였을 때, 단기간(3개월) 추적 관찰 시 증상 개선 효과는 유의하지 않았지만, 장기간(6~12개월) 추적 관찰에서 유의하게 증상이 개선되었다[32,33]. 이 결과를 바탕으로 유럽의 Maastricht V 가이드라인과 미국과 캐나다 가이드라인에서는 소화불량증의 일차적인 치료로 H. pylori 제균 치료를 강력히 권고하고 있다[34,35].
본 지침에서는 소화불량증 환자에서 H. pylori 제균 치료의 장기 효과를 평가하기 위하여 1997년 1월부터 2017년 12월까지 18개의 RCT를 선택하여 메타분석을 시행하였다[36-53]. 총 18개 연구, 4,672명을 대상으로 시행한 메타분석에서 대조군이 제균 치료군에 비해 소화불량 증상이 지속될 위험도비(risk ratio, RR)가 1.18 (95% CI, 1.07~1.31)로 통계적으로 유의하였으나, 치료에 필요한 환자수(number needed to treat, NNT)가 14로 그 효과가 월등하지 않았고 연구 간의 이질성은 중등도였다(I2=34%) (Supplmentary Table 2, Supplementary Fig. 1) [54].
연구 간에 이질성이 있기 때문에 지역에 따라 하위 집단 분석을 시행하여 5개의 아시아 지역에서 나온 논문들과 13개의 아시아 외의 지역에서 나온 논문들을 분석하였다. 아시아 외 지역에서 나온 논문들을 분석하면 제균 치료는 유의한 이질성 없이 소화불량 증상의 개선 가능성을 유의하게 높였다(RR, 1.22; 95% CI, 1.08~1.38; I2=33%). 하지만 아시아에서 나온 연구들을 분석한 결과 제균 요법이 소화불량 증상 개선에 미치는 영향은 유의하게 높지 않았다(RR, 1.10; 95% CI, 0.92~1.31;I2=32%).
정리하면, 기능성 소화불량증에서 H. pylori 제균 치료는 통계적으로 유의하게 증상을 개선시켰으나 14명의 소화불량증 환자들 중 1명에서 제균 치료로 증상이 호전되는 정도여서(NNT=14) 임상 효과가 크다고 보기 힘들고, 아시아 지역에서 수행된 연구들의 하위 분석 결과는 통계적으로 유의하지 않았다. H. pylori 유병률을 전 세계적으로 추정한 논문에 따르면 국내 H. pylori의 유병률은 54% (95% CI, 50.1~57.8%)로 추정된다[55]. H. pylori 유병률이 높은 지역에서는 제균 요법과 관련된 비용과 부작용, 내성 균주의 출현 위험 및 재감염 위험이 유병률이 낮은 지역보다는 높을 것으로 생각되어 이번 지침에서는 소화불량증에서 H. pylori 제균 치료는 근거가 높음에도 불구하고 약한 권고를 하기로 결정하였다. 국내를 포함하여 H. pylori 유병률이 높은 지역에서 기능성 소화불량증 환자에서 제균 치료의 비용 효과 분석을 포함하는 RCT가 필요하다.
4) 만성 위축성 위염 및 장상피화생
헬리코박터 파일로리 양성이면서 위축성 위염, 장상피화생이 있는 경우 제균 치료를 하는 것이 위암 예방에 효과가 있는가?
H. pylori 제균 치료는 위암의 발생 위험을 줄인다고 알려져 있다. 하지만, 위축성 위염이나 장상피화생과 같이 전암성 병변을 가진 환자에서 제균 치료가 위암의 예방에 효과가 있는지에 대해서는 아직 논란의 여지가 있다.
최근에 발표된 두 개의 메타분석 결과에 따르면 전암성 병변이 전혀 없는 경우나 위축성 위염이 있는 경우에 H. pylori 제균 치료가 향후 위암의 발생 위험을 줄이지만 장상피화생이나 위선종이 있는 경우에는 위암의 발생 위험을 줄이지 못하였다[56,57]. 또한 제균 치료의 효과는 위축성 위염의 정도에 의해 영향을 받아 광범위한 위축성 위염을 가진 환자보다 경증의 위축을 가지고 있는 환자에서 H. pylori 제균 치료가 위암을 예방하는 데 더 효과적이었다[58]. 이 연구를 기반으로 Maastricht V 지침에서는 위축성 위염이나 장상피화생의 발생 전에 제균 치료를 함으로써 위암을 효과적으로 줄일 수 있다고 권고하고 있다[34].
하지만, 위에서 언급된 두 개의 메타분석은 일반인에 대한 연구뿐만 아니라, 조기 위암으로 내시경 절제술을 받은 환자에서 제균 치료 후 이시성 위암이 발생하였는지를 본 연구도 포함하고 있다. 제균 치료의 효과는 일반인군과 조기 위암으로 내시경 치료를 받은 고위험군에서 다를 수 있다. 또한 두 메타분석에 포함되지 않은 일반인을 대상으로 한 중국의 대규모 코호트 연구에 따르면 H. pylori 제균 치료는 장상피화생이 있거나 위선종이 있던 환자에서도 위암의 위험도를 줄였다[59]. 이 연구는 일반인을 대상으로 하였을 때는 장상피화생이 있어도 제균 치료가 위암 예방 가능성이 있음을 시사한다.
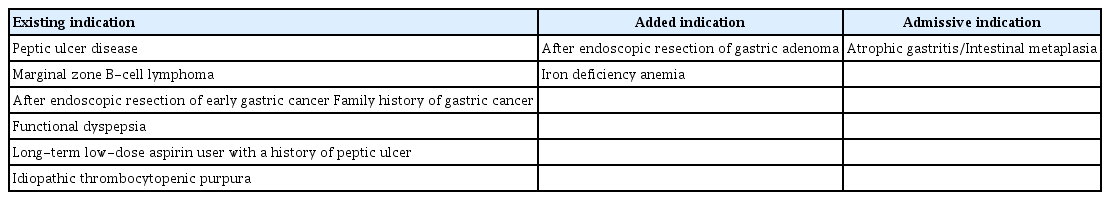
본 지침에서 일반 인구 집단을 대상으로 한 무작위 대조 연구만을 선택하여 메타분석을 시행한 결과, 기존 연구와 같이 H. pylori 제균 치료는 유의하게 위암의 발생을 감소시켰지만(Fig. 3), 위축성 위염이나 장상피화생을 가진 대상자만을 포함한 하위 분석에서는 제균 치료가 위암의 예방에 효과가 없었으며, 위축성 위염이나 장상피화생이 없는 대상자를 포함한 2개의 연구에서도 유의한 위암 예방 효과를 입증하지 못하였다(Supplementary Fig. 2). 그러나 후자의 경우, 위암의 발생건수가 작아 정확한 결론을 도출하는 데 제한점이 있다. 이 결과를 근거로 전문가 합의도출을 실시한 결과, 1차 이메일 설문에서 48.0%가 동의하였고, 2차 대면 합의에서는 63.3%만이 동의하였다. 즉, 위축성 위염이나 장상피화생에서 H. pylori 제균 치료를 권고하기에는 확실한 근거나 전문가 합의가 없어 추후 위축성 위염이나 장상피화생이 있는 일반 인구 집단에서 위암 예방에 H. pylori 제균 치료가 도움을 주는지에 대한 연구 결과가 축적된 후 재논의가 필요하다. 이상에서 제시된 H. pylori 제균 치료의 적응증들은 Table 3에 정리되어 있다.
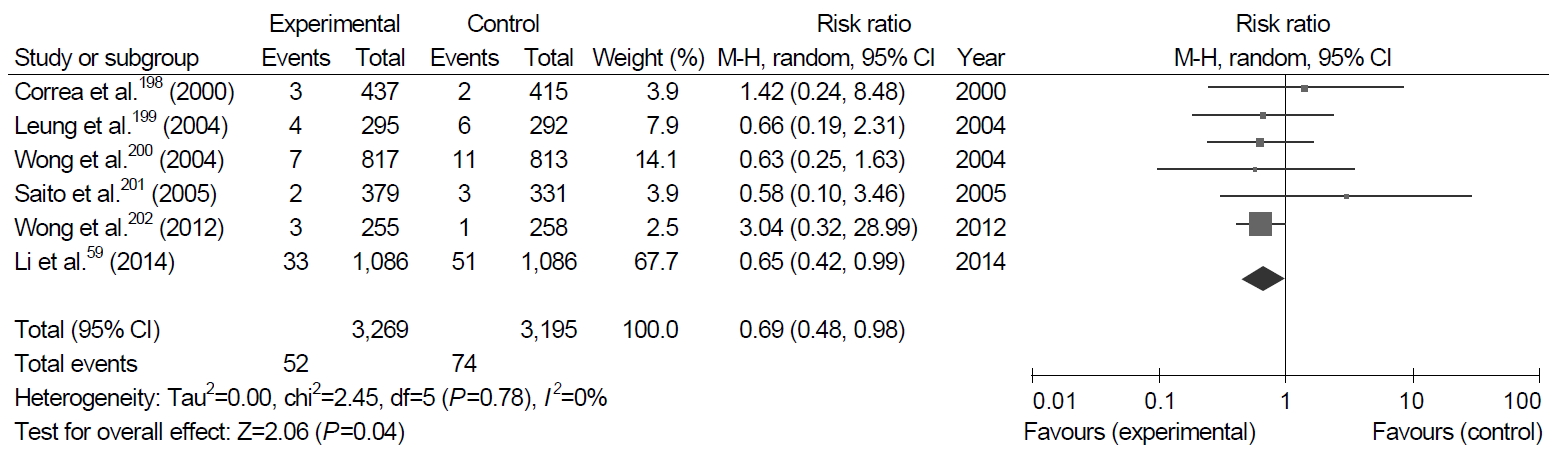
Forest plot of studies reporting gastric cancer in the eradication group and control group from studies assessing the general population. M-H, Mantel-Haenszel test.
3. 헬리코박터 파일로리 제균 치료 방법
1) 1차 치료
H. pylori 제균 치료를 처음 시행하는 환자에서 1) 표준3제 요법, 2) bismuth를 포함하지 않는 4제요법(순차 치료, 동시 치료 등), 3) clarithromycin 내성 검사 후 표준3제요법 선택, 4) 일부 환자에서 bismuth 포함 4제요법을 사용할 수 있다.
(1) 표준3제요법
표준3제요법은 헬리코박터 파일로리 감염의 1차 제균 치료로 사용될 수 있는가?
지침 4. 1차 제균 치료로 표준3제요법(양성자펌프억제제 표준 용량, amoxicillin 1 g, clarithromycin 500 mg 하루 2회) 14일 치료를 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 중간
∙ 전문가 합의: 77.0% (2차), 63.3% (1차)
1차 제균 요법의 적절한 선택을 위해서는 지역의 항생제 내성률과 약물 치료에 따른 제균율을 고려해야 한다. 제균 치료의 성공 여부에는 환자의 순응도, 항생제의 항균력에 영향을 줄 수 있는 PPI의 산분비 억제능 등 다양한 인자들이 관련되나, 가장 중요한 요인은 항생제 내성, 특히 clarithromycin 내성 유무이다. 한국에서 clarithromycin 내성률은 지난 10년 동안 점차 증가해왔으며, 최근의 연구에서는 17.8~31.0%로 높다[2,11]. 한국 내에서도 지역에 따라 clarithromycin 내성률은 차이를 보이고 있는데, 전국 항생제 내성률 조사에서 서울과 충청도 지역은 15% 미만이었으나 이 두 지역을 제외한 지역에서는 15% 이상의 내성률을 보였다[2]. 제균율을 기준으로 할 때, H. pylori 제균 치료에서 intention-to-treat (ITT) 제균율이 적어도 80% 이상이 되어야 초치료 요법으로서 추천할 수 있다[60].
본 지침에서는 한국에서 최근 10년간의 표준3제요법의 제균율을 구하기 위해 2007년 이후 표준3제요법을 이용한 RCT들을 대상으로 체계적 문헌 검색을 실시하였다. 사전에 정해진 선택기준과 제외기준에 따라 총 26개의 연구들이 선택되었다(Supplementary Table 3) [61-86]. 이 연구들로부터 도출된 표준3제요법의 ITT 제균율은 71.6% (95% CI, 69.9~73.3%)였고, per protocol (PP) 제균율은 79.6% (95% CI, 76.6~82.2%)였다(Fig. 4). 위의 연구들을 기간별로 나누면 2007년부터 2011년까지 ITT 제균율은 72.3% (95% CI, 71.2~74.4%), 2012년부터 2016년까지는 70.3% (95% CI, 68.4~72.1%)로 제균율이 감소하였다. 결과를 종합해 보면 표준3제요법의 제균율은 유의하게 감소하여 ITT 제균율은 71.6%로 초치료로 사용하기에 부적절하였다. 이는 2018년 대한상부위장관・헬리코박터학회에서 시행한 전향적 무작위 연구와 유사한 결과였다[87]. 따라서 7일 표준3제요법의 ITT 제균율이 80%보다 낮아 초치료로 사용하기 위해서는 clarithromycin 감수성 검사를 도입하거나 다른 제균 치료를 선택할 것을 고려해야 한다.
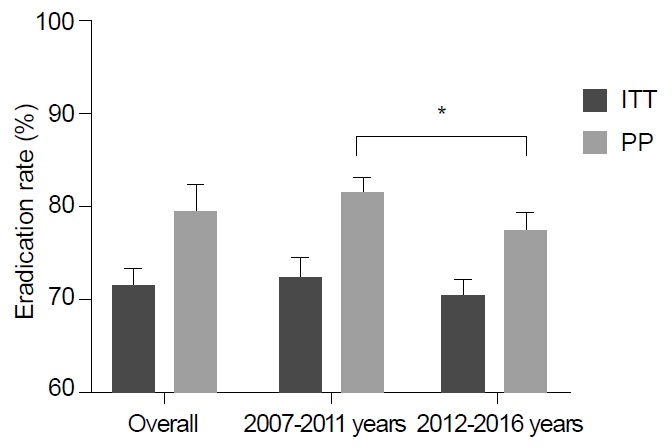
Time trends of pooled Helicobacter pylori eradication rates with standard triple therapy based on data from randomized controlled trials performed in Korea. Overall eradication rates of standard triple therapy were 71.6% (95% CI, 69.9~73.3%) in intention-to-treat (ITT) analysis and 79.6% (95% CI, 76.6~82.2%) in per protocol (PP) analysis. Eradication rates from 2007 to 2011 were 72.3% (95% CI, 71.2~74.4%) in ITT analysis and 81.5% (95% CI, 79.9~82.9%) in PP analysis. Eradication rates from 2012 to 2016 were 70.3% (95% CI, 68.4~72.1%) in ITT analysis and 77.4% (95% CI, 75.6~79.2%) in PP analysis. *P<0.01.
본 지침에서 치료 기간에 따른 표준3제요법의 제균율을 보기 위하여 7일, 10일, 14일 치료의 제균율에 대한 하위 분석을 시행하였다. 7일 표준3제요법의 ITT 제균율은 70.0% (95% CI, 68.5~71.4%), 10일 치료 73.7% (95% CI, 69.8~77.2%), 14일 치료 78.1% (95% CI, 75.2~80.7%)로, 14일 치료의 제균율이 7일이나 10일 치료에 비해 유의하게 높았으나(각각 P<0.01), 7일과 10일 치료의 제균율 간에는 유의한 차이가 없었다(Supplementary Fig. 3).
같은 주제를 다룬 2017년 네트워크 메타분석에서도 유사한 결과를 보였으며, 7일, 10일, 14일 치료의 ITT 제균율은 각각 71.1% (95% CI, 68.3~73.7%), 67.0% (95% CI, 60.0~73.4%), 76.4% (95% CI, 73.3~79.2%)였다[88]. 또한 2019년에 발표된 전국 다기관 연구 결과, 7일 표준3제요법의 ITT 제균율은 63.9%, PP 제균율은 71.4%였다[87].
상기의 분석과 근거에 의하면 clarithromycin 내성 검사 없이 표준3제요법을 1차 제균 치료로 사용할 때는 14일 요법이 권장된다.
(2) Bismuth 비포함 4제요법
① 순차 치료(sequential therapy)
순차 치료는 헬리코박터 파일로리 감염의 1차 제균 치료로 사용될 수 있는가?
지침 5. 1차 제균 치료로 10일 순차 치료(양성자펌프억제제 표준 용량과 amoxicillin 1 g 하루 2회 5일간 사용 후 양성자 펌프억제제 표준 용량, clarithromycin 500 mg, metronidazole 500 mg 하루 2회 5일간)를 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 높음
∙ 전문가 합의: 70.0% (2차), 63.3% (1차)
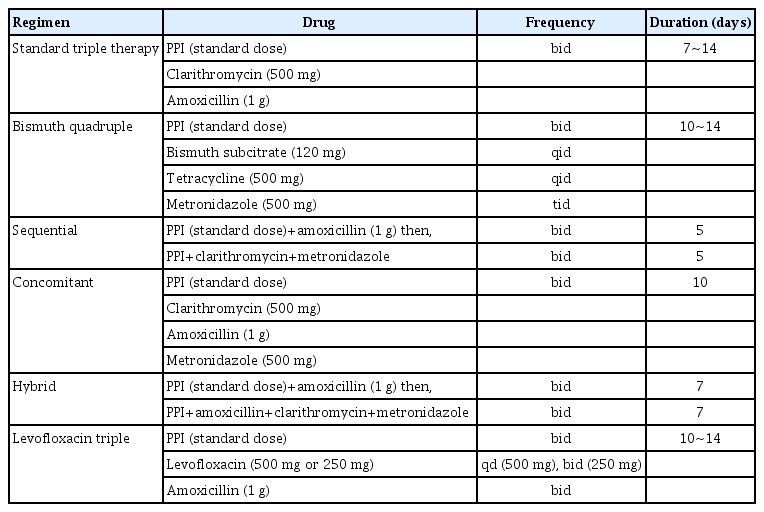
최근 여러 외국 가이드라인에서 clarithromycin 내성률이 15% 이상인 지역에서는 bismuth를 포함하지 않는 4제요법(non-bismuth quadruple therapy)인 순차 치료나 동시 치료 또는 bismuth 4제요법을 1차 치료로 권장한다[34,89]. Bismuth를 포함하지 않는 4제요법은 PPI와 함께 amoxicillin, clarithromycin, metronidazole의 4가지 약제를 동시에 사용하되 그 방법 마다 개별 항생제의 사용 기간이 다르다. 순차 치료는 PPI와 amoxicillin을 초기 5일간 사용한 후, 6일부터 10일까지 5일간 PPI, clarithromycin과 metronidazole을 투여하는 방법이다.
1차 제균 치료로서 순차 치료에 대한 효과를 확인하기 위하여 24개의 RCT를 대상으로 메타분석을 시행하였다(n=5,070)(Supplementary Table 4) [71,73-76,86,90-107]. 표준3제요법과 비교한 RCT 20개, bismuth 포함 4제요법과 비교한 연구 2개, 병합 치료(hybrid therapy)와 비교한 연구 2개가 포함되었으며, 동시 치료와의 비교 연구는 동시 치료 부분에서 기술하였다.
ㄱ. 표준3제요법과 10일 순차 치료의 비교
표준3제요법과 10일 순차 치료의 치료 성적을 비교한 메타분석에서 10일 순차 치료가 표준3제 치료에 비해 ITT 분석에서는 37% (95% CI, 1.21~1.52), PP 분석에서는 60% (95% CI, 1.40~1.93) 제균율이 높았다. 이를 표준3제요법의 치료 기간으로 나누어 분석해 보면 10일 순차 치료는 7일과 10일 표준3제요법에 비하여 유의하게 제균율이 높았으나, 14일 표준3제요법과는 유사한 제균율을 보였다(Fig. 5).
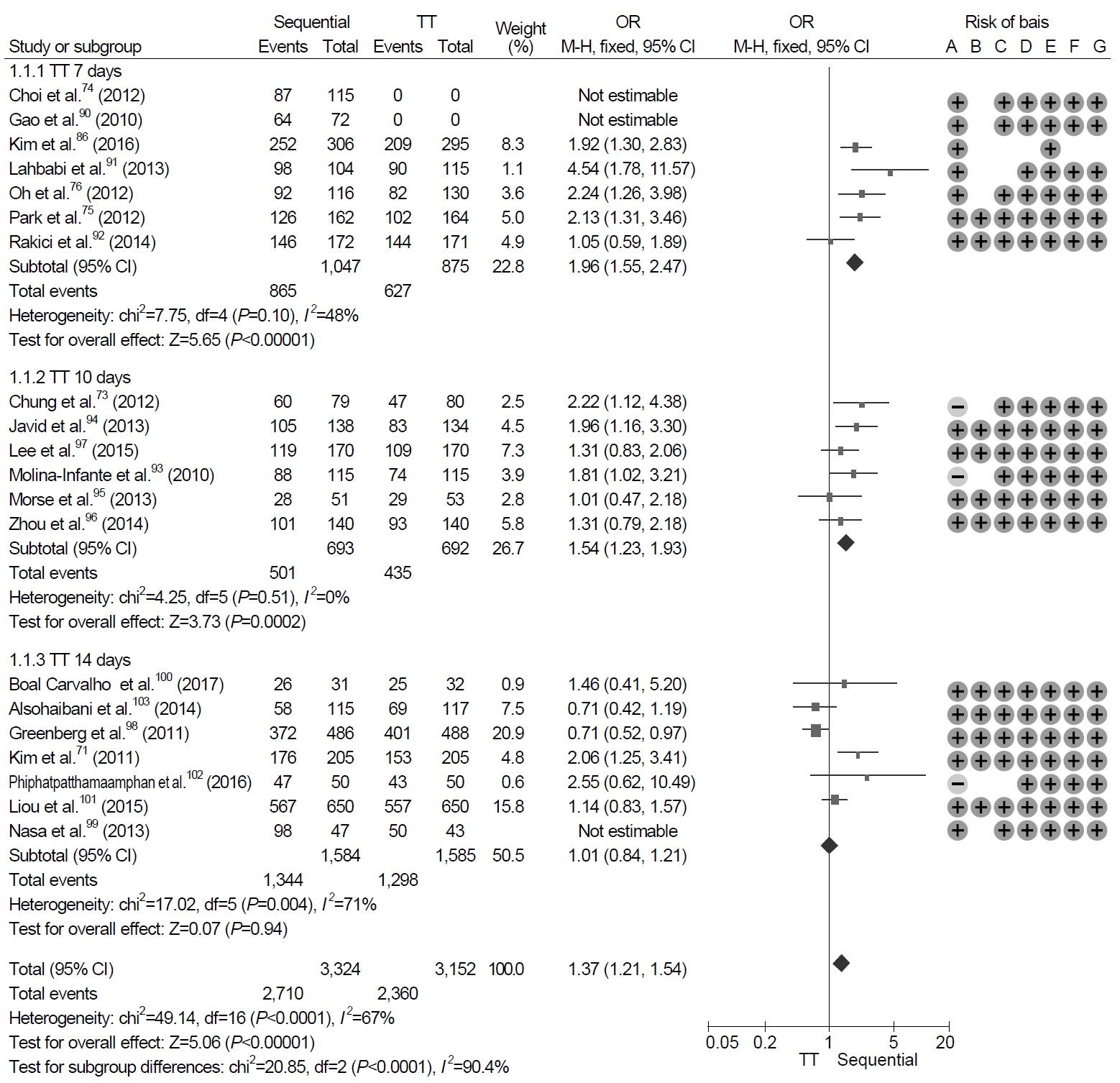
Comparison of 10-day sequential therapy and standard triple therapy (TT) according to treatment duration of TT in intention-to-treat analysis. Risk of bias: A, random sequence generation (selection bias); B, allocation concealment (selection bais); C, blinding of participants and personnel (performance bias); D, Blinding of outcome assessment (detection bias); E, incomplete outcome data (attrition bias); F, selective reporting (reporting bias); G, other bias. M-H, Mantel-Haenszel test.
20개 연구의 10일 순차 치료의 제균율(pooled eradication rates)을 종합해보면 ITT 분석 80.3%, PP 분석 86.6%였으며, 이 중 7개의 국내 연구만을 분석하였을 때는 ITT 분석 78.6%, PP 분석 87.5%였다.
ㄴ. 10일 순차 치료와 bismuth 4제요법의 비교
10일 순차 치료와 bismuth 4제요법을 비교한 2개의 RCT 연구의 메타분석에서 두 치료법의 제균율은 차이가 없었으나(RR, 0.79; 95% CI, 0.47~1.32 in ITT analysis; RR, 0.63; 95% CI, 0.27~1.49 in PP analysis), 포함된 환자수가 적고 국내 연구가 포함되지 않았다는 제한점이 있다(Supplementary Fig. 4).
ㄷ. 10일 순차 치료와 병합 요법(hybrid therapy)과의 비교
10일 순차 치료와 병합 요법을 비교한 2개의 RCT 연구의 메타분석에서 10일 순차 치료가 병합 요법에 비해 제균율이 낮았으나(RR, 0.36; 95% CI, 0.23~0.58 in ITT analysis; RR, 0.18; 95% CI, 0.10~0.35 in PP analysis), 포함된 환자 수가 적고 국내 연구가 포함되지 않았다는 제한점이 있다.
요약하면, 1차 제균 치료로서 10일 순차 치료의 제균율은 표준3제요법의 제균율에 비해 높았으며, 하위 분석에서 7일과 10일 표준3제요법에 비하여 순차 치료가 높은 제균율을 보였으나 14일 표준3제요법과는 유사하였다. Bismuth 4제요법과 병합 요법과의 비교 분석은 RCT 수가 적어 결론을 내리기 어렵다. 그러므로 국내에서 clarithromycin 내성이 증가함에 따라 내성 검사 없이 1차 제균 치료를 하는 경우 10일 순차 치료를 권고한다.
② 동시 치료
동시 치료는 헬리코박터 파일로리 감염의 1차 제균 치료로 사용될 수 있는가?
지침 6. 1차 제균 치료로 10일 동시 치료(양성자펌프억제제 표준 용량, clarithromycin 500 mg, amoxicillin 1 g, metronidazole 500 mg 하루 2회)를 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 높음
∙ 전문가 합의: 80.0% (1차)
동시 치료는 표준3제요법의 제균율 감소를 극복하기 위하여 사용되는 bismuth 미포함 4제요법의 하나로 PPI와 함께 amoxicillin, clarithromycin, metronidazole을 10일간 동시에 투여하는 방법이다.
1차 제균 치료로 동시 치료의 효과를 보기 위하여 동시 치료를 포함한 RCT를 추출하였고, 5일, 7일 동시 치료 단기 요법은 제외하였다. 총 26개의 RCT들이 최종적으로 분석에 포함되었다(Supplementary Table 5) [80,85,105,108-127]. 21개의 10일 동시 치료, 6개의 14일 동시 치료가 포함되었고, 1개의 RCT는 10일 동시 치료와 14일 동시 치료를 모두 포함하고 있었다. 10일 동시 치료의 제균율은 ITT 분석 85%, PP 분석 91%였고, 14일 동시 치료의 제균율은 ITT 분석 86%, PP 분석 94%로 표준3제요법보다 높았고, 10일 동시 치료와 14일 동시 치료의 제균율은 차이를 보이지 않았다. 국내 연구에 대한 하위 분석에서 10일 동시 치료 제균율은 ITT 분석 84%, PP 분석 92%, 14일 동시 치료 제균율은 ITT 분석 79%, PP 분석 94%였으며, 투여 기간에 따른 제균율의 차이는 없었다(Supplementary Table 6).
동시 치료와 다른 치료법의 제균율을 표준화된 기준으로 근거의 질을 평가하기 위하여 GradePro (www.gradepro.org; McMaster University and Evidence Prime Inc., Hamilton, Ontario, Canada)를 이용하였다. 10일 동시 치료는 순차 치료에 비해서 근소하게 제균율이 높았고 10일/14일 표준3제요법에 비해서는 17% 높은 제균율을 보였으며, 이에 대한 근거 수준은 높았다. Bismuth 4제요법, 병합 요법과는 제균율의 차이를 보이지 않았으며, 근거 수준은 각각 중등도, 높음으로 평가하였다.
검색 과정을 통해 10일 동시 치료와 다른 치료법을 비교한 21개의 RCT들이 선정되었다. 8개의 RCT에서 10일 동시 치료와 10일/14일 표준3제요법의 제균율을 비교하였다. 10일 동시 치료 제균율은 10일/14일 표준3제요법의 제균율보다 유의하게 높았다(RR, 1.17; 95% CI, 1.05~1.30 in ITT analysis; RR, 1.15; 95% CI, 1.06~1.25 in PP analysis; Fig. 6).
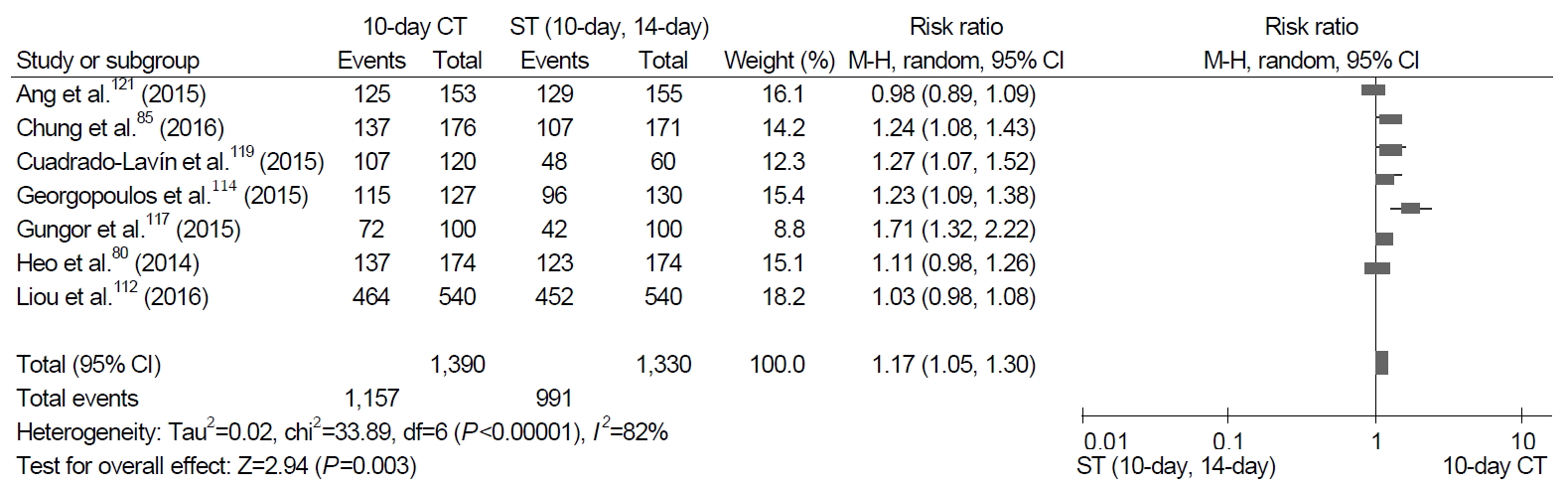
Comparison of 10-day concomitant therapy (CT) and 10-/14-day standard triple (ST) therapy in intention-to-treat analysis. M-H, Mantel-Haenszel test.
13개의 RCT에서 10일 동시 치료와 10일 순차 치료를 비교하였다. 10일 동시 치료 제균율이 10일 순차 치료에 비해서 유의하게 높았으나, 그 차이는 크지 않았다(RR, 1.04; 95% CI, 1.00~1.08 in ITT analysis; RR, 1.04; 95% CI, 1.01~1.07 in PP analysis; Supplementary Fig. 5). 동시 치료의 제균율이 순차 치료에 비해서 근소하게 높았는데, 이는 clarithromycin이나 metronidazole 중 하나에만 내성이 있을 경우 동시 치료가 순차 치료에 비해 효과적이기 때문으로 생각된다. 실제로 clarithromycin에 내성이 있는 경우 동시 치료가 순차 치료에 비해 제균율이 높았으며[128,129], metronidazole에 내성이 있지만 clarithromycin에 내성이 없는 경우에서도 동시 치료가 순차 치료에 비해 제균율이 높았다[128,130].
6개 RCT에서 10일 동시 치료와 10일/14일 bismuth 4제요법의 제균율을 비교하였다(Supplementary Fig. 6). 10일 동시 치료의 제균율은 bismuth 4제요법의 제균율과 유의한 차이가 없었다(RR, 1.05; 95% CI, 0.96~1.15 in ITT analysis; RR, 1.01; 95% CI, 0.97~1.06 in PP analysis). 2개 RCT에서 10일 동시 치료와 병합 요법의 제균율을 비교하였는데, 양 군의 제균율은 차이가 없었다(RR, 0.99; 95% CI, 0.93~1.05 in ITT analysis). 3개의 RCT에서 14일 동시 치료와 10일/14일 순차 치료의 제균율을 비교하였다. 14일 동시 치료의 제균율은 ITT 분석에서는 순차 치료와 차이가 없었으나(76% vs. 79%), PP 분석에서는 14일 동시 치료가 순차 치료에 비해서 제균율이 약간 높았다(89% vs. 82%). 2개의 RCT에서 14일 동시 치료와 14일 표준3제요법의 제균율을 비교하였으며, 14일 동시 치료의 제균율이 14일 표준3제요법의 제균율에 비해 유의하게 높았다(88% vs. 79% in ITT analysis; 94% vs. 82% PP analysis). 2개의 RCT에서는 14일 동시 치료와 병합 요법의 제균율을 비교하였는데, 14일 동시 치료의 제균율이 병합 요법의 제균율에 비해 약간 높았다(91% vs. 85%, P=0.05 in ITT analysis; 96% vs. 92%, P=0.07 in PP analysis).
요약하면, 1차 제균 치료로서 10일 동시 치료의 제균율이 10일/14일 표준3제요법에 비해서는 유의하게 높았으나, 순차 치료에 비해서는 근소하게 높고, 병합 요법 및 bismuth 4제요법과는 유사하였다. 14일 동시 치료는 14일 표준3제요법과 비교 시 PP 및 ITT 분석 모두에서 유의하게 제균율이 높았으며, 10일/14일 순차 치료에 비해서는 PP 분석에서 제균율이 높았다. 10일 동시 요법과 14일 동시 요법의 제균율은 비슷하였다. 따라서 내성 검사 없이 1차 치료를 고려하는 경우, 10일 동시 치료가 권장된다.
(3) Clarithromycin 내성 검사에 기반한 표준3제요법
Clarithromycin 내성 검사는 표준3제요법의 제균율을 향상시키는가?
지침 7. 7일 동안의 표준3제요법을 1차 제균 요법으로 사용하고자 할 때에는 중합효소연쇄반응 또는 염기서열법을 이용한 clarithromycin 내성 검사를 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 낮음
∙ 전문가 합의: 83.3% (1차)
우리나라의 경험적 H. pylori 감염 표준3제요법의 제균율은 점차 감소하여 약 70% 정도이다[131-133]. Maastricht V 가이드라인에서는 clarithromycin의 내성이 15%를 초과하는 지역에서는 경험적 표준3제요법을 1차 치료로 사용하지 않을 것을 강력히 권고하고 있다[34]. 우리나라에서 표준3제요법의 낮은 제균율과 clarithromycin에 대한 높은 내성률을 고려하면, H. pylori 감염의 치료에 대한 새로운 전략이 필요한 시점이다.
H. pylori를 배양하고 항생제 감수성 검사 결과를 토대로 항생제를 선택하는 것이 가장 이상적인 방법이지만[134,135], H. pylori는 배양 기간이 오래 걸리고, 배양 환경이 까다롭기 때문에 배양이 쉽지 않아 임상에 적용하기가 어렵다. 그러나 clarithromycin의 내성과 관련이 있다고 알려진 23S 리보솜 RNA의 점돌연변이를 찾아내는 중합효소연쇄반응(PCR) 또는 염기 서열법을 이용하여 약제를 선택하는 방법은 임상에서 비교적 쉽게 사용할 수 있다.
국내 1,232명을 대상으로 시행된 환자-대조군 연구에서 dual priming oligonucleotide-based multiplex PCR법을 이용하여 A2142G, A2143G 부위에 점돌연변이를 가지고 있는 환자군은 PPI+amoxicillin+metronidazole (PAM)로 7일 동안 치료하고, 점돌연변이가 없는 환자군은 표준3제요법 7일 동안 치료하는 맞춤 치료를 시행하였고, 대조군은 7일 동안의 경험적 표준3제요법을 시행하여 H. pylori 제균율을 비교하였다. 맞춤 치료 환자군의 제균율은 ITT 분석에서 80.7% (176/218)로 경험적 치료를 시행한 대조군의 표준3제요법(69.5% [214/308]; P=0.004) 또는 PAM (71.1% [219/308]; P=0.012)의 제균율보다 높았다[78]. 최근에 발표된 두 개의 환자-대조군 연구 결과를 살펴보면, bismuth 4제요법, PAM, 또는 표준3제요법를 이용한 7일 동안의 맞춤형 치료의 PP 분석 제균율이 각각 91.8%와 94.3%로, 7일 동안의 경험적 표준3제요법 대조군의 72.1%와 76.5%보다 높았다[17,18]. 특히, 맞춤 치료의 비용은 14일 동안의 경험적 표준3제요법의 비용과 거의 동등하여 비용-효과 측면에서도 열등하지 않았다[18].
Clarithromycin 내성이 있는 환자의 제균 요법은 현재까지 발표된 연구를 근거로 7일 동안의 PAM 또는 bismuth 4제요법을 고려할 수 있다[16,17,77]. 그러나 최근 국내 연구에서는 clarithromycin 내성이 있는 환자에서 7일 동안의 PAM 치료의 제균율이 만족스럽지 않아(55.4% [51/92] in ITT analysis, 66.2% [51/77] in PP analysis) metronidazole의 용량을 높이고 치료 기간을 늘려야 할 필요성을 제시하였다[136]. 따라서 clarithro- mycin 내성이 있는 경우에서의 제균 요법에 대한 권고안은 현재 우리나라에서 진행 중인 RCT 결과에 근거하여 추가해야 할 것이다. 요약하면, 7일 동안의 제균 요법을 고려할 때는 임상에 적용 가능한 검사법을 이용하여 clarithromycin 내성 검사를 시행하고, 내성이 없는 환자에게 표준3제요법을 권고한다.
(4) Bismuth 4제요법
Bismuth 4제요법은 헬리코박터 파일로리 감염의 1차 제균 치료로 사용될 수 있는가?
지침 8. Bismuth 4제요법(양성자펌프억제제 표준 용량 하루 2회, metronidazole 500 mg 하루 3회, bismuth 120 mg과 tetracycline 500 mg 하루 4회 10일에서 14일간)은 14일 표준3제요법, 10일 동시 치료 및 순차 치료와 유사한 1차 치료 제균율을 보이나 약물 부작용이 높고 구제 요법으로 사용할 가능성이 있어 다른 제균 치료를 사용할 수 없는 경우에 1차 치료로 사용할 것을 권고한다.
∙ 권고 강도: 약함
∙ 근거 수준: 중간
∙ 전문가 합의: 83.3% (1차)
H. pylori의 항생제 내성은 제균율에 직접적인 영향을 주는데, 그중에서도 clarithromycin 내성이 H. pylori 제균 성공 여부에 가장 중요한 요인으로 알려져 있다. 여러 가이드라인들에 따르면, clarithromycin 내성률이 높은 지역에서는 1차 치료로 bismuth를 기본으로 한 4제요법 또는 bismuth를 포함하지 않은 4제요법을 사용할 것을 권고하고 있다[34,137]. 일반적으로 clarithromycin 내성이 높은 지역의 정의는 일정 지역에서 clarithromycin 내성이 있는 H. pylori가 15% 이상일 때를 뜻한다[34]. 우리나라의 경우, 지난 10년 동안 H. pylori의 clarithromycin 내성률은 점차적으로 증가해왔으며[11], 최근 논문들에서도 국내의 clarithromycin 내성률은 17.8~31.0%로 보고하였다[2,138].
Bismuth를 포함한 4제요법과 관련된 RCT들을 이용한 두 개의 네트워크 메타분석 연구 결과, bismuth를 기본으로 한 4제요법의 효과는 항생제의 조합과 치료 기간에 따라 상당한 차이가 있는 것으로 나타났다[139,140]. 이에 본 지침에서는 2008년 1월부터 2018년 7월까지 1차 치료로 bismuth를 기본으로 한 4제요법을 사용한 9개의 RCT들을 대상으로 bismuth를 기본으로 한 4제요법의 효과와 안전성을 확인하기 위한 메타분석을 시행하였다(Supplementary Table 7) [105,112,117,141-146]. Bismuth를 기본으로 한 4제요법의 제균율은 ITT 분석에서는 84.5% (95% CI, 74.9~90.9%), PP 분석에서는 90.6% (95% CI, 82.8~95.1%)로 확인되었다. 그러나 다른 제균 치료법들의 제균율과 비교한 ITT 분석 결과에서는 bismuth를 기본으로 한 4제요법 10~14일의 제균율이 14일 표준3제요법(RR, 1.28; 95% CI, 0.97~1.70) (Fig. 7A), 10일 순차 치료(RR, 0.96; 95% CI, 0.83~1.12) (Fig. 7B), 10일 동시 치료(RR, 1.01; 95% CI, 0.93~1.10) (Fig. 7C)의 제균율에 비해 통계적으로 우월함을 보여주지 못하였다.

Helicobacter pylori eradication rates with bismuth quadruple therapy as a first-line therapy. (A) Comparison of 10-/14-day bismuth quadruple therapy and 14-day standard triple therapy in intention-to-treat analysis. (B) Comparison of 10-/14-day bismuth quadruple therapy and 10-day sequential therapy in intention-to-treat analysis. (C) Comparison of 10-/14-day bismuth quadruple therapy and 10-day concomitant therapy in intention-to-treat analysis. Risk of bias: A, random sequence generation (selection bias); B, allocation concealment (selection bais); C, blinding of participants and personnel (performance bias); D, Blinding of outcome assessment (detection bias); E, incomplete outcome data (attrition bias); F, selective reporting (reporting bias); G, other bias. PBMT, bismith quarduple therapy; M-H, Mantel-Haenszel test; SQT, sequential therapy; CCT, concomitant therapy.
또한, PP 분석에서도 bismuth를 기본으로 한 4제요법 10~14일의 제균율은 14일 표준3제요법(RR, 1.37; 95% CI, 0.95~1.99), 10일 순차 치료(RR, 0.99; 95% CI, 0.93~1.05), 10일 동시 치료(RR, 1.01; 95% CI, 0.95~1.07)에 비해 통계적으로 유의한 차이가 없었다. 이번 메타분석에 포함된 논문들의 이질성은 전반적으로 중간 정도였으나, 결과 해석에 있어 분석에 이용된 연구의 수가 적다는 제한점은 감안해야 할 것이다.
부작용 측면에서는 연구들 사이에 상당한 이질성이 있는 것으로 확인되었으나(I2=92%), bismuth를 기본으로 한 4제요법의 부작용이 다른 제균 치료들에 비해 유의하게 높은 것으로 나타났다(RR, 1.72; 95% CI, 1.23~2.40; Supplementary Fig. 7).
Bismuth를 기본으로 한 4제요법은 페니실린 알레르기가 있는 환자들이나 중복 내성이 있는 H. pylori에 감염된 환자들에서도 효과적으로 사용할 수 있는 제균 치료법이기 때문에[137], 임상의들에게 유용한 치료 방법 중 하나일 수 있다. 하지만, 실제 임상에서 bismuth를 기본으로 한 4제요법을 1차 치료법으로 사용하기에는 bismuth를 기본으로 한 4제요법의 높은 부작용과 1차 치료에 실패하였을 때 사용할 수 있는 구제 요법이 적다는 현실에 직면하게 된다. 따라서, bismuth를 기본으로 한 4제요법은 다른 1차 치료법들을 사용할 수 없는 경우에 일차 치료로 사용할 것을 권고하며, 향후 1차 bismuth를 기본으로한 4제요법의 효과를 확인하기 위한 잘 디자인된 국내 연구가 필요하겠다.
추가적으로, bismuth의 용량과 관련하여 국내에서 사용하는 bismuth subcitrate인 DeNol® 300 mg에는 elemental bismuth 120 mg이 들어있다. 따라서, 임상에서 bismuth를 사용할 때에는 bismuth subcitrate를 기준으로 하여 300 mg을 하루 네 번 사용하는 것이 권고된다.
2) 구제 요법
헬리코박터 파일로리 제균 치료가 실패한 이후 추천되는 구제 요법은 무엇인가?
체계적 문헌 검색에서 하나 이상의 구제 요법을 비교한 RCT들은 총 36개 검색되었다[147-182]. 이들을 이전에 실패한 요법에 따라 분류한 결과는 Supplementary Table 8에 정리되어 있으며, 이들 연구들은 비교한 구제 요법 혹은 이전에 실패한 요법이 서로 매우 달라서 메타분석이 가능한 경우가 많지 않았다. 메타분석은 3개 이상의 RCT가 있는 경우에 시행하였다. 아래 언급되는 모든 제균율은 ITT 제균율이며 근거들은 Supplementary Table 9에 요약되어 있다.
지침 9. 1차 제균 치료로서 표준3제요법에 실패한 경우 2차 제균 치료로서 bismuth 포함 4제 14일 요법을 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 높음
∙ 전문가 합의: 96.7% (1차)
Bismuth 4제요법은 9개의 RCT에서 제균율이 75.5% (95% CI, 71.6~79.1%)였다(Fig. 8) [156,161,162,165,167,175,176,179,182]. 치료 기간은 7일, 10일 혹은 14일이었으며, 10일 치료 요법과 14일 치료 요법이 비슷한 효과를 보였기 때문에, 하위 분석에서 7일 치료 요법과 10~14일 치료 요법을 비교하였다. 그 결과, 10~14일 치료 요법의 제균율이 81.6% (95% CI, 76.9~85.6%; I2=29.6%)로 7일 치료 요법의 제균율 68.4% (95% CI, 53.0~73.5%; I2=73.8%)보다 유의하게 높았다(P<0.01). Bismuth 4제요법의 14일 치료를 7일 치료와 직접 비교한 3개의 RCT의 메타분석에서도 14일 치료가 7일 치료보다 유의하게 높은 제균율을 보였다(risk difference [RD], 0.09; 95% CI, 0.02~0.15).

Meta-analysis of nine studies that compare bismuth quadruple therapy with other regimens after the failure of first-line clarithromycin triple therapy. The pooled eradication rate of bismuth quadruple therapy as a second-line therapy is 75.5% (95% CI, 71.6~79.1%).
Levofloxacin 3제요법은 8개의 RCT에서 제균율이 73.1% (95% CI, 68.4~77.3%)였다(Fig. 9) [147,152,165,166,168,175,176,182]. 하위 그룹 분석에서 10~14일 치료 요법의 제균율이 78.5% (95% CI, 71.9~84.0%)로 7일 치료 요법의 69.1% (95% CI, 61.6~74.9%)보다 유의하게 높았다(P=0.04). Levofloxacin 3제요법의 10일 치료와 7일 치료를 직접 비교한 1개의 RCT에서도 10일 치료 요법이 7일 치료 요법보다 제균율이 유의하게 높았다(87.5% vs. 67.5%, P<0.01) [177].
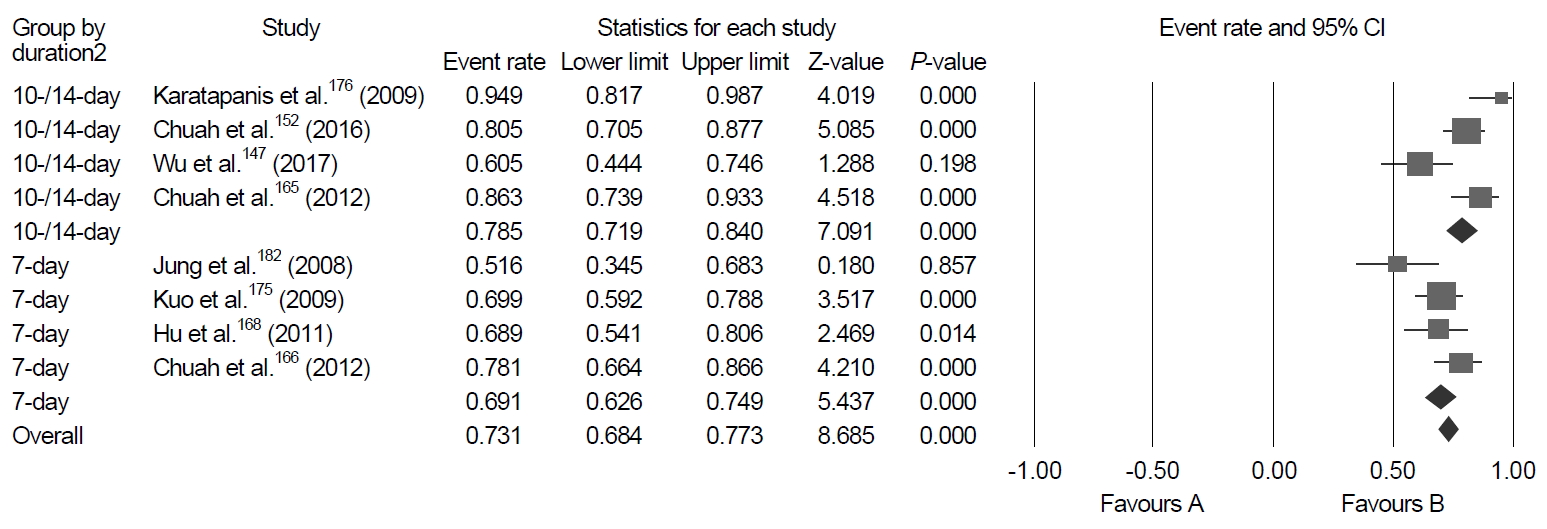
Meta-analysis of eight studies that compare levofloxacin triple therapy with other regimens after the failure of first-line clarithromycin triple therapy. The pooled eradication rate of levofloxacin triple therapy as a second-line therapy is 73.1% (95% CI, 68.4~77.3%).
Bismuth 4제요법과 levofloxacin 3제요법을 직접 비교한 4개의 RCT의 메타분석에서 두 요법의 제균율에 유의한 차이는 없었다[165,175,176,182]. 다만, ITT 분석에서는 levofloxacin 3제요법이 우월한 경향을 보였고(bismuth 4제요법 vs. levofloxacin 3제요법; RD, -0.06; 95% CI, -0.14~0.02; Supplementary Fig. 8), PP 분석에서는 bismuth 4제요법이 우월한 경향을 보였다(RD, 0.02; 95% CI, -0.05~0.10; Supplementary Fig. 8). 이는 bismuth 4제요법의 복약 순응도가 낮기 때문일 것으로 생각된다. 2006년에 발표된 2개의 체계적 문헌 고찰에서 levofloxacin 3제요법 10일 치료가 bismuth 4제요법 7일 치료보다 우월한 제균 효과를 보였으나 [183,184], 본 메타분석에 포함된 연구들에서는 두 치료법을 서로 같은 기간 동안 사용하였다는 차이가 있다(7일 vs. 7일, 10일 vs. 10일, 14일 vs. 14일).
Levofloxacin 3제요법의 주요 제한점은 levofloxacin 내성이 있는 경우 제균 효과가 상당히 감소한다는 것이다[165]. 최근 한국인의 H. pylori 항생제 내성 전국 조사에서 levofloxacin 내성률이 37.0%였다[2]. 그러므로 우리나라에서는 levofloxacin 3제요법보다는 bismuth 4제요법이 바람직하다고 할 수 있다. Metronidazole의 내성률도 29.5%로 높지만 치료 용량과 기간을 증가시켜 극복할 수 있기 때문에[185], bismuth 4제요법을 구제 요법으로 사용할 때는 14일 치료가 10~14일 치료보다 바람직하다. 그러므로 일차 제균 치료로서 표준3제요법에 실패한 경우 이차 제균 치료로서 bismuth 4제요법 14일 치료를 권고한다.
지침 10. 1차 치료로서 순차 치료 혹은 동시 치료에 실패한 경우 2차 제균 치료로서 bismuth 4제요법을 권고한다.
∙ 권고 강도: 강함
∙ 근거 수준: 매우 낮음
∙ 전문가 합의: 90.0% (1차)
문헌 검색에서 1차 제균 치료로서 순차 치료 또는 동시 치료에 실패한 환자에서 2차 제균 치료법을 비교한 RCT는 없었다. 코호트 연구들의 메타분석에서 levofloxacin 3제요법은 5개 연구 86명의 환자에서 제균율이 81% (95% CI, 71~91%; I2=28%)였다[186]. 또 다른 메타분석에서는 순차 치료 실패 후 제균율이 81% (6개 연구; 95% CI, 73~90%; I2=19%), 동시 치료 실패 후 제균율은 78% (3개 연구; 95% CI, 58~97%; I2=67%)였다[34]. 그러나 상기에서 언급한 바와 같이 이러한 결과를 levofloxacin 내성률이 높은 국내에서 직접 적용하기는 어렵다[2,11,187,188].
Bismuth 4제요법은 코호트 연구들의 메타분석에서 제균률이 84% (95% CI, 63~100%, I2=56%)였다[34]. 그러나 이 분석에서는 두 개의 코호트 연구에서 약 30명의 환자만이 포함되었다.
그러므로 1차 제균 치료로서 순차 치료 혹은 동시 치료에 실패한 경우 2차 제균 치료로서 bismuth 4제요법을 권고한다. 그러나 이러한 권고를 뒷받침하기 위한 자료가 좀 더 필요하다.
지침 11. 1차 혹은 2차 치료로서 bismuth 4제요법에 실패한 경우 levofloxacin 포함 3제요법을 고려할 수 있다.
∙ 권고 강도: 약함
∙ 근거 수준: 매우 낮음
∙ 전문가 합의: 70.0% (1차)
1차 제균 치료로서 표준3제요법, 순차 치료, 혹은 동시 치료에 실패한 뒤에 2차 치료로서 bismuth 4제요법에 실패하였다면, 3차 제균 치료 요법에 clarithromycin을 다시 사용하는 것은 추천되지 않는다. 1차 제균 치료로서 bismuth 4제요법에 실패한 경우에도 clarithromycin을 사용하는 것은 부적절할 수 있다. Bismuth 4제요법을 1차 제균 치료로 선택한 이유가 clarithromycin 내성이 의심되는 상황이었을 가능성이 많기 때문이다[133]. 배양 검사, PCR, 혹은 염기서열법을 이용한 항생제 감수성 검사를 기반으로 치료법을 결정할 수도 있다. 일반적으로 clarithromycin, fluoroquinolone, rifabutin에 대한 내성이 있는 경우에는 해당 항생제를 다시 사용하는 것이 추천되지 않는다. 한편, amoxicillin과 metronidazole은 다시 사용할 수 있다[185]. 그러나 1차 치료와 달리, 2차 혹은 3차 치료에서 이전에 실패한 항생제를 알고 있다면, 이를 바탕으로 한 경험 치료도 항생제 감수성 검사를 기반으로 한 치료법과 효과가 비슷할 수 있다[135]. 문헌 검색에서 1차 혹은 2차 제균 치료로서 bismuth 4제요법이 실패한 뒤에 구제 요법을 비교한 RCT는 없었다. 따라서, 코호트 연구 결과 혹은 다른 상황에 사용된 RCT 결과를 바탕으로 다음과 같은 제균 요법들을 고려할 수 있다. 이상의 내용을 종합한 H. pylori 치료의 1차 및 2차 치료법들과 알고리듬은 각각 Table 4 및 Fig. 10에 정리되어 있다.
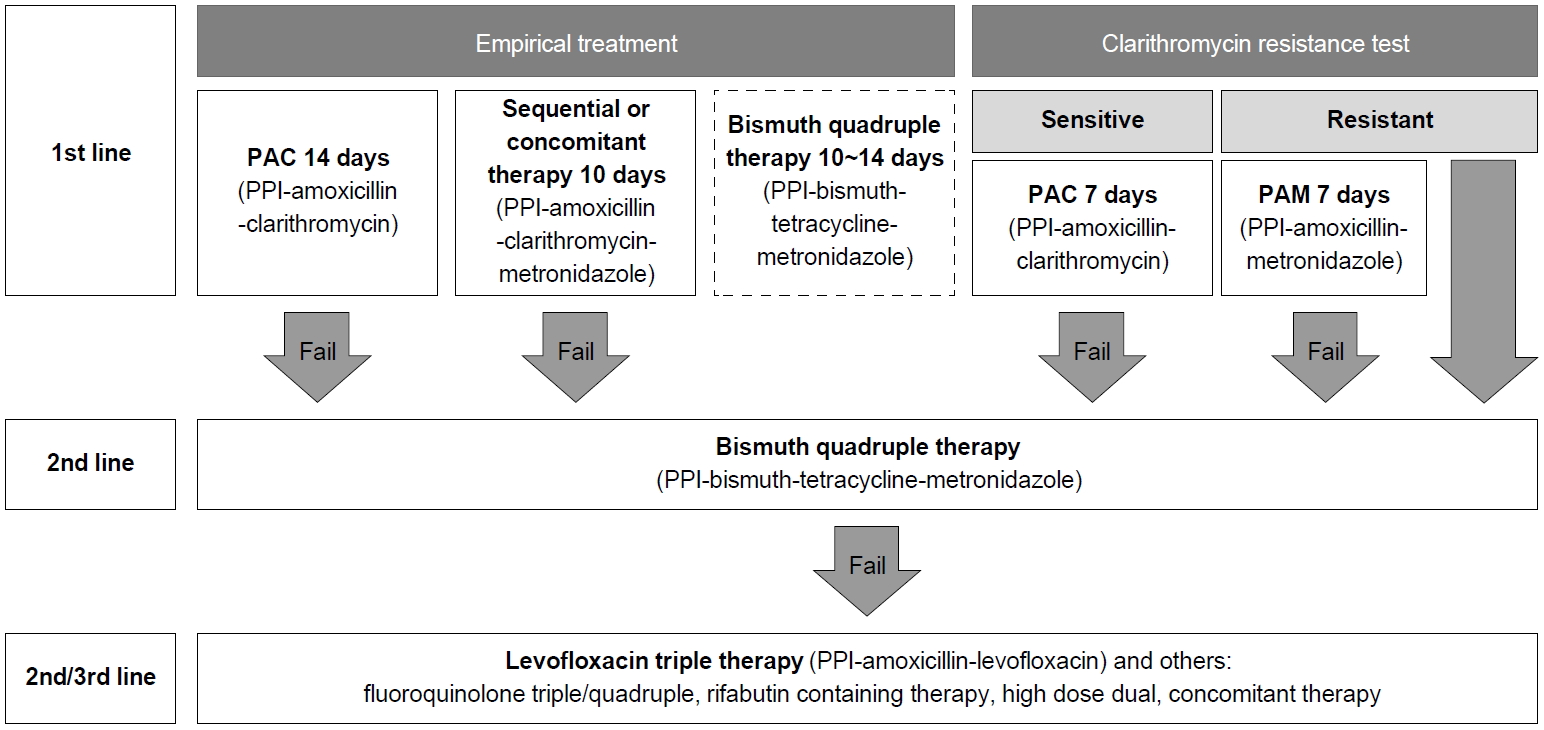
Proposed algorithm for the treatment of Helicobacter pylori infection. Bismuth quadruple therapy as a first-line therapy is dotted because it is less preferred than other regimens. PPI, proton pump inhibitor.
(1) Levofloxacin 3제요법
코호트 연구들의 메타분석에서 levofloxacin 3제요법은 5개 연구 501명에서 제균율이 70.0% (95% CI, 62.4~76.6%; I2=58.5%)였으며[34], 2017년 우리나라 14개 기관의 후향적 코호트 연구에서 levofloxacin 3제요법의 제균율은 56.9% (62/109)였다[189]. 이렇게 낮은 제균율의 원인은 우리나라의 높은 levofloxacin 내성률 때문으로 추정할 수 있다[2,11,187,188]. 그러므로 1차 혹은 2차 제균 치료로서 bismuth 4제요법에 실패한 경우 levofloxacin 3제요법(PPI 표준 용량 하루 2회, amoxicillin 1 g 하루 2회, levofloxacin 500 mg 하루 1회 혹은 250 mg 하루 2회) 10일 치료를 권고한다. 그러나이 요법의 제균율은 외국 연구 결과보다 낮을 수 있다는 점을 고려해야 한다.
(2) 기타 fluoroquinolone 3제요법
일본 및 유럽에서 sitafloxacin, gatifloxacin 혹은 moxifloxacin을 이용한 3제요법의 구제 치료 효과를 보고한 바 있으나[150,160,181], bismuth 4제요법에 실패한 뒤에 사용한 결과는 없었다. 우리나라 후향적 코호트 연구에서 1차 제균 치료로서 bismuth 4제요법에 실패한 뒤에 사용된 moxifloxacin 3제요법 7~14일 치료의 제균율은 67.9% (95% CI, 51.5~84.9%)에 불과하였다[190]. 그러므로 bismuth 4제요법에 실패한 뒤 기타 fluoroquinolone 3제요법에 대한 근거는 제한적이다. Fluoroquinolone 사이의 잠재적인 교차 내성이 있기 때문에 levofloxacin의 대안으로 기타 fluoroquinolone을 사용하는 것은 더욱 제한된다고 할 수 있다[188].
(3) Fluoroquinolone 4제요법
Fluoroquinolone 4제요법은 bismuth 4제요법이 아닌 다른 요법에 실패한 뒤에 사용된 RCT 결과만 보고되고 있어, 아직은 참고만 할 수 있는 상황이다[147,151,152,157,162,163,169,171]. Levofloxacin-bismuth 4제요법(levofloxacin, bismuth, PPI, amoxicillin)은 bismuth와 levofloxacin의 상승 효과로 항생제 내성을 극복할 수 있다는 근거로 Maastricht V 가이드라인에서 bismuth 4제요법 실패 후에 사용할 수 있는 “고무적인 구제 요법”으로 제안되었다[34]. 두 개의 코호트 연구에서 2차 제균 치료로서 bismuth 4제요법에 실패한 뒤에 제균율이 83.8% (31/37; 95% CI, 71.3~96.2%)였다[191]. 다른 상황에서 구제 요법으로 사용된 경우 제균율은 73~90%로 상이한 결과가 보고되었다[147,157,192,193]. 그러므로 비록이 요법이 효과적일 것으로 기대되나, 한국인에서 사용되기 전에 검증될 필요가 있다.
Levofloxacin 순차 요법(PPI 및 amoxicillin 사용 후 levofloxacin, PPI, amoxicillin, metronidazole)은 3개의 RCT에서 다양한 일차 3제요법에 실패한 환자를 대상으로 82.2~90.2%의 제균율을 보였다[151,152,163]. 이 요법 역시 bismuth 4제요법 실패 후에 사용하기 위해서는 검증이 필요하다.
(4) Rifabutin 포함 요법
H. pylori 제균 치료에서 rifabutin을 이용하는 주요 제한점은 높은 가격, 골수 독성 및 Mycobacterium tuberculosis에 대한 내성 유발에 관한 염려이다[194]. 2012년에 보고된 체계적 문헌 고찰에서 rifabutin 3제요법의 2차, 3차 및 4차 제균 치료 요법으로서 제균율이 각각 79% (95% CI, 67~92%), 66% (95% CI, 55~77%) 및 70% (95% CI, 60~79%)였다[194]. 포함된 논문들에서 사용한 rifabutin의 용량은 150 mg bid 혹은 300 mg qd였고 PPI와 amoxicillin과 함께 7일에서 10일간 사용하였다. 그러므로 rifabutin 3제요법은 bismuth 4제요법을 포함하여 여러 차례 제균에 실패한 뒤에 사용할 수 있는 구제 요법의 하나로 제안될 수 있다. 그럼에도 불구하고, 상대적으로 부족한 근거와 알려진 위험을 신중하게 고려할 필요가 있다.
(5) 고용량 2제요법
고용량 2제요법은 amoxicillin의 혈중 최저 농도를 높게 유지하기 위하여 하루 3 g 이상, 하루 3회 이상 투약하는 것으로 정의된다[137]. 하나의 RCT에서 1차례 이상 특정되지 않은 요법에 실패한 환자들을 대상으로 rabeprazole 20 mg과 amoxicillin 750 mg 하루 4회 14일 요법의 제균율이 89.3% (50/56; 95% CI, 80.9~97.6%)였다[154]. 2008년 이전에 보고된 두 개의 RCT에서는 제균율은 각각 70~76%였다[195,196]. 이 요법 역시 bismuth 4제요법 실패 후 구제 요법으로 고려될 수 있으나, 이를 뒷받침할 수 있는 자료가 더 필요하다.
(6) 동시 치료
비록 clarithromycin 포함 요법에 실패한 뒤에 clarithromycin을 다시 사용하는 것은 부적절하지만, 동시 치료는 clarithromycin과 metronidazole의 병용 요법이 clarithromycin 내성을 극복할 수도 있다는 측면에서 bismuth 4제요법 실패 후 구제 요법으로 선택될 수 있다[185]. 그러나 근거 자료는 매우 부족한 상황이다. 한 RCT에서 표준3제요법에 실패한 뒤에 동시 치료 7일 요법이 86.5% (45/51; 95% CI, 76.9~96.1%)의 제균율을 보였다[174]. 다른 RCT 내부에서 시행된 전향적 코호트 연구에서는 bismuth 4제요법에 실패한 뒤에 동시 치료 10일 요법이 84.6% (11/13; 95% CI, 57.8~95.7%)의 제균율을 보였다[197].
결 론
H. pylori는 국내 유병률이 50% 내외에 달하는 매우 흔한 감염이며 소화성 궤양 및 위암 등의 질환을 일으키는 균으로 이에 대한 치료 적응증을 확립하고 효과적인 1차 및 2차 제균 요법을 제시하는 것은 임상적으로 매우 중요하며 국가적으로 의료 비용을 효율적으로 사용하는 데 필요하다. 근래에 H. pylori의 clarithromycin에 대한 내성률이 증가함에 따라 기존의 표준3제요법의 제균율은 하락하는 추세이며, 이를 극복하기 위한 방안으로 치료 기간을 늘리거나 순차 치료나 동시 치료와 같은 bismuth를 포함하지 않는 4제요법, clarithromycin 내성 검사를 이용하는 방법 그리고 bismuth 4제요법과 같은 방안이 이용될 수 있다. 구제 요법의 경우 다양한 1차 제균 요법이 사용됨에 각 요법에 따른 전략이 필요한데, 구제 요법에 대한 RCT 논문들의 메타분석 결과, 표준3제요법, 순차 치료, 동시 치료에서 실패한 경우 bismuth 4제요법이 권장된다. 일차 치료로 bismuth 4제요법을 사용하였을 때, 구제 치료로는 levofloxacin 3제요법이 권장된다.
이 지침은 최신 문헌들에 대한 메타분석과 동시에 근거 기반의 가이드라인 제작 방법을 사용하였으며 권고문은 한국의 내성률을 고려하여 만들어졌으며, 따라서 한국과 항생제 내성률이 유사한 극동 지역에서 적용이 가능할 것으로 생각된다. 그리고 최근에 도입된 PCR과 sequencing 기법에 기반한 clarithromycin 내성 검사 기법을 이용한 제균 치료에 대한 최신의 문헌들을 기반으로 한 권고문도 작성되어 이의 사용을 고려하는 임상 상황에서 도움을 줄 것으로 생각한다.
이번 지침에서 만성 위축성 위염 및 장상피화생에 대한 제균 치료의 적응증에 대한 권고문은 전문가들의 합의에 도달하지 못하였다. 이 적응증은 매우 중요한 주제로 향후 만성 위축성 위염 및 장상피화생이 있는 환자에서 H. pylori 제균 치료가 위암의 발생을 낮출 수 있는지에 대한 장기적인 잘 계획된 연구가 필요해 보인다. 또한 위암의 가족력 역시 위암의 위험인자로 잘 알려져 있으며 이 환자군에 대한 치료 적응증을 확립하기 위한 추가 연구가 필요할 것으로 생각된다. 또한 일차 요법 간의 비용 효율성에 대한 연구가 이뤄진다면 이번 가이드라인에 제시된 다양한 1차 치료 요법들 중 어떤 환자나 임상 상황에서 어떤 치료를 선택하는 게 가장 효율적인지에 대한 결정에 도움을 줄 수 있을 것으로 보인다.
Acknowledgements
We would like to express our deep gratitude to Miyoung Choi, PhD of National Evidence based Healthcare Collaborating Agency who performed initial literature search for systematic review, Ein Soon Shin, PhD & MPH, Research Head of the Research Agency for Clinical Practice Guidelines of Korean Academy of Medical Sciences for the Meta-Analysis Workshop, and Soo Young Kim, a professor from the Department of Family Medicine, Hallym University College of Medicine for conducting the Workshop on Expert Consensus Method. We also thank Nayoung Kim, a professor from the Department of Internal Medicine, Seoul National University College of Medicine and Gwang Ha Kim, a professor from the Department of Internal Medicine, Pusan University College of Medicine who reviewed the draft of the guidelines by peer review. Finally, we thank the Internet community 'Bokanyi' for helping us with the patient preference survey.
Notes
No potential conflict of interest relevant to this article was reported.
Supplementary Materials
Studies Included in Meta-analysis about the Efficacy of Helicobacter pylori Eradication after Endoscopic Resection of Gastric Adenoma
Studies Included in Meta-analysis about the Efficacy of Helicobacter pylori Eradication in Patients with Functional Dyspepsia
Evidence Table about the Eradication Rate of Standard Triple Therapy in Helicobacter pylori Infection
Evidence Table about the Eradication Rate of Sequential Therapy in Helicobacter pylori Infection
Studies Included in Meta-analysis about the Eradication Rate of Concomitant Therapy in Helicobacter pylori Eradication
Pooled Eradication Rate of Concomitant Therapy from Randomized Controlled Trials with Random Effect Model
Evidence Table about Bismuth Quadruple Therapy in Helicobacter pylori Eradication
Categorization of Salvage Regimens from Overall 36 Randomized Controlled Trials with 77 Intervention Arms
Evidence Table of 16 Randomized Controlled Trials Which Were Included in the Meta-analysis of Regimens for Salvage Therapy
Meta-analysis of efficacy of Helicobacter pylori eradication in patients with functional dyspepsia. M-H, Mantel-Haenszel test; ORCHID, Optimal Regimen Cures Helicobacter Induced Dyspepsia Study Group.
Meta-analysis of effect of Helicobacter pylori eradication on gastric cancer development. (A) Forest plot of studies reporting gastric cancer in eradication group and control group in subjects with no precancerous lesions at baseline. (B) Forest plot of studies reporting gastric cancer in eradication group and control group in subjects with atrophic gastritis, intestinal metaplasia, and dysplasia at baseline. M-H, Mantel-Haenszel test.
Pooled eradication rates of standard triple therapy by treatment duration from randomized controlled trials performed in Korea. Eradication rates of standard triple therapy (STT) for 7 days were 70.0% (95% CI, 68.5~71.4%) in intention-to-treat (ITT) analysis and 78.4% (95% CI, 77.0~79.7%) in per protocol (PP) analysis. Eradication rates of STT for 10 days were 73.7% (95% CI, 69.8~77.2%) in ITT analysis and 78.9% (95% CI, 74.9~82.4%) in PP analysis. Eradication rates of STT for 14 days were 78.1% (95% CI, 75.2~80.7%) in ITT analysis and 86.0% (95% CI, 83.4~88.3%) in PP analysis. *P<0.05.
Forest plot comparing the different therapies in terms of the eradication rates between sequential therapy. (A) Intention-to-treat analysis. (B) Per protocol analysis. BQT, bismuth quadruple therapy; M-H, Mantel-Haenszel test.
Comparison between 10-day concomitant therapy and 10-day sequential therapy. (A) Intention-to-treat analysis. (B) Per protocol analysis. CT, concomitant therapy; SQT, sequential therapy; M-H, Mantel-Haenszel test.
Comparison between 10-day concomitant therapy and 10-/14-day bismuth quadruple therapy. (A) Intention-to-treat analysis. (B) Per protocol analysis. CT, concomitant therapy; BQT, bismuth quadruple therapy; M-H, Mantel-Haenszel test.
Comparison of adverse events between 10-/14-day bismuth quadruple therapy and other regimens (standard triple therapy, sequential therapy, concomitant therapy). PBMT, bismuth quadruple therapy; M-H, Mantel-Haenszel test.
Meta-analysis of four studies which compared bismuth quadruple therapy and levofloxacin triple therapy after failure of first-line standard triple therapy. (A) Intention-to-treat analysis. (B) Per protocol analysis. PBTM, bismuth quadruple therapy; PAL, proton pump inhibitor, amoxicillin, levofloxacin; M-H, Mantel-Haenszel test.