위체부에 점상 발적을 보인 Helicobacter pylori 미감염자
Helicobacter pylori-naive Subject with Spotty Redness in the Gastric Corpus
Article information
요약: 29세 남자가 4개월간 7 kg의 체중 감소가 있어 시행한 위내시경 검사에서 이상 소견을 보여 병원에 왔다. 체중 감소 이외에 다른 증상은 없었으며 약물 복용력이나 병력도 없었다. 조부가 대장암으로 진단받은 가족력이 있었다. 위내시경 검사를 시행한 결과, 분문부와 상부 체부에서 무수히 많은 작은 흰색 함몰형 미란들이 보였다(Fig. 1A). 위주름에서는 다발성 혈성 반점으로 구성된 점상 발적(spotty redness)이 관찰되었다(Fig. 1B). 위각의 후벽에서는 미세혈관 증식과 이전 조직 검사로 인한 흰색 흉터가 관찰되었다(Fig. 1C). 전정부에서는 균일한 혈관상(regular arrangement of collecting venules)이 관찰되었다(Fig. 1D). 위체부의 대만측과 위각의 후벽측에서 조직 검사를 시행하였다(Fig. 2). Giemsa 염색에서 Helicobacter pylori (H. pylori)는 관찰되지 않았으며 요소호기 검사도 음성이었다. 혈청 검사에서 항H. pylori immunoglobulin G (IgG) 수치는 <5 AU/mL로 음성, 펩시노겐(pepsinogen, PG) I 수치는 36.0 ng/mL, PG II 수치는 9.5 ng/mL, PG I/II 비는 3.8로 정상 소견을 보였다. H. pylori가 아닌 Helicobacter (non-H. pylori Helicobacter, NHPH) 감염을 진단하기 위해 균염기서열 분석(pyrosequencing analysis)을 시행하였다(Fig. 3). 위내시경에서 관찰된 광범위한 병변의 진단은 무엇인가?

Gastroscopic findings. (A) Multiple, minute, whitish, and depressed erosions seen from the fundus to the upper body in the retroflexed view. (B) Multiple, minute hemorrhagic spots, also referred to as spotty redness, seen in the gastric rugae. Gastric biopsies were performed during the procedure. Yellow arrow indicates the biopsy sites. (C) Whitish ulcer scars and increased vasculature in the posterior aspect of the angle. Yellow arrow indicates the biopsy sites. (D) Regular arrangement of the collecting venules are observed in the antrum.

Pathology findings for the gastric biopsy specimens obtained during the initial gastroscopy. Representative images of the upper body are shown here. Similar pathology findings observed using the biopsy specimens from the angle. (A) Atypical lymphoid infiltration seen in a lymphoepithelial lesion. The findings are consistent with extranodal marginal zone B cell lymphoma of the mucosa-associated lymphoid tissue (H&E, ×200). (B) Infiltrating lymphoid cells are po- sitive for CD20 which is specific for B cells (CD20 immunohistochemical stain, ×200).
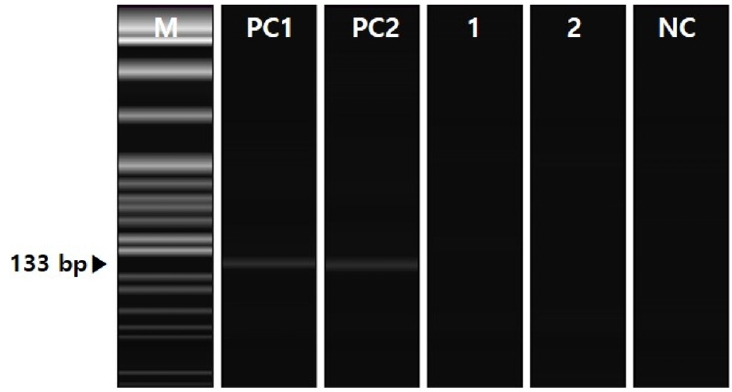
Findings of the pyrosequencing analysis to confirm the presence of Helicobacter pylori (H. pylori) and non-H. pylori Helicobacter. There is no evidence of the Helicobacter species in the specimens. M, marker (100 base pair [bp]); PC, positive controls showing Helicobacter at 133 bp; NC, negative control using deionized sterile water.
해설: H. pylori 음성으로 진단하기 위해서는 침습적인 검사와 비침습적인 검사에서 모두 음성 소견을 보여야 하며, 정상 혈관상이 보일 경우에는 H. pylori 미감염자일 가능성이 32.2배 상승한다[1]. 반대로 상부 체부에서 광범위한 발적이 보일 경우에는 H. pylori 감염자일 가능성이 26.8배 상승하며, 이는 활동성 H. pylori 감염을 시사하는 특징적인 소견으로 NHPH 감염성 위염에서 보고된 적이 없다[2]. Helicobacter suis 등의 NHPH 감염은 조기위암(early gastric cancer, EGC) 형태의 악성 종양, 결절성 위염, 소화성 궤양, 위각을 중심으로 한 대리석 모양의 경미한 위축성 위염, 전정부의 불균일한 발적이나 미란 등은 유발할 수 있지만 H. pylori 감염처럼 광범위한 발적이나 주름 비대는 유발하지 못한다[3].
이 증례는 상부 체부의 대만측을 중심으로 H. pylori 활동성 감염을 시사하는 점상 발적이 관찰되었으나 비침습적인 검사와 침습적인 검사 모두에서 H. pylori 음성으로 보고되었으며 NHPH도 진단되지 않은 드문 경우이다. 면역염색 결과에서 CD20 양성, CK 림프상피병변 양성, Ki-67 3~5% 양성, Bcl-2 양성, Bcl-6 음성, CD10 음성, CD3 음성으로 보고되어 H. pylori 음성인 위 말트 림프종(mucosa-associated lymphoid tissue [MALT] lymphoma)으로 진단하였다. 혈액 검사에서 젖산탈수효소(lactate dehydrogenase) 수치는 336 IU/L (참고치 263~450 IU/L)였으며 흉부와 복부 컴퓨터단층촬영(CT)에서 위의 좌측 림프절이 1.5 cm로 측정되었다(Fig. 4A, B). 병기는 Ann Arbor stage II1E, 국제예후지표(international prognostic index, IPI)는 낮은 IPI 위험도로 판단되었다. Clonal IgH gene rearrangement는 없었으며 apoptosis inhibitor 2 (API2)-MALT lymphoma-associated translation 1 (MALT1) chimera 유전자와 연관된 염색체 전위 11q21: t(11;18) (q21;q21)도 발견되지 않았다.
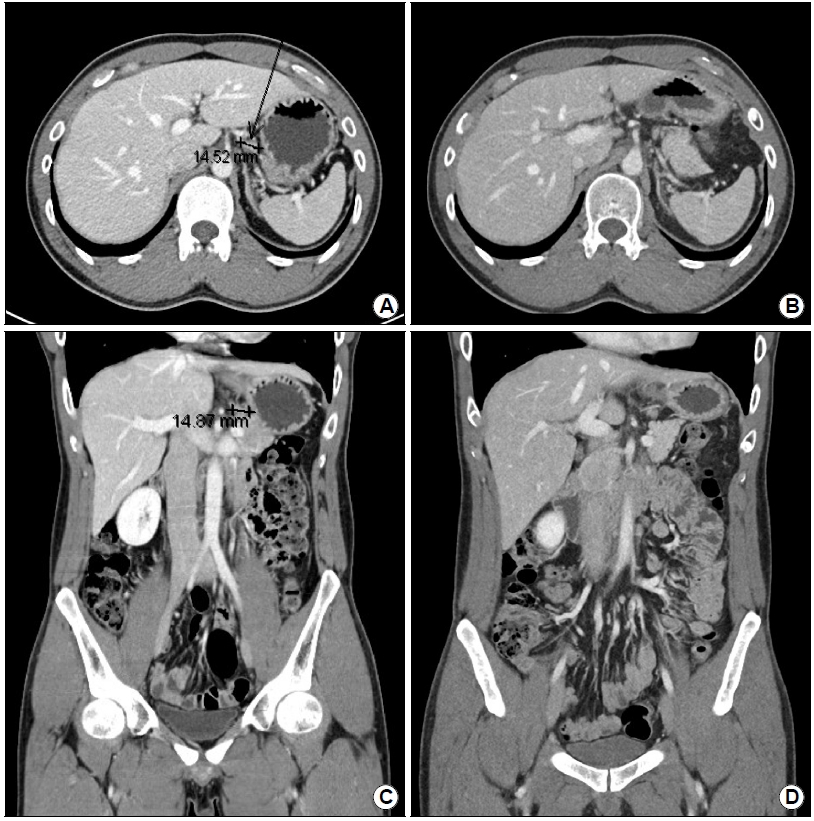
Findings of the initial and followup contrast-enhanced CT. (A) In the coronal view, a 1.5 cm sized left gastric lymph node (LN) is observed with edematous gastric wall thickening on the posterior side of the lower body. (B) In the axial view, a 1.5 cm sized left gastric LN is observed. (C) Four months after involved-site radiation therapy (ISRT) using a total dose of 30.6 Gy in 17 fractions, the enlarged LN in the coronal view is not visualized. (D) The axial view after ISRT shows a decrease in the size of the left gastric LN. There is no observable abnormality in the stomach.
10% 미만의 위 말트 림프종은 NHPH 감염이나 염색체 전위 또는 자가면역질환에 의해 발생하는 H. pylori 음성 림프종으로 진단된다[4]. 가장 흔한 원인은 NHPH 감염으로 일부는 H. pylori 제균 치료에 반응하지만[5], API2-MALT1 양성이면 관해율이 낮다[6]. 국내에서 가장 많은 위 말트 림프종 환자 345명을 분석한 연구에서는 57.1%의 H. pylori 음성 위 말트 림프종이 제균 치료로 관해되었다[7]. 메타분석 연구에 의하면 제균 치료 후의 H. pylori 음성 위 말트 림프종의 관해율은 29.3% (95% CI, 22.2~37.4%)로[8], 한국에서 관해율이 가장 높고 일본에서 가장 낮다[9]. 일본이 낮은 이유는 침습적인 검사, 혈청 항H. pylori IgG, 요소호기 검사뿐만 아니라 대변항원 검사와 혈청 PG 검사까지 모두 음성 소견을 보여야 H. pylori 음성으로 진단하기 때문으로 추정된다. 혈청 PG I 수치가 70 ng/mL 이하이면서 PG I/II 비가 3.0 이하로 혈청학적 위축이 보고되면 H. pylori 음성이 아닌 과거 감염자로 분류하므로[10], 우리나라에서는 H. pylori 음성인 종양이 일본에서는 과거 감염으로 인해 발생한 H. pylori 연관성 종양으로 진단되는 경향이 있다.
위 말트 림프종의 병기는 치료에 대한 반응을 예측하는 데 있어서 중요하며, H. pylori 양성인 IE기나 II1E기의 위 말트 림프종은 제균요법이나 적은 양(25.2 Gy)의 방사선 치료로 관해될 수 있다[11]. 제균 치료에 반응하는 H. pylori 음성 위 말트 림프종은 주로 위의 원위부에서 발생하며 H. pylori 감염성 위 말트 림프종과 유사한 함몰형 조기위암 유사형(EGC IIc-like type), 점막하 종양형(submucosal tumor type), 다발성 미란형(multiple erosion type), 조약돌형(cobblestone type), 부분적인 주름비대형(partial giant-fold type), 퇴색형(discoloration type) 등으로 관찰된다[12]. 반면에 제균 치료에 반응하지 않는 H. pylori 음성 위 말트 림프종은 주로 위의 근위부에서 상피하 종양이나 용종 같은 융기형 병변으로 진단되며 diffuse large B cell lymphoma와 유사한 모양으로 진행한다[13]. 방사선 치료에도 반응하지 않을 때는 항암 치료나 rituximab과 같은 항CD20 단클론항체 면역요법을 고려할 수 있다[11].
이 증례는 API2-MALT1 음성과 Helicobacter 음성인 II1E 병기의 위 말트 림프종으로 방사선 치료를 권하였으나 덜 침습적인 제균 치료에 대한 반응을 먼저 확인하길 원하여 amoxicillin 1 g, clarithromycin 500 mg, lansoprazole 30 mg을 하루 두 번 일주일간 투여하였다. 위내시경 소견이 제균 치료에 반응하는 다발성 미란형과 퇴색형 소견을 보였고, 조직 검사로 시행한 NHPH 진단이 위음성일 가능성도 있어서 제균 치료에 반응하길 기대했었으나 두 달 후의 위내시경 조직 검사에서 위 말트 림프종이 여전히 보고되어 지체 없이 방사선 치료(30.6 Gy, 17 fractions)를 권하였다. 방사선 치료를 마친 후 4개월 뒤에 시행한 CT 검사에서 작아진 림프절이 확인되었다(Fig. 4C, D). 위내시경 검사상 상부 체부에서 관찰되던 흰색 함몰형 미란들은 이전에 비해 감소하였으며(Fig. 5A), 위주름의 점상 발적은 사라진 상태였다(Fig. 5B). 위각의 후벽에는 조직 검사한 흔적만 남아있었다(Fig. 5C). 처음에 림프종이 진단되었던 체부의 대만과 위각의 후벽에서 추적 조직 검사를 하였으나 모두 음성으로 보고되었다.
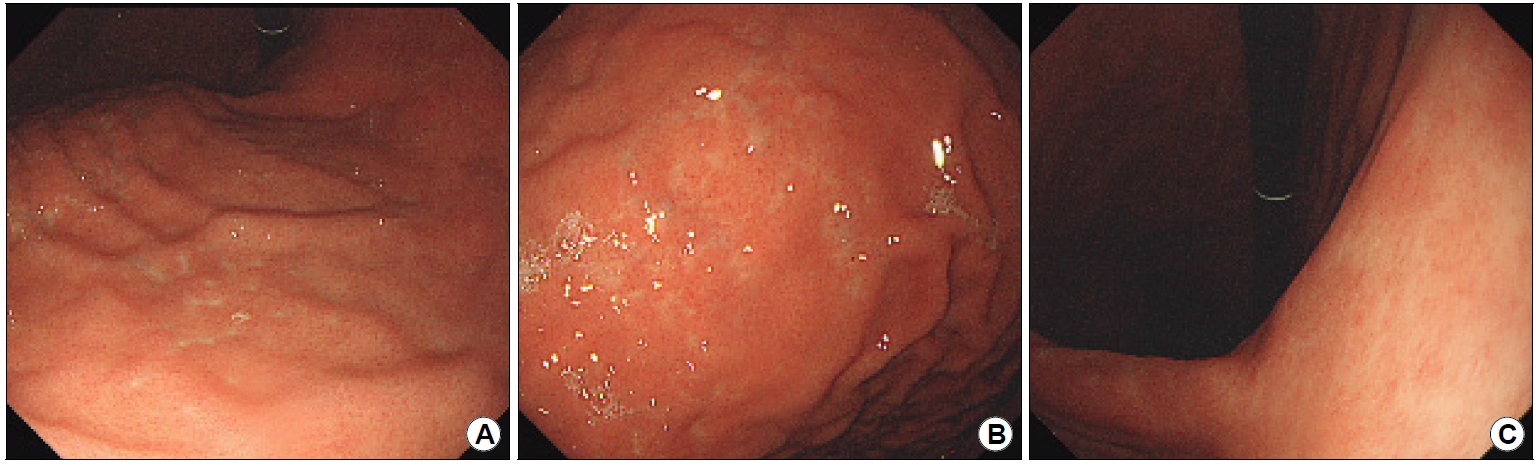
Gastroscopic images obtained after involved-site radiation therapy (ISRT). (A) Four months after ISRT, a decreased number of whitish and depressed erosions is observed in the fundus. (B) Previous lesions that extended from the greater curvature side of the upper body to the fundus are resolved. (C) On the posterior side of the angle, a previous ulcer has healed to a whitish scar.
종합할 때, 이 증례는 비침습적인 검사(혈청 검사와 요소호기 검사)와 침습적인 검사(H&E와 Giemsa 염색, 균염기서열분석)에서 모두 음성 소견을 보인 H. pylori 음성 위 말트 림프종으로, 활동성 H. pylori 감염을 시사하는 점상 발적을 보인 특이한 증례이다. 육안적인 소견은 제균 치료에 잘 반응하는 다발성 미란형과 퇴색형을 보였으나 제균 치료에 반응하지 않아서 방사선 치료가 필요하였다. 이처럼 육안적으로는 H. pylori 감염성 위 말트 림프종을 의심할 수 있는 소견을 보여도 방사선 치료 후에야 관해된 H. pylori 음성 위 말트 림프종을 경험하였기에 보고한다.
Notes
No potential conflict of interest relevant to this article was reported.
