장기간 양성자펌프억제제를 복용한 Helicobacter pylori 미감염자에서 발생한 위 체부의 비후와 출혈성 과형성 용종
Gastric Corpus Hypertrophy with a Bleeding Hyperplastic Polyp in a Helicobacter pylori-naive Subject after Long-term Proton Pump Inhibitor Use
Article information
Trans Abstract
A 22-year-old man presented with recurrent dizziness and melena. He had no remarkable medical history except for the reflux symptoms for which 18 months of proton pump inhibitor (PPI) intake was required. Gastroscopy revealed a 1-cm, blood-tinged polyp within the gastric rugae. A thickened gastric corpus was observed with a regular arrangement of collecting venules on its surface. Hyperplastic foveolar epithelium was observed in the biopsied specimens from the fundus and gastric rugae. The diagnosis after polypectomy was gastric hyperplastic polyp. Abdominal CT revealed hypertrophy only in the gastric corpus without antral involvement. Increased levels of serum pepsinogen I (>160 ng/mL), pepsinogen II (>50 ng/mL), chromogranin A (>1,800 ng/mL), and gastrin (534 pg/mL) were noted. Three months after PPI discontinuation, CT revealed improvement of the hypertrophic gastric corpus. Serum chromogranin A and gastrin levels decreased to 950.4 ng/mL and 517.0 pg/mL, respectively. Herein, we report a young, Helicobacter pylori-naive patient with prominent hyperplasia in the gastric corpus and a bleeding hyperplastic polyp after long-term PPI use.
서 론
위산억제제를 장기간 복용하는 환자들이 많아지면서 다양한 부작용이 보고되고 있다[1]. 양성자펌프억제제(proton pump inhibitor, PPI)를 복용하면 위저선의 벽세포(parietal cell)는 억제되지만 장크롬친화유사(enterochromaffin-like) 세포, 주세포(chief cell), 가스트린(gastrin) 세포는 상대적으로 활성화되어 chromogranin A, 히스타민, 펩시노겐(pepsinogen, PG), 가스트린 분비가 증가한다[2]. 이 중에서 고가스트린혈증은 선와상피 증식(foveolar epithelial hyperplasia)과 벽세포의 돌출을 유발하여 위선 협부(glandular isthmus)를 막아 위저선의 낭성 확장을 유발한다[3]. 그리고 이러한 변화가 장기간 누적되면 위저선 용종이나 과형성 용종, 다발성 흰색 융기형 병변(multiple white elevated lesion)이나 조약돌 모양의 점막(cobblestone-like mucosa)이 형성된다[4].
PPI 복용 후에 용종이 발생하는데 걸리는 평균 기간은 32.5개월로[5], 혈청 가스트린 수치가 400 pg/mL 이상으로 높으면 과형성 용종이 발생하기 쉽다[6]. 위저선 용종은 Helicobacter pylori (H. pylori) 감염이 없을수록 호발하는데, PPI를 6개월 이상 복용하면 발생률이 4.71배 높아지고 1년 이상 복용하면 5.32배 높아진다[7]. PPI로 인한 위저선 용종은 다른 위저선 용종에 비해 낭성 확장이 크고 많으며, 선와상피 증식과 벽세포 돌출이 저명하고, Ki-67과 MUC5AC 염색에 양성 소견을 보이는 세포의 비율이 높다[8]. 아울러 벽세포에서 발현되는 aquaporin-4 water channel과 KCNQ1 potassium channel 염색에 양성 소견을 보이는 경우가 흔하고, 용종에서 출혈이 관찰되기도 한다[9]. 한편, 고령의 여성에서는 위저선의 낭성 확장과 벽세포 과형성이 다발성 흰색 융기형 병변으로 관찰되기 쉬운 반면[10], 고령의 남성에서는 조약돌 모양의 점막으로 관찰되기 쉽다[11]. 장상피화생이 있는 고령의 남성일수록 선와상피 증식과 벽세포 돌출이 제한되어 큰 용종을 만들지 못하고 소결절형 융기만 형성하기 때문이다[12].
이 증례는 H. pylori 감염력이 없는 22세 남성이 18개월간 PPI를 복용하던 중 흑색변이 발생하여 검사한 결과, 위 체부의 비후와 출혈성 과형성 용종이 진단된 증례이다. 용종 절제술과 PPI 복용을 중단한 후에 두꺼웠던 위벽이 호전되는 교훈적인 증례를 경험했기에 보고한다.
증 례
22세 남자가 2~3주 간격으로 흑색변과 어지러움이 반복되어 왔다. 1년 반 동안 속쓰림과 명치 통증이 있어서 1년간 omeprazole 40 mg을 복용하다가 증상이 심해져서 반년 전부터는 pantoprazole 40 mg으로 바꿔서 복용하는 중이라고 했다. 하지만 증상은 호전되지 않았으며, 수개월 전부터 심한 어지러움이 2~3주 간격으로 발생했다. 쓰러질 정도로 어지러운 뒤에는 반드시 냄새가 고약한 흑색변이 뒤따른다고 했다. 미국 국적의 백인 남성으로 다른 병력은 없었으며, 함께 내원한 모친이 실리악병(celiac disease)을 진단받았으나 치료 없이 관찰 중이었다. H. pylori 감염력이나 위장관 종양의 가족력은 없었다. 내원 당시의 키는 176.2 cm, 몸무게는 79.6 kg이었다.
혈액검사에서 백혈구 6.82×103/μm (참고치 4~10×103/μm), 적혈구 4.66×106/μm (참고치 4.2~6.3×106/μm), 혈소판 225×103/μm (참고치 140~400×103/μm), 헤모글로빈 13.6 g/dL (참고치 13~16.5 g/dL), 혈색소 38.8% (참고치 39~49%), mean corpuscular volume 83.4 fL (참고치 80~98 fL), mean corpuscular hemoglobin (MCH) 29.2 pg (참고치 27~33 pg), MCH concentration 35.1% (참고치 32~36%)로 보고되었다. 건강한 백인 남성의 정상 혈색소 수치가 14.0 g/dL 이상이라는 점을 감안할 때[13], 혈색소와 헤모글로빈 수치는 낮았으나 빈혈로 진단받거나 치료받은 적은 없다고 했다. 혈청 PG I 수치는 >160 ng/mL, PG II 수치는 >50 ng/mL, 가스트린 수치는 534.0 pg/mL (참고치 13~115 pg/mL), chromogranin A 수치는 >1,800 ng/mL (참고치 ≤108.0 ng/mL)로 높았다. PPI 복용 이외에 고가스트린혈증을 유발할 만한 다른 원인이나 질환은 없었다.
위내시경 검사에서 체부와 기저부는 점막의 비후와 위선 개구부(opening of gastric pit)의 확장을 보였으나, 전정부와 위각에서는 이상이 관찰되지 않았다(Fig. 1). 위주름 사이에서 발견된 용종에서 출혈이 관찰되어 용종 절제술을 시행했으며, 과형성 용종으로 진단되었다(Fig. 2A, B). 기저부와 체부에서 채취한 조직에서는 위저선의 낭성 확장과 선와상피 증식이 관찰되었으며, 림프구와 섬유아세포 침윤으로 인한 점막 비후를 보였다(Fig. 2C, D). H. pylori 감염은 비침습적인 혈청 항H. pylori immunoglobulin G IgG 검사와 침습적인 Giemsa 염색 모두에서 진단되지 않았으며, 장상피화생이나 위축도 관찰되지 않았다. 위각과 체부에서 규칙적인 혈관상이 관찰되었고, 현감염이나 과거 감염을 의심할 만한 소견이 없어서 요소호기 검사는 시행하지 않았다. 함께 시행한 대장내시경 검사에서는 이상이 관찰되지 않았다. 위용종 절제술 후에는 PPI 대신 히스타민 2 차단제(histamine 2 receptor antagonist, H2-blocker)인 famotidine 20 mg을 4주간 하루 2회 복용하도록 하였다.

Initial gastroscopic findings. (A) Edematous mucosal change and wide opening of gastric pits are observed in the corpus. (B) On the greater curvature side of the upper body, a 1 cm-sized, semi-pedunticular polyp is observed. Minimal amount of fresh blood is observed on the polyp. (C) A regular arrangement of collecting venules (RAC) is observed on the surface of the gastric folds with edematous mucosal changes. (D) In the antrum and angle, RAC is observed without swelling.

Microscopic findings after gastric polypectomy and endoscopic biopsy. (A) Cross-sectional view shows the serrated and star-like appearance of the mucosal pits (H&E stain, ×40). These findings are consistent with those of a hyperplastic polyp. (B) The resected polyp showing the elongated and dilated foveolar epithelium with red blood cell aggregation (arrow) (H&E stain, ×100). (C) The biopsied specimen of the fundus showing the inflammatory reaction of the stroma with an elongated and dilated foveolar epithelium. The lamina propria is infiltrated by lymphocytes and fibroblasts (H&E stain, ×100). (D) The biopsied specimen of the gastric rugae showing the inflammatory reaction of the stroma without intestinal metaplasia or atrophy. Edematous stroma is visible with hyperplastic foveolar epithelium (H&E stain, ×200).
복부 컴퓨터촬영(CT) 검사에서 위체부와 기저부의 위벽 비후를 보였다(Fig. 3A, B). 보만 4형의 진행성 위암이나 림프종을 시사하는 불규칙한 조영증강이나 주변 조직 침범, 림프절 비대 등은 관찰되지 않았다. 위내시경과 CT 검사 소견으로 볼 때, 초음파 내시경 검사를 시행하더라도 치료계획(PPI 중단과 위용종 절제술)이 바뀌지 않을 것으로 예상되어 시행하지 않았다. PPI를 중단한 3개월 후의 CT 추적 검사에서 근위부의 위벽 비후는 호전된 소견을 보였다(Fig. 3C, D). 추적한 혈청 가스트린 수치는 517.0 pg/mL, chromogranin A 수치는 950.4 ng/mL로 각각 감소 중이었다. PPI 복용을 중단한 이후에 흑색변은 없었으며, 혈색소 수치는 15.7 g/dL 이상으로 안정적으로 유지되었다. 증상이 재발하면 H2-blocker를 권하려고 했으나, 이전과 같은 심한 증상은 없다고 하여 치료 없이 관찰 중이다.
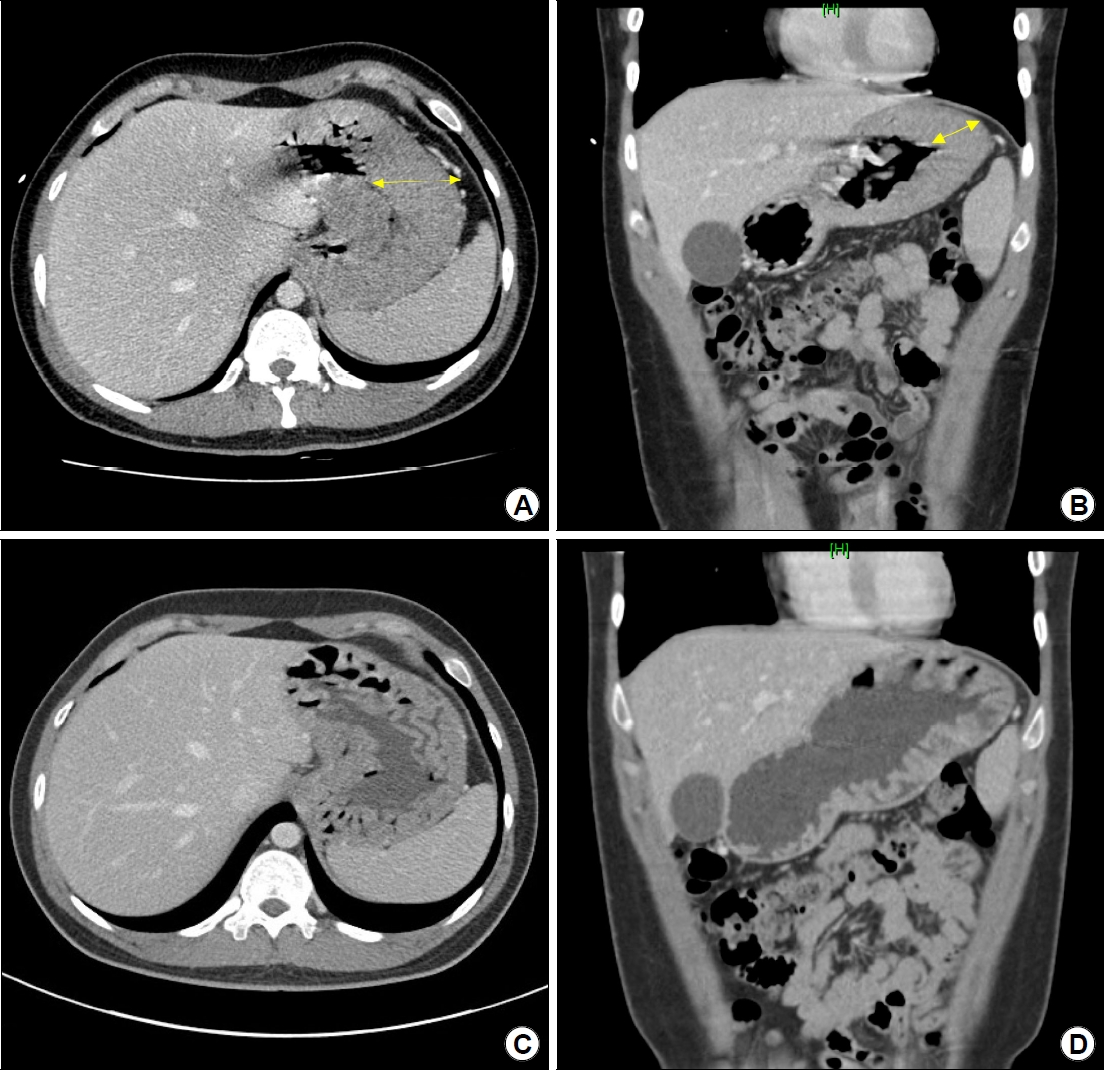
Findings of abdominal contrastenhanced CT. (A) Axial view of the stomach showing gastric corpus hypertrophy (yellow arrow) from the initial visit. (B) Coronal view showing gastric wall thickening (yellow arrow) only in the corpus. No wall thickening is observed in the antrum. (C) Axial view at three months after the discontinuation of the proton pump inhibitor (PPI) treatment shows improvement of the hypertrophic gastric corpus. (D) Coronal view at three months after the discontinuation of PPI treatment shows a remarkable improvement in the gastric corpus.
고 찰
이 증례는 H. pylori에 감염된 적이 없는 젊은 미감염자가 PPI를 장기간 복용한 후에 선와상피 증식과 위저선의 낭성 확장이 과도하게 발생하여 상부위장관 출혈까지 유발한 드문 경우이다. 진단 당시에는 위 근위부의 비후와 함께 혈청 가스트린과 chromogranin A 수치의 상승이 관찰되었으나, PPI 복용을 3개월간 중단한 후에 위벽의 비후와 혈청 수치가 호전되는 소견을 보였다.
위저선의 벽세포를 억제하는 약물 복용으로 인한 위점막의 변화는 주로 고가스트린혈증에 의해 발생한다(Fig. 4). 위축이나 장상피화생이 없는 미감염자일수록 큰 용종이 발생하기 쉬우며(Fig. 5), 위암은 드물다[14]. 과형성 용종이 발생한 경우에도 예후는 양호하여 PPI를 중단하는 것만으로도 83%가 작아지거나 사라진다[15]. 그러나 H. pylori 감염자라면 선암으로 진행할 수 있으므로, PPI 중단과 함께 제균 치료를 해야 한다[16]. 향후에도 PPI나 potassium-competitive acid blocker (P-CAB) 복용을 피해야 하는데, P-CAB는 PPI보다 위산 억제 효과가 탁월한 만큼 고가스트린혈증의 발생률도 높기 때문이다[17]. P-CAB를 1년 이상 복용하면 8.8%에서 위저선 용종이 발생하고 1.3%에서 과형성 용종이 발생한다는 내용의 초록이 2018년 일본소화기내시경학회에서 발표되었으며(unpublished data), 3년간 vonoprazan 10 mg을 복용한 51세 남성에서 선와형 위선암(foveolartype gastric adenocarcinoma)이 발생했다는 증례보고도 있다[18]. 따라서 복용이 불가피한 상황에서는 고가스트린혈증을 줄이기 위해 muscarinic receptor antagonist인 pirenzepine을 병용하거나[19], H2-blocker을 함께 투여해 용량을 줄이도록 한다[20]. H2-blocker는 PPI나 P-CAB와 달리 고가스트린혈증이나 PG 상승 및 위저선 증식을 유발하지 않기 때문이다[21]. 제균 치료 시에는 PPI를 1~2주만 투여하기 때문에 이조차 금기해야 한다는 연구는 없다. 다만 장기간 PPI를 투여해온 감염자의 위 내 pH는 이미 상승되어 불충분한 위산 억제로 인한 제균 실패의 가능성은 낮을 것이므로 PPI 대신 H2-blocker를 고려해볼 수 있을 것이다.

Changes induced by long-term use of acid suppressants acting on the parietal cells long-term inhibition of proton pumps in the parietal cells leads to hyperplasia of gastrin (G) cells, enterochromaffin-like (ECL) cells, and chief cells in the fundic gland. These changes induce the hypersecretion of gastrin from the G cells; chromogranin A and histamine from the ECL cells; and pepsinogen I from the chief cells. Hypergastrinemia induces foveolar epithelial hyperplasia, edematous stroma, fundic gland extension, and proliferation of parietal and chief cells in the corpus. On endoscopy, corpus mucosal hyperplasia is visible as multiple white elevated lesions, a cobblestone-like mucosa, fundic gland polyps, or a hyperplastic polyp. HCO3-, bicarbonate; M3, muscarinic acetylcholine type 3 receptor; H2, histamine type 2 receptor; ATPase, adenosine triphosphatase; CCK2, cholecystokinin type 2 receptor.

Representative cases of gastric mucosal lesions found in Koreans after long-term use of proton pump inhibitor. (A) A 38-year-old, H. pylori-naive woman presented with a large semi-pedunculated polyp in the cardia. A 3.5×2.0×1.6 cm hyperplastic polyp was diagnosed after gastric polypectomy. She was taking pantoprazole (40 mg) with prednisolone once a day since kidney transplantation in 2013. She had no history of H. pylori infection, and all previous H. pylori tests performed in 2013, 2020, and 2021 showed negative findings. (B) There is no notable finding in the antrum in this 38-year-old H. pylori-naive subject. (C) Cobblestone appearance is observed in the retroflexed view of the corpus in a 72-year-old man with a history of successful H. pylori eradication in 2010. He was taking 20 mg of rabeprazole every day for 7 years because of recurrent reflux symptoms. The serum anti-H. pylori IgG titer was 6.3 AU/mL (seronegative) and Giemsa staining findings were negative. The serum pepsinogen (PG) I level was >160 ng/mL, PG II level was 20.6 ng/mL, and PG I/II ratio was 11.3. (D) Metaplastic gastritis is observed in the antrum without a cobblestone appearance in a 72-year-old man with a history of infection. (E) Multiple white elevated lesions are observed in the fundus of a 57-year-old woman. She was taking 60 mg of dexlansoprazole daily for 2 years. She had undergone H. pylori eradication in 2005. On the day of endoscopy, serum anti-H. pylori IgG titer level was <5 AU/mL. The serum PG I level was 116.0 ng/mL, PG II level was 15.0 ng/mL, and PG I/II ratio was 7.7. Biopsied specimens taken from white elevated lesions near the cardia (yellow arrow) are consistent with fundic gland polyps. (F) An atrophic border is observed in the greater curvature side of the proximal antrum in a 57-year-old woman with a past infection. There are no white elevated lesions in the antrum. H. pylori, Helicobacter pylori.
고가스트린혈증은 PPI나 P-CAB 복용 이외에도 식후, 신부전, 자가면역성 위염, H. pylori 감염에 의한 위축성 위염, Zollinger-ellison 증후군에서도 관찰되는 소견으로, PPI를 5년간 복용하면 정상 수치의 1.4배인 200 pg/mL 전후로 상승되고 복용 기간이 길수록 수치도 증가한다[22]. 만약 혈청 가스트린 수치가 1,000 pg/mL를 초과하고 위 내 pH가 2 미만이라면 가스트린종을 의심해야 한다[23]. 또한 PPI 장기 복용자에서 가스트린 수치가 높다면 위 신경내분비 종양을 의심해야 한다[24]. 유럽의 다기관 연구에서 발표한 위 신경내분비 종양 환자들의 혈청 가스트린 수치는 964 (585~1,702) pg/mL였으며[25], 일본의 다기관 연구에서는 2,305 (279~22,956) pg/mL였다[26]. 따라서 일본에서는 PPI나 P-CAB 장기 복용자에서 혈청 가스트린 수치가 700 ng/mL 이상으로 높게 나오면 신경내분비 종양에 대해 검사하는 분위기가 조성되어 있으나, 증례가 드물어서 아직 전세계적으로 cutoff value에 대한 연구는 없다. 한편, 혈청 chromogranin A 수치는 1형 당뇨나 자가면역성 질환에서도 상승되므로 혈청 가스트린에 비해 종양에 대한 진단적 가치가 낮아서 치료 효과 판정이나 재발 예측용으로만 사용한다[27].
이 환자의 경우, 흑색변이 나타나기 18개월 전부터 PPI를 복용했으며(temporal relationship), PPI 이외에 다른 원인을 찾을 수 없었다(coherence). 또한, PPI 복용 후에 관찰된 검사 소견들이 기존 보고들과 일치했으며(consistency), 특이한 소견들(specificity)이었다[1-3,5-8,12]. 다만, 이 환자가 출혈로 인한 증상을 느낀 것은 총 4~5회로 수혈을 요할 정도로 많은 양은 아니었기에 헤모글로빈 수치는 13.6 g/dL, 혈색소 수치는 38.8%로 경미한 감소만 보인 것으로 추정된다. 아울러 고가스트린혈증이 심할수록 위저선 용종보다 과형성 용종이 발생하기 쉬운데[28], 이 환자에서도 혈청 가스트린 수치가 높게 측정되어 과형성 용종과의 연관성을 찾을 수 있었다(strength). 나아가서 PPI를 중단한 이후에 위벽의 비후가 3개월 만에 호전되었고, 혈청 가스트린과 chromogranin A 수치도 감소하는 연관성도 관찰되었다. 이 증례에서 chromogranin A 수치가 최고치인 >1,800 ng/mL에서 950.4 ng/mL로 빠르게 감소하면서 증상도 호전된 것으로 볼 때, 환자가 처음에는 위산과다로 인해 PPI를 복용하기 시작했지만 이후에는 PPI 부작용으로 인해 위 근위부가 팽창하면서 증상이 발생한 것으로 추정된다. 위 5가지 특성들(temporal relationship, coherence, consistency, specificity, strength)을 종합할 때, 이 증례는 장기간 PPI 복용으로 인한 약제성 병변으로 해석된다.
결론적으로 이 증례는 젊은 나이의 미감염자가 18개월간 PPI를 복용하면서 기저부와 체부의 위점막이 과도하게 증식했고, 동반된 과형성 용종이 출혈된 경우이다. 출혈성 용종에 대한 내시경 절제술과 PPI복용 중단 이후에 흑색변은 사라졌으며, CT에서는 위벽의 부종이 호전되었고 혈청 가스트린과 chromogranin A수치는 감소했다. 위축이나 장상피화생이 없는 미감염자가 장기간 PPI를 복용한 이후에 위장관 출혈이 발생할 수 있다는 것을 상기시켜준 증례였다. 갈수록 국내에서도 미감염자의 비율이 증가하고 있고, PPI나 P-CAB를 장기 복용하는 사람들도 증가하고 있으므로 특징적인 검사 소견들을 종합해서 보고하였다.
Notes
No potential conflict of interest relevant to this article was reported.
