칼륨 경쟁적 위산분비 억제제의 위산연관질환에서 효과
Role of Potassium-competitive Acid Blockers in the Treatment of Gastric Acid-related Disorders
Article information
Trans Abstract
Owing to their superior pharmacokinetic and pharmacodynamic profiles, potassium-competitive acid blockers (P-CABs) score over proton pump inhibitors (PPIs) in the treatment of gastric acid-related disorders and may provide clinical benefit in the management of these conditions. Previous studies have compared P-CABs with PPIs for treatment of gastric acid-related disorders, and current data show that P-CABs are non-inferior to PPIs in the treatment of erosive esophagitis and as maintenance therapy. P-CABs are useful for effective healing and as maintenance medications in patients with severe esophagitis. These drugs also aid with healing of peptic ulcers and artificial ulcers secondary to gastric endoscopic submucosal dissection (ESD). Few studies have discussed prevention of delayed ulcer bleeding after gastric ESD and ulcers associated with long-term nonsteroidal anti-inflammatory drug administration. Well-controlled, large-scale prospective studies are warranted in future to compare P-CABs with PPIs.
서 론
칼륨 경쟁적 위산분비 억제제(potassium competitive acid blocker, P -CAB)은 H+, K+-ATPase의 K+ exchange channel에 경쟁 결합하여 H+ 교환과정을 방해함으로써 위산 분비를 억제한다. P-CAB은 양성자펌프 결합이 가역적이고 경쟁적이다. 양성자펌프억제제(proton pump inhibitor, PPI)의 경우 pH가 4 미만에서 활성화되는 전구약물의 형태이지만, P-CAB은 활성 약물이므로 위산에 의한 활성화가 필요하지 않다. 그러므로 식전, 식후 관계없이 투여할 수 있고. 위산억제효과가 빠르게 나타난다. P-CAB의 위산분비 억제 효과는 길게 지속되므로 야간 산분비돌파를 억제하는 데 효과적이다. Cytochrome P (CYP) 2C19에 의해 대사되는 PPI는 유전적 다형성에 의한 개인차이가 있으며 클로피도그렐 등 약제 상호작용의 가능성을 고려해야 한다[1.2]. 하지만 CYP3A4에 의해 대사되는 P-CAB은 개인차가 작고 상호작용을 보이는 약물이 적다. 이러한 약동학적 장점때문에 위산관련질환에서 표준 치료제인 PPI와 동등 이상의 효과를 보일 것으로 예상되고 있다[1.2].
1세대 P-CAB으로 개발된 레바프라잔(revaprazan)이 사용된 이후 보노프라잔(vonoprazan), 테고프라잔(tegoprazan), 펙수프라잔(fexuprazan), 케베프라잔(keverprazan) 등의 임상결과가 보고되고 있다. 대부분의 P-CAB은 한국, 일본 등에서 개발되어 아시아환자의 임상결과가 대부분이지만 최근 보노프라잔은 미국와 유럽에서 미란성식도염의 치료와 유지에 대한 3상 연구결과가 보고되었다. 본고에서는 P-CAB과 관련된 현재까지의 임상연구를 종합하고 효과와 안전성에 대해 PPI와 비교하고자 한다.
미란성식도염의 치료와 유지치료
위식도역류질환의 표준치료제는 PPI이다. 미란성식도염에서 8주, 비미란성역류질환에서 4주 표준용량의 PPI 치료가 권고된다. 2015년 보노프라잔 출시 이후 P-CAB의 위식도역류질환치료에 대한 많은 임상데이터가 축적되었다. 이 결과를 근거로 2020년 한국의 위식도역류질환 진단 및 치료에 대한 진료지침[3], 2021년 일본의 위식도역류질환 가이드라인에서 P-CAB은 PPI와 같이 위식도역류질환의 초기 표준치료로서 인정된다[4]. P-CAB은 1) 미란성식도염의 치료 및 증상완화, 2) 비미란성역류질환의 증상 완화, 3) 유지치료, 4) PPI에 반응하지 않는 위식도역류질환 등의 치료에서 PPI와 비교되고 있다. 메타분석에 포함된 연구는 보노프라잔연구가 대부분이지만, 테고프라잔, 리나프라잔(AZD0865), 케베프라잔의 연구결과도 포함되고 있다[5-7].
몇몇 메타분석의 결과는 다음과 같다. 7,023명의 환자가 포함된 19개 연구의 메타분석에서 보노프라잔은 PPI와 비교하여 효과적이었다. PPI와 비교한 식도염치유율의 상대적위험도(relative risk, RR)는 각 2, 4, 8주 치료기간 동안 1.09 (95% confidence interval [CI] 1.03~1.14), 1.03 (95% CI 1.00~1.07), 1.02 (95% CI 1.00~1.05)로 PPI보다 효과적이었다. 하지만 증상 완화효과는 동일하였다. 약물이상반응과 안전성은 PPI와 차이가 없었다[5].
다른 메타분석은 보노프라잔, 테고프라잔, 리나프라잔(AZD0865), 케베프라잔의 6개 임상연구를 종합하였다. 보노프라잔의 3개 연구를 종합하면 치료 2주간 PPI보다 효과적이었으나(RR 1.02, 95% CI 1.00~1.05), 4주(RR 1.03, 95% CI 1.00~1.07), 8주 (RR 1.02, 95% CI 1.00~1.05)에는 차이가 없었다. 테고프라잔(RR 1.00, 95% CI 0.90~1.11), 리나프라잔(RR 1.00, 95% CI 0.93~1.07), 케베프라잔(RR 1.01, 95% CI 0.90~1.14)의 4주 치유율은 차이가 없었다. 테고프라잔(RR 1.03, 95% CI 0.96~1.10), 케베프라잔(RR 1.07, 95% CI 0.99~1.14)의 8주 치유율도 PPI와 차이가 없었다[6,7].
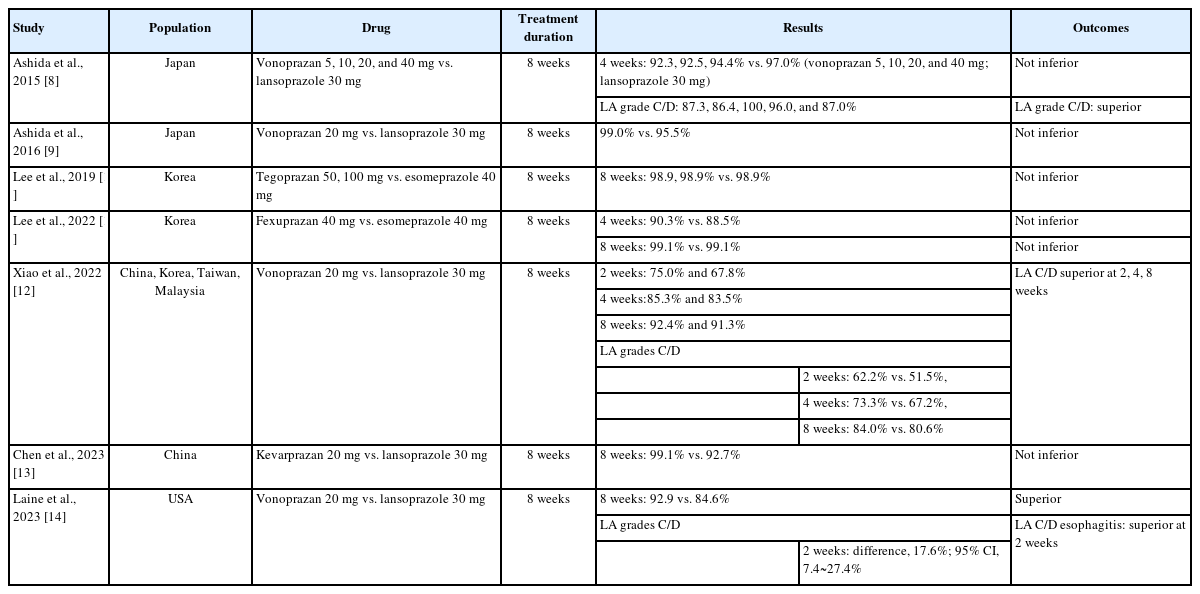
732명의 미란성식도염 환자를 대상으로 한 2상 연구에서 미란성식도염의 4주 치유율은 보노프라잔 5, 10, 20 및 40 mg과 란소프라졸 30 mg에서 각각 92.3, 92.5, 94.4, 97.0, 93.2%였다. 중증미란성식도염(로스앤젤레스 LA 등급 C/D)의 8주 치유율은 보노프라잔 5, 10, 20 및 40 mg과 란소프라졸 30 mg에서 각각 87.3, 86.4, 100, 96.0, 87.0%로 보노프라잔 20, 40 mg은 란소프라졸 30 mg보다 더 효과적이었다[8]. 3상 연구에서 미란성식도염 8주 치료율은 보노프라잔 40 mg에서 99.0%로 란소프라졸 30 mg 95.5%와 비교하여 비열등하였다. 역시 LA 등급 C/D에서 효과적이었으며 후속연구로 진행된 장기간 유지요법에서 LA 등급 C/D의 재발률은 10% 미만으로 낮았다. 혈청가스트린은 치료기간 동안 용량 의존적으로 증가하였다[9]. 테고프라잔 50 mg, 펙수프라잔 40 mg은 각각 란소프라졸 30 mg, 에소메프라졸 40 mg과 비교하여 4, 8주 미란성식도염 치료효과가 동일하였다. 테고프라잔, 펙수프라잔 연구에서 LA 등급 C/D의 중증식도염 환자의 비율이 낮아, 중증 식도염에서의 치료효과를 PPI와 비교하지 못하였다. 두 약제 모두 혈중 가스트린은 P P I와 비교하여 비슷한 정도로 상승하였다[10,11]. 보노프라잔은 최근 미국과 유럽에서 미란성식도염의 3상 연구 및 유지 치료의 결과가 발표되고 있다. 미국의 란소프라졸 대비 8주 치료에서 식도염소실율은 차이가 없었으나 LA 등급 C/D에서 더 효과적이었다. 6개월 유지치료도 마찬가지로 내시경관해의 유지율은 란소프라졸 대비 차이가 없었으나 LA 등급 C/D에서 더 효과적이었다[12]. 여러 임상연구결과를 종합하면 P-CAB 제제는 미란성식도염 치료에서 PPI와 동일한 효과와 안전성을 보이고 있으며, 중증 미란성식도염에서 효과가 있을 가능성이 있다(Table 1) [8-14].
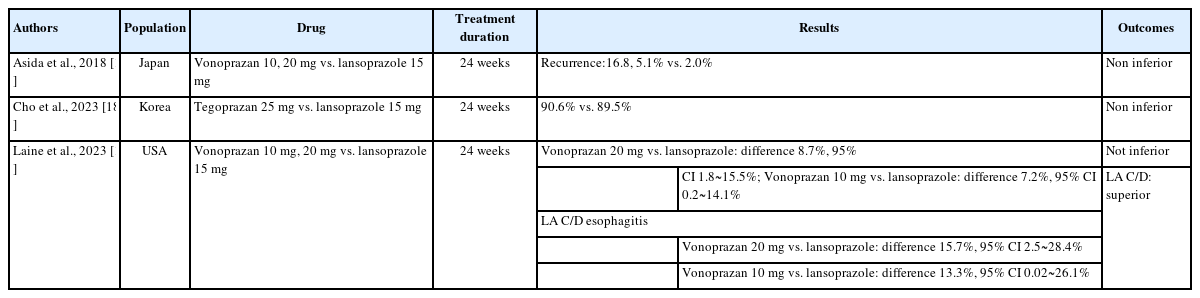
P-CAB은 미란성식도염의 치료뿐 아니라 유지에 있어 PPI에 비해 동등한 효능을 보였다(Table 2). Ashida 등[16]의 일본 3상 연구에 이은 후속연구에서 보노프라잔 10, 20 mg은 란소프라졸 15 mg에 비해 미란성식도염의 24주 재발률이 현저히 낮았다(각각 5.1, 2.0, 16.8%). LA 등급 A 또는 B에서 보노프라잔 10, 20 mg 치료군이 란소프라졸 15 mg 치료군보다 재발율이 낮았다(각각 3.1, 1.3, 11.0%) [16]. 기타 단일기관 관찰연구에서 보노프라잔 20 mg의 26, 52주 치료 동안 내시경관해 유지율은 92, 80% 정도였다 [17,18]. 테고프라잔 25 mg 6개월 유지요법의 경우 미란성식도염의 내시경관해 유지율은 90.6%로 란소프라졸 89.5%와 차이가 없었다. 혈중 가스트린은 대조약인 PPI와 비슷한 정도로 치료기간 중 상승하였다가 치료 종결 후 기저치로 감소하였다[19]. 연구결과를 근거로 일본의 위식도역류질환가이드라인에서 위식도역류질환의 유지치료로 저용량 보노프라잔 10 mg을 저용량 PP와 같이 권고하고 있다[4].
위식도역류질환에서 증상효과
미란성식도염 연구에서 Sakurai 등[20]의 연구와 여러 연구에서 식도염의 증상완화효과는 PPI와 비슷하였다. 비미란성역류질환 임상 시험의 경우 증상 평가에서 위약 효과가 크므로 유의성을 입증하기 어려운 제한점이 있다. 보노프라잔은 비미란성역류질환에서 가슴쓰림 증상을 호전시키는 데 위약대비 우월한 효과를 입증하지 못하였다[21]. 테고프라잔은 비미란성역류질환에서 위약 대비 4주 치료효과가 있었다(테고프라잔 50, 100 mg, 위약 각각 42.5, 48.5, 24.2%) [22]. 이 연구에서 위약군과 시험군 모두 증상소실율이 낮은 이유로 기능성 가슴쓰림환자가 두 군 모두 다수 포함되었을 가능성이 있다. PPI에 반응하지 않는 위식도역류질환환자에서 보노프라잔이 더 강한 위산억제 및 증상완화를 보인다는 몇몇 연구가 있으나 적은 수의 환자를 포함하는 소규모 연구여서, 아직 결론을 내리기 힘들다[23-26]. PPI의 치료반응으로 위식도역류질환을 진단하는 PPI 검사의 진단 정확도와 민감도는 높지 않다. PPI에 치료반응이 낮은 불응성 환자가 검사 정확도를 낮추는 원인으로 고려될 수 있다[4]. PPI 대신 P-CAB의 치료반응으로 위식도역류질환을 진단하는 P-CAB 검사는 아직 용량과 치료기간, 검사 방법이 정립되지 않았지만 PPI 진단검사의 대안으로 고려될 수 있다[4].
P-CAB의 위산억제효과가 빠르고 길기 때문에 야간산분비 돌파에 의한 야간 증상의 완화에도 효과적일 가능성이 있다. 32명의 미란성식도염 환자 연구에서 보노프라잔 20 mg은 란소프라졸보다 미란성식도염 환자들에게 치료 첫 주 동안 더 빠르게 가슴쓰림을 완화시켰다. 보노프라잔과 란소프라졸은 첫날 각각 31.3%와 12.5%의 환자에서 가슴쓰림이 소실되었다[27]. 46명의 미란성식도염 예비연구에서 테고프라잔의 2주 치료는 빠르게 야간증상을 완화시키는 데 에소메프라졸과 비슷한 효과가 있었다. 야간 속쓰림이 소실될 때까지의 시간은 테고프라잔 1.5일로 에소메프라졸 3일과 유의한 차이는 없었다(P=0.195) [28].
새로 개발된 P-CAB의 미란성식도염 임상결과
펙수프라잔은 혈장 평균 반감기가 약 9시간으로 여러 PPI와 비교하여 반감기가 긴 장점이 있다[29]. 263명의 미란성식도염 환자연구에서 내시경 치료율은 펙수프라잔의 8주 치료 후 99.1%, 4주치료 후 90.3%로 에소메프라졸 99.1, 88.5%와 비교하여 차이가 없었다. 혈청 가스트린 수치와 약물 관련 부작용은 두 군 간에 차이가 없었다. 부분군 분석에서 펙수프라잔은 증상이 심한 환자에서 에소메프라졸군보다 증상완화 효과가 좋았으며 만성기침 증상이 에소메프라졸 치료군에 비해 큰 증상개선을 보였다[17]. JP-3301 (자스타프라잔)은 최근 종료된 미란성식도염 3상 연구에서 미란성식도염의 누적소실율은 8, 4주 각각 97.9, 95.1%로 에소메프라졸 94.9, 87.7%와 차이가 없었다[30].
소화성 궤양
보노프라잔 20 mg은 4주간 위궤양의 누적치료에서 란소프라졸 30 mg 대비 비열등하였다(각각 93.5, 93.8%; P=0.0011) (Table 3). 그러나 십이지장 궤양은 란소프라졸대비 비열등성이 확인되지 않았다(각각 95.5%, 98.3%; P=0.0654) [31,32]. 한국과 인도에서 시판된 첫 번째 P-CAB인 레바프라잔(revaprazan)은 8주 십이지장 궤양과 위궤양의 치유에서 오메프라졸과 유사한 누적 치유율을 보였다(각각 99.1, 100%; P=0.322) [33]. 테고프라잔 50, 100 mg의 8주 위궤양누적치유율은 94.8, 95.0%로 란소프라졸 30 mg의 95.7%와 차이가 없었다[34].
위내시경 점막하박리술 후 발생한 의인성 궤양과 출혈예방
내시경 점막하 박리술(endoscopic submucosal dissection, ESD)의 주된 합병증은 출혈과 천공이다. PPI는 ESD 시술로 유발된 의인성 궤양의 치유를 촉진하고 출혈을 예방하기 위해 사용된다. 내시경 절제술로 인한 의인성 궤양에서 궤양이 P-CAB 치료로 얼마나 빠르고 잘 치유될 수 있는지에 대한 여러 연구가 보고되었다. 현재까지 보노프라잔에 대한 연구는 보고된 바가 많지 않다. Ichida 등[35]의 연구에서 보노프라잔과 레바미피드 병합치료는 에소메프라졸과 레바미피드 병합치료에 비해 우수한 궤양치료 효과를 보이지 않았다. 테고프라잔 50 mg은 란스톤 30 mg에 비해 4, 8주 궤양 치유효과가 비열등하였다[36].
보노프라잔은 ESD 후 궤양 출혈을 예방하는 데 효과적일 수 있다. Hamada 등[36]은 보노프라잔 치료군에서 위 ESD 후 지연 출혈률이 란소프라졸에 비해 낮다고 보고하였지만 차이가 작고 69명 환자가 포함된 단일기관연구라는 한계가 있다. 최근 일본에서 시행된 1,715명을 포함한 전국규모 후향적코호트 연구에서 보노프라잔 치료군은 다양한 PPI 치료군보다 출혈률(11.9% vs. 17.2%; P=0.008)과 2일에서 30일 사이의 출혈률(7.8% vs. 11.8%; P=0.015)이 낮았다[38]. 49명 환자가 참여한 소규모의 단일기관연구에서 보노프라잔은 지속적인 항혈소판 치료를 사용하는 환자의 ESD 후 출혈을 예방하는 데 효과적이었다[39]. 하지만 P-CAB의 출혈예방효과를 PPI와 비교하기 위해서는 대규모의 추가 비교 연구가 필요하다.
NSAIDs 장기 사용자의 소화성 궤양 예방
Nonsteroidal anti-inflammatory drug (NSAID) 장기 사용자의 궤양 재발 예방에 대한 몇몇 연구가 보고되었다. 10 mg과 20 mg의 용량 모두에서 보노프라잔은 24주간 NSAID를 복용하는 환자에서 란소프라졸 15 mg에 비해 비열등하였다. 24주 NSAID 복용 후 궤양발생율은 보노프라잔 10, 20 mg, 란소프라졸 15 mg이 각각 3.3, 3.4, 5.5%였으며 유의한 약제관련 부작용은 없었다[40]. 유의한 안전 문제는 확인되지 않았다. 14, 24주 연구와 장기간 연장 연구 모두에서 보노프라잔에비해 란소프라졸의 위장관 출혈률이 더 높았다[41]. 테고프라잔과 펙수프라잔의 장기 NSAID 사용으로 유발된 궤양에 미치는 영향에 대한 3상 연구가 진행 중이다.
결 론
P-CAB은 현재까지 임상결과에서 미란성식도염의 치료, 비미란성역류질환의 증상 완화, 유지치료에서 PPI와 동일한 효과와 안전성을 보이고 있다. 심한 미란성식도염의 치료에 효과적일 가능성이 제시된다. PPI에 반응하지 않는 위식도역류질환 치료에서 P-CAB의 효과에 대해서는 더 많은 연구가 필요하다. P-CAB은 소화성궤양과 내시경절제술 후 의인성궤양 치료에서 PPI와 동일한 효과와 안전성을 보이고 있다. 내시경절제술 후 출혈예방과 NSAID관련 궤양의 예방효과에 대하서는 더 많은 연구가 필요하다.
Notes
AVAILABILITY OF DATA AND MATERIAL
The datasets generated or analyzed during the study are available from the corresponding author on reasonable request.
CONFLICT OF INTEREST
There is no potential conflict of interest related to this work.
AUTHOR CONTRIBUTIONS
Conceptualization: Mun Young Cho and Yu Kyung Cho. Data curation: Mun Young Cho and Yu Kyung Cho. Formal analysis : Mun Young Cho and Yu Kyung Cho. Supervision: Yu Kyung Cho. Writing - original draft: Mun Young Cho and Yu Kyung Cho. Writing - review & editing: Yu Kyung Cho.
FUNDING STATEMENT
None.
ACKNOWLEDGMENTS
None.