 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 19(3); 2019 > Article |
|
Abstract
Endoscopic ultrasonography (EUS) is commonly used to detect the depth of cancer invasion in the preoperative stage. Intrapapillary capillary loop (IPCL) patterns observed in magnification endoscopy with narrow band image are also known to well demonstrate cancer invasion depth. Here, we report a case of superficial esophageal cancer with massive submucosal invasion, which presented as a superficial esophageal cancer confined to the mucosal layer and with a coincidental hypoechoic submucosal tumor under EUS and IPCL evaluation.
표재성 식도 편평상피세포암종(superficial esophageal squamous cell carcinoma)은 조기위암에 대응하는 식도암의 분류로서 림프절 전이의 위험이 충분히 낮은 경우 내시경적 점막하 박리절제술(endoscopic submucosal dissection, ESD)을 근치적 치료방법으로 적용할 수 있다[1,2]. 표재성 식도편평상피세포암종의 침범 깊이를 평가하기 위하여 내시경 초음파 검사(endoscopic ulrasonography, EUS)와 확대-협대역 내시경을 이용한 유두내 모세혈관 고리(intrapapillary capillary loops, IPCLs) 패턴 관찰법이 널리 사용되고 있으며 전체적인 예측 정확도는 약 90%에 이른다[3]. 건강보험심사평가원 통계에 따르면 우리나라에서는 2017년 한 해 동안 452건의 식도 점막하 박리절제술이 시행되었다[4]. 국가 암 검진 사업의 참여가 늘어나고 내시경 검사의 접근성이 향상됨에 따라 식도암의 조기 진단 빈도가 늘어날 것이다. 따라서 표재성 식도편평상피세포암종의 정확한 진단과 적절한 평가를 위한 경험을 지속적으로 축적하고 특이한 증례에 대한 정보를 공유하는 것이 중요하다. 저자들은 협대역 내시경(narrow band imaging) 관찰 결과 상피암 또는 고유판에 국한된 표재성 식도암의 특성을 보이며 초음파 내시경에서 식도벽의 층별 구조와 연속성에 단절이 없었지만, ESD 결과 점막하층에 현저한 침윤으로 덩어리를 이룬 점막하 침윤 표재성 식도암 1예를 경험하여 문헌 고찰과 함께 보고하는 바이다.
58세 남자가 상부위장관 내시경 검사에서 우연히 발견된 식도의 표재성 병변과 동반된 상피하 종양에 대하여 의뢰되었다. 남자는 50갑년의 흡연력이 있는 현성 흡연자였으며 일주일에 한 번 정도의 음주를 하였다. 앓고 있는 질환이나 복용하는 약물은 없었다. 삼킴 곤란이나 체중 감소 증상도 없었다. 활력징후는 정상 범위에 있었으며 신체 검사에서 이상 소견은 없었다. 혈액학 검사와 혈액화학 검사의 결과는 모두 정상 범위 안에 있었다.
상부위장관 내시경 검사 결과 종축이 약 2 cm 길이인 지도 모양의 표재성 편평형 발적을 띄는 병변을 절치 아래 31~33 cm 위치에서 확인하였다(Fig. 1). 표재성의 편평형 발적 병변은 표면이 미세한 과립상으로 거친 질감이었다. 병변의 근위부쪽은 편평하였지만 원위부쪽은 불쑥 튀어 올라 상피하 종양의 동반을 시사하였다. 루골액을 도포하였을 때 표재성의 편평형 발적병변은 연분홍색으로 변색되는 두 개의 구별되는 병변이 서로 인접한 것으로 드러났다. 고해상도 근접 협대역 영상에서 두 개의 병변은 각기 명확한 경계선을 가지고 있었으며, IPCLs은 비정상적으로 확장되고 불규칙적으로 배열된 둥근 점으로 나타나 일본내시경학회(Japanese Endoscopy Society, JES) 분류 B1형으로 판단하였다.
병변의 원위부에 위치한 상피하 병변에 대하여 EUS를 시행하였다. 식도벽의 층 구조는 정상적으로 유지되었고 각 층의 연속성의 단절은 보이지 않았다. 상피층은 고에코의 1층으로 관찰할 수 있었는데 병변의 위치에서 층의 두께 변화나 단절은 없었다. 병변의 원위부에서 0.9 cm 크기의 점막하 균질한 저에코 종괴를 확인하였다. 종괴는 경계가 명료하였고 상피층과 고유근층에서 분리되어 있었다. 점막근층 기원의 평활근종으로 판단할 수 있는 EUS 소견이었다(Fig. 2).
상부위장관 내시경 겸자 생검 결과 중등도 분화를 보이는 편평상피세포암종으로 진단하였다. 흉부와 복부 전산화단층촬영에서 식도벽의 암은 구별되지 않았으며 주변의 림프절이나 원격 장기의 전이는 없었다. 내시경 검사와 협대역 영상, EUS, 전산화단층촬영 그리고 내시경 생검 병리 진단을 종합하여 식도의 병변은 상피 또는 고유판에 국한된 표재성 식도편평상피세포암종으로 판단하였고, 식도 ESD를 계획하였다. 병변의 원위부에 있는 상피하 종양도 상부의 편평상피세포암종과 함께 일괄 절제하기로 하였다.
ESD는 좌측와위로 전신 마취 하에 진행하였으며 합병증 없이 안전하게 일괄 절제로 완료하였다(Fig. 3). 절제술 후 회복은 양호하였으며 48시간 경과 시점부터 정상적인 식이를 시작하였다.
ESD로 절제된 검체에 대한 병리 진단은 절제술 전 임상적 판단과 차이가 있었다. 병변은 각각 분리된 두 개의 종양으로서 근위부는 1.4×1.2 cm 크기의 상피내암이었으며 원위부는 1.7×1.2 cm 크기의 중등도 분화의 편평상피세포암종으로 상피층의 기시부는 매우 작았으나 점막하층으로의 광범위 확장이 관찰되었다. 점막하층으로 침윤한 종양의 경계는 침습성보다는 밀어내는 양상을 보이는 덩어리를 형성하여 플라스크 병 모양의 상피하 종양 형태를 나타내었다(Fig. 4). 동반된 림프관, 혈관, 신경으로의 침습은 없었다. 절제된 조직의 수평면 변연은 암 조직의 침범이 없었으나 수직면은 암 침범이 존재하여 비근치적 치료로 판정하였다. 환자의 나이와 림프절 전이의 가능성을 고려하여 추가적인 식도 절제술을 시행하였다. 수술로 절제된 조직에서 총 14개의 림프절이 수거되었다. 수술 조직에 대한 조직 검사에서 잔존하는 암 조직이나 림프절 전이는 없었으며, ESD로 인한 반흔만 남아 있었다. 환자는 식도 절제술 후 경과 양호하며 1년 6개월째 재발이나 합병증 없이 건강한 상태이다.
식도암은 전 세계적으로 매년 약 45만 명에서 발생하고 있으며, 그 발생률은 증가하는 추세이다[5]. 식도암은 기원 조직에 따라 편평상피세포암종과 선암종(adenocarcinoma)으로 구별한다. 서구에서는 위식도 접합부의 바렛식도에서 기원한 식도선암종이 주로 많이 발생하지만, 우리나라에서는 편평상피세포암종이 대부분이다. 우리나라를 포함한 동북아시아와 중동에서의 편평상피세포암종의 발생은 연간 10만 명당 100명이며[6] 우리나라의 국가 통계 포털에 따르면 식도암 발생률은 10만 명당 4.9명으로 매년 약 2,500명의 새로운 환자가 발생한다[7].
표재성 식도편평상피세포암종은 점막과 점막하층에 침범이 국한된 식도암으로서 내시경 절제술의 대상이다. 특히 점막근층(m3)을 침범하지 않고 상피층과 점막 고유판에 국한된(m1-m2) 식도암은 림프절 전이의 위험이 1% 미만으로 내시경 절제술을 근치적 치료로 적용할 수 있다. 점막근층과 점막하층을 침범한 경우에도 내시경 절제술 이후 5년 암-특이-생존율은 95%로 식도 절제 수술을 받았던 환자의 93.5%와 차이가 없어 수술의 고위험군에서는 충분히 고려할 만하다[2]. 표재성 식도암에 대한 ESD를 적용하는 것에 대하여 일본의 진료지침은 상피층에 국한된 경우(m1)와 고유판에 국한된 경우(m2)를 절대 적응증으로, 점막근층을 침범한 경우(m3)와 점막하층 200 μm 또는 1/3까지 침범한 경우(sm1)를 상대적 적응증으로 분류하고 있다[1].
표재성 식도편평상피세포암종의 침범 깊이를 예측하기 위한 방법은 내시경 초음파 검사와 협대역 영상을 이용하여 점막의 미세표면 패턴과 미세혈관 패턴을 분류하는 것이 유용하다[8,9]. 협대역 영상을 확대 내시경으로 얻는 경우 IPCLs의 형태를 관찰하여 조직학적 진단과 침범 깊이를 추정할 수 있다. 현재까지 다양한 분류법이 제안되었으나 JES 분류 기준은 비교적 단순하여 관찰자 간 변이가 적은 장점이 있다. IPCLs이 직경 7~10 μm의 머리핀 고리 모양을 가지는 정상 패턴인 경우(type A) 상피 내 신생물을 포함하는 이형성증을 시사한다. IPCLs이 머리핀 고리 모양을 유지하되 혈관의 직경이 20~30 μm로 두꺼워지고 염주알이나 구불구불해진 형태로 바뀐 경우(type B1) 상피나 고유판에 국한된 편평상피세포암종으로 추정할 수 있다. IPCLs이 고리의 형태를 소실하고 불규칙한 주행과 중층의 배열을 가지는 경우(type B2) 점막근층 또는 점막하 1/3층을 침범한 편평상피세포암종으로 판단할 수 있다. 이보다 침습의 깊이가 깊은 점막하층 편평상피세포암종은 60 μm 이상으로 두꺼워진 IPCLs 형태를 보인다(type B3). 이렇게 분류하여 예측하는 경우 정확도는 80.4~94.1%에 이른다[3].
식도의 상피하 종양은 병리학적으로는 평활근종이 70~80%로 가장 흔하며 EUS에서는 저에코성 병변으로 나타난다. 근층 기원의 저에코성 병변으로 나타날 수 있는 위장관 기질종양(gastrointestinal stromal tumor)은 식도에서는 흔하지 않으며 다른 악성의 상피하 종양은 극히 드물다[10]. 식도의 평활근종은 대부분 고유근층에서 기원한다. 내시경에서 점막에 고정되지 않고 식도벽에 고정된 양상이며 외연은 매끄러운 원형 또는 타원형을 띄고 있다. 점막근층에 기원한 평활근층은 상대적으로 드물고 고유근층 기원 평활근종에 비하여 납작한 모양이며, 점막에 고정되어 생검을 할 때 미끄러지지 않는다. 저자들의 증례는 비교적 납작한 결절 모양으로 나타났으며 점막에 고정된 상피하 종양의 특징을 가지고 있었다. 종괴 상부의 암종을 고려할 때 점막하 침윤을 의심하여야 하나 EUS 소견이 이전의 보고와 차이가 있었다. 식도편평상피세포암종이 점막하 침윤을 하여 상피하 종양으로 오인된 증례의 보고가 우리나라와 인도에서 있었으나, 두 증례는 모두 초음파 EUS에서 불균질의 저에코 종괴로 나타난 점이 본 증례와 다른 점이다[11,12].
저자들은 현성 흡연자인 중년의 남성에서 발견된 식도 편평형 병변에 대하여 식도 표재성 신생물을 의심하여 협대역 내시경 검사와 EUS를 시행하였다. 협대역 내시경 검사 결과 IPCLs 패턴이 JES 분류 B1형으로 점막암을 시사하였으며, EUS에서는 균질한 저에코의 경계가 분명한 원형 종괴가 점막하층에 국한되어 점막근층 기원의 중간엽 종양으로 판단하였다. 그러나 ESD 후 병리 진단은 점막하 침윤 편평상피세포암종으로 변경되었다. 암의 대부분은 점막에 국한된 식도편평상피세포암종이었으나 항문 측의 일부 암 조직이 플라스크 형태로 점막하층에 침윤하여 종괴를 형성하고 있었다. 식도편평상피세포암종과 점막하층 침윤암의 종괴는 ESD로 일괄 완전 절제하였으나 근치적 치료 실패로 판단하여 추가적인 식도 절제술을 시행하였다. 식도편평상피세포암종에 더불어 상피하 종괴가 존재하는 경우 중간엽 종양의 우연한 병발보다는 암의 점막하 침윤 가능성을 염두에 두고 면밀한 술 전 평가가 필요하다.
Fig. 1.
(A) Endoscopic findings. Endoscopy shows a 2 cm sized superficial flat erythematous area with a geographical pattern. The lesion has a fine granular-irregular surface and the contour looks flat on the proximal side and round-heaped up in the distal direction. (B, C) On iodine staining, a pink color sign is observed on delayed imaging. Two discrete lesions are identified just adjacent to each other. (D) High-definition endoscopy with narrow band imaging shows a definite demarcation line encircling the lesion. The surface microvascular pattern inside the demarcation line reveals prominent and scattered intrapapillary capillary loops (IPCLs). The pattern was compatible with IPCL type B1 of the Japanese Endoscopy Society classification.
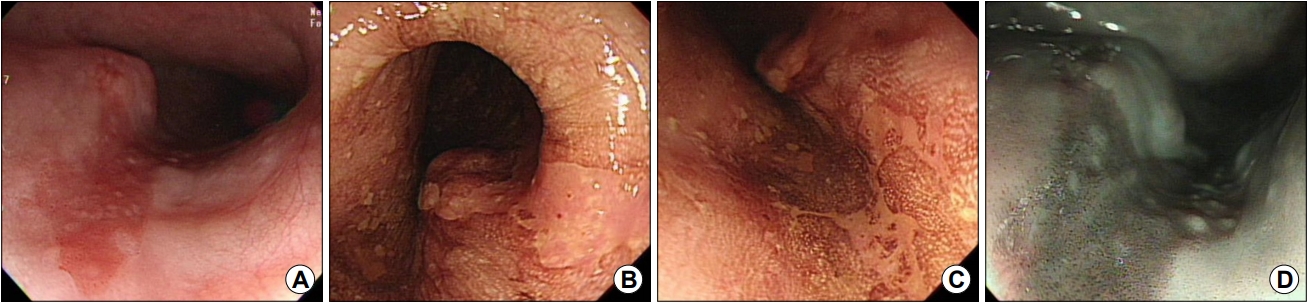
Fig. 2.
(A, B) EUS findings. The layered structure is well maintained for the lesions as well as for the adjacent normal esophageal mucosa (arrows). Epithelial thickening of the cancer areas is negligible. EUS for the distal side of the lesion showed a submucosal hypoechoic mass with a size of 0.9 cm in diameter. The homoge- neously hypoechoic mass has a definite outline and looks separated from the epithelial layer and proper muscle layer. Leiomyoma arising in the muscularis mucosae is the most probable diagnosis.
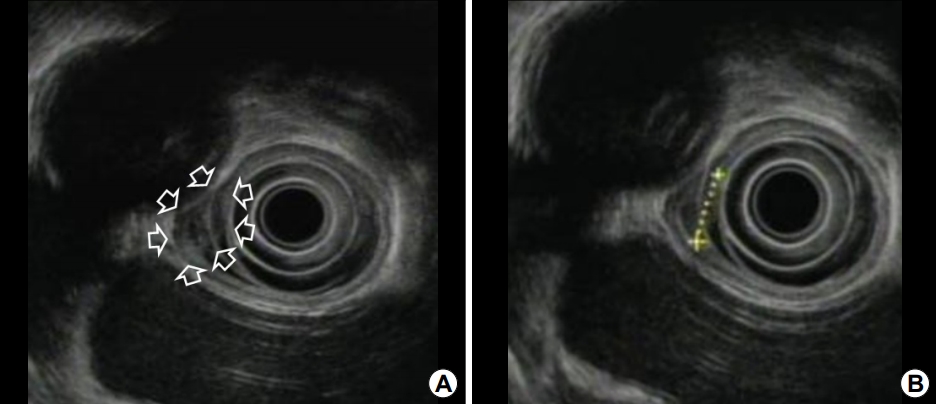
Fig. 3.
Endoscopic submucosal dissection. (A) Mucosal defect remained after endoscopic submucosal dissection for superficial esophageal squamous cell cancer at the at mid-esophagus. (B) The gross specimen after formalin fixation. A discrete and round submucosal mass with white hue is seen on the distal side of the specimen. (C) Inverted view of the resected specimen also shows a protruded submucosal mass at the center.
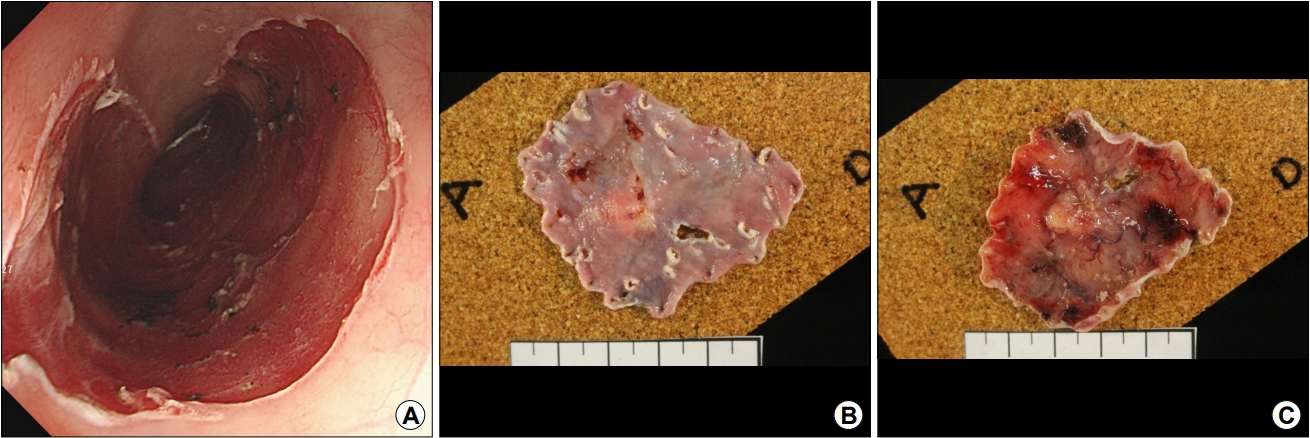
Fig. 4.
Histological findings. (A) Carcinoma in situ at the oral side (H&E, ×200). (B) Moderately differentiated squamous cell carcinoma with extensive submucosal invasion of the distal side (H&E, ×10). (C) The superficial portion of the squamous cell carcinoma is very tiny, but the submucosal expansion is large with a pushing margin rather than an infiltrative margin, which presents a flask-like appearance in the vertical section. Despite a significant expansion of the cancer, the lymphatic-vascular-neural invasion is not present (H&E, ×200).

REFERENCES
1. Kuwano H, Nishimura Y, Oyama T, et al. Guidelines for diagnosis and treatment of carcinoma of the esophagus April 2012 edited by the Japan Esophageal Society. Esophagus 2015;12:1–30.


2. Shimizu Y, Tsukagoshi H, Fujita M, Hosokawa M, Kato M, Asaka M. Long-term outcome after endoscopic mucosal resection in patients with esophageal squamous cell carcinoma invading the muscularis mucosae or deeper. Gastrointest Endosc 2002;56:387–390.


3. Mizumoto T, Hiyama T, Quach DT, et al. Magnifying endoscopy with narrow band imaging in estimating the invasion depth of superficial esophageal squamous cell carcinomas. Digestion 2018;98:249–256.


4. Healthcare Bigdata Hub. Medical practice (examination/surgery, etc.) [Internet]. Health Insurance Review & Assessment Service; 2019 [cited 2019 Feb 1]. Available from: http://opendata.hira.or.kr/op/opc/olapDiagBhvInfo.do.
7. Korean Statistical Information Service. Statistical database: cancer incident cases and incidence rates by site (24 items), sex, age group [Internet]. [cited 2019 Feb 1]. Available from: http://kosis.kr/statHtml/statHtml.do?orgId=117&tblId=DT_117N_A00023&conn_path=I2&language=en.
8. Lee MW, Kim GH, I H, et al. Predicting the invasion depth of esophageal squamous cell carcinoma: comparison of endoscopic ultrasonography and magnifying endoscopy. Scand J Gastroenterol 2014;49:853–861.


9. Oyama T, Inoue H, Arima M, et al. Prediction of the invasion depth of superficial squamous cell carcinoma based on microvessel morphology: magnifying endoscopic classification of the Japan Esophageal Society. Esophagus 2017;14:105–112.



10. Miettinen M, Sarlomo-Rikala M, Sobin LH, Lasota J. Esophageal stromal tumors: a clinicopathologic, immunohistochemical, and molecular genetic study of 17 cases and comparison with esophageal leiomyomas and leiomyosarcomas. Am J Surg Pathol 2000;24:211–222.


-
METRICS

-
- 1 Crossref
- 4,766 View
- 55 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
Esophageal Squamous Cell Carcinoma Presenting as a Subepithelial Tumor2017 September;17(3)
A Case of Duodenal Ganglioneuroma Manifesting as a Subepithelial Tumor2018 December;18(4)






