|
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 19(4); 2019 > Article |
|
Abstract
Addressing the increasing antibiotic resistance, including clarithromycin resistance, which affects Helicobacter pylori (H. pylori) eradication therapy, is a challenge for clinicians. Antibiotic resistance is the main reason for H. pylori eradication failure and the resistance rate for clarithromycin may drastically increase, up to 38.5%, due to 23S ribosomal RNA point mutations. Therefore, the standard triple regimen is no longer suitable as the first-line treatment in most regions. However, there is a growing interest in personalized care for patients. Increased eradication rates of tailored therapy based on antibiotic susceptibility have been reported using nucleic acid-based techniques for clarithromycin resistance with a focus on the first-line eradication therapy of H. pylori infection. Herein, we discuss the eradication therapy for H. pylori, with a diagnostic test and appropriate treatment for clarithromycin resistance.
헬리코박터 파일로리(Helicobacter pylori, H. pylori) 제균은 궤양 치료를 향상시키고 궤양의 재발을 감소시킨다. 또한 위암의 예방 효과와 아울러 기능성 소화불량증의 원인으로서 감염에 대한 검사와 제균을 일차적으로 추천하고 있다[1,2]. 국내의 경우에서도 2018년 1월 이후 H. pylori 제균에 대한 보험급여의 확대로 제균 치료는 앞으로 폭발적으로 늘어날 가능성이 높다. 현재 일차 치료로는 1998년 대한상부위장관·헬리코박터학회에서 제시한 amoxicillin 2.0 g, proton pump inhibitor (PPI) 그리고 clarithromycin 1.0 g이나 metronidazole 1.0 g을 이용한 삼제요법을 사용하고 있다. 하지만 최근 항생제 내성에 의한 제균율 감소 추세에 대한 연구들도 많이 보고되었고, 더욱이 일차 제균 치료 실패 후 이차 제균 치료로 사용되는 PPI, bismuth, tetracycline, metronidazole의 사제요법에 대한 제균율마저도 2000년 초반에 90% 이상이었던 것이 2000년대 중반 이후 점점 저하되고 있는 실정이다[3-5]. 이러한 전반적인 제균율 감소의 원인으로는 항생제 내성, 환자의 나이, 흡연 여부, 숙주 면역의 차이, 기저질환, 순응도 감소 등이 있지만 이 중 항생제 내성이 가장 중요한 인자로 알려져 있다[5-7].
1997년 아시아-태평양 합의 보고서에서 이상적인 제균 치료는 제균율이 intention-to-treat 분석으로 80% 이상, per-protocol 분석으로 90% 이상 되어야 한다고 하였으나[8], 실제 국내에서 근래 보고되는 제균 치료의 제균율은 이에 미치지 못하고 있다. 새로운 항생제의 조합으로 이전보다는 좋은 제균율을 보일 수는 있지만 경우에 따라서는 새로운 항생제의 내성을 일으키는 계기가 된다는 것을 예상하고 있다. 실제로 대만의 경우에서 그 예를 볼 수 있는데[9], 제한적이면서 적절한 항생제 사용이 현재로는 가장 이상적이라 생각하며 이에 일차 제균 요법을 실시하기 전에 제일 문제가 되는 clarithromycin의 내성 검사를 실시하고 이에 따라 적절한 치료 약제를 선택하면 제균율을 90% 이상으로 높일 수 있을 것으로 기대하고 있다. 최근 개정된 고시에 따라 H. pylori 제균 전에 미리 clarithromycin 내성을 판단할 수 있게 되었고, 적절한 항생제를 사용함으로써 항생제 남용을 줄일 수 있으면서 이상적인 제균율에 접근할 수 있는 가능성을 열게 되었다.
Clarithromycin은 macrolide 계열의 항생제로 erythromycin의 6번 hydroxyl기를 methylation 시킨 반합성 항생제이다. 세균의 리보솜(ribosome)에 결합하여 단백질 생성을 억제하게 되는데, 이 계열의 다른 항생제에 비하여 산성 환경에서도 안정성이 높고 흡수율이 높은 장점이 있다. 한편, 제균에 사용하고 있는 항생제들의 각각의 내성률을 보면 2000년 이전에는 metronidazole, clarithromycin, amoxicillin에 대한 내성률이 각각 40.6%, 5.9%, 0%였으나[10,11], 2003년에는 66.2%, 13.8%, 18.5%로 증가하였고[12], 2007~2009년에는 27.6%, 38.5%, 4.8%로 metronidazole, amoxicillin에 대한 내성은 감소하였으나 clarithromycin에 대한 내성률은 꾸준히 증가하는 추세에 있다[13]. 최근 10년 이내에 수행된 연구의 clarithromycin에 대한 내성률(2007∼2009년)이 38.5%로 급격히 증가하였다는 점은 놀라운 일이다. 다만 연구자에 따라 다소 차이는 있으나 clarithromycin 내성은 대체적으로 증가하고 있으며, 2011년 시행된 다기관 연구에서도 clarithromycin 내성률을 26.3%로 보고하였는데[14], 이러한 점을 감안하면 최근 표준 삼제요법 치료 실패의 주요한 원인이 clarithromycin에 대한 내성임을 알 수 있다. 주목할 것은 amoxicillin과 clarithromycin에 모두 내성이 없는 경우에는 표준 삼제요법의 제균율은 95% 내외인 반면, clarithromycin에 내성이 있는 경우에서 제균율은 43∼65% 정도로 보고하고 있어 clarithromycin의 내성이 제균 치료 실패에 가장 큰 영향임을 증명하였다[13,15].
두 가지 이상의 항생제에 내성을 보이는 다약제 내성 H. pylori 균주도 지속적으로 꾸준히 증가하고 있다. 다약제 내성균은 1987년 24%, 1994년 33%, 2003년 47.7%로 증가하였으며[16], 이후 연구에서도 2007∼2009년 40.3%로 증가하였다[13]. 최근의 연구에서도 2011∼2012년 23.4%로 나타났다[17]. 다약제 내성을 보이는 항생제의 조합은 매우 다양한데, 특히 제균 치료의 일차 약제로 사용되고 있는 amoxicillin과 clarithromycin에 동시 내성을 나타낸 균주는 2011년 연구에서 4.0%였다[14]. Clarithromycin과 metronidazole에 함께 내성을 보이는 균주 또한 2013년 연구에서 6.1%로 나타났다[17].
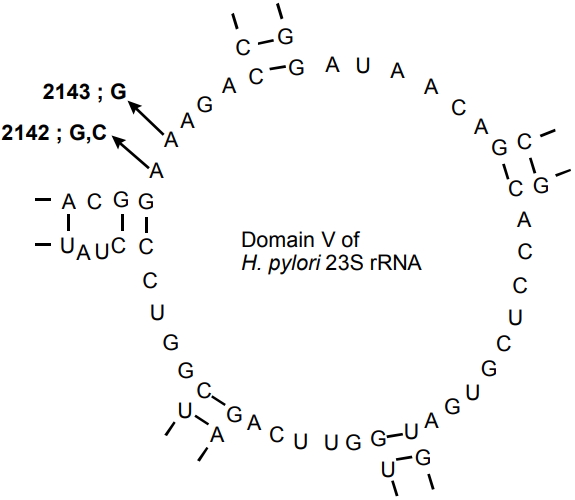
Clarithromycin은 H. pylori에 대하여 사용 가능한 가장 강력한 항생제로 남아 있으며 정균 활성은 23S ribosomal RNA (rRNA) gene에 결합, 작용을 하여 단백질 합성을 방해하는 기전을 가지고 있는 약제이다. 중합효소연쇄반응검사(polymerase chain reaction, PCR) 기반 광범위 연구에 따르면, 23S rRNA의 V 영역에 코드 영역의 점 돌연변이(point mutation)가 세균 내성을 일으키는 것으로 밝혀졌다(Fig. 1) [18]. 이러한 돌연변이는 clarithromycin과 특정 항생제 관련 단백질 합성에 사용되는 ribosomal subunit 사이의 결합을 억제할 수 있다. 또한 H. pylori는 유출 채널(efflux channel)을 통하여 항생제를 세균 밖으로 빠르게 이동시켜 항생제가 리보솜에 결합하는 것을 방해한다[19]. 따라서 표준 삼제요법이나 순차 치료(sequential therapy)에서 처음 사용되는 amoxicillin은 유출 채널을 약화시켜 이후에 투여되는 clarithromycin의 효과를 향상시키고 내성을 억제하게 된다[20,21].
PCR 기반 검사가 보편화되기 전에는 주로 clarithromycin에 대한 내성을 진단하기 위하여 배양 및 디스크 확산법(disk diffusion method), E-test 등의 방법이 이용되어 왔다. 최소 억제 농도(minimal inhibitory concentration)는 항균력을 측정하는 지표로서 항생제 감수성 검사에서 미생물의 번식을 억제할 수 있는 항생제의 최저 농도로 정의한다[16]. 그러나 H. pylori의 항생제에 대한 최소 억제 농도는 보고자에 따라 많은 차이를 보이는데, 지역마다 균주의 차이가 존재하고 균주의 배양하는 조건이 까다로울 뿐 아니라 검사법이 통일되지 않는 점에서 기인한다[22,23]. 정확한 균주의 배양을 위하여 검사 전 적어도 2주간의 PPI 복용 및 4주간의 항생제 복용이 제한되며, 채취한 조직은 가능한 빠르게 처리되어야 한다. 또한 배양검사는 민감도는 73% 이하로 낮다는 단점이 있는 반면 clarithromycin 내성 전반을 평가할 수 있다는 장점이 있다[24,25].
PCR 방법이 H. pylori 감염을 판단하는 검사로서 요양급여가 확대되면서 보편화되었는데, 이로써 검사의 민감도 및 진단의 정확도는 눈부시게 상승하였다. 더욱이 clarithromycin에 대한 내성은 대부분 23S rRNA gene의 2142 혹은 2143 위치의 점 돌연변이에 의하여 일어나는데, PCR 방법을 이용한 검사로 항생제 내성도 예측할 수 있게 되었다. 주로 점 돌연변이의 위치는 주로 염기서열 2142와 2143 위치에 adenine이 guanine으로 치환되는 경우(A2142G, A2143G)이며, 드물게 2142 위치에 adenine이 cytosine으로 치환되는 경우(A2142C)와 그 외에도 A2115G, G2141A, A2142T, T2182C를 보고하고 있다[26,27]. 지역마다 돌연변이의 분포는 다소 차이가 있는데, 미국에서 A2142G, A2143G 변이는 각각 48~53%와 39~45%이면서 A2142C 변이는 0~7%이고, 유럽은 A2142G, A2143G 변이가 각각 23~33%와 44~67%이면서 A2142C 변이는 2~10%로 보고하여 미국과 유럽의 clarithromycin 내성의 주요 변종의 분포는 유사하다[28-30]. 하지만 일본에서는 A2143G의 경우가 90% 이상이면서 A2142C는 발견되지 않았고[31,32], 중국의 연구에서도 비록 적은 수의 연구이지만 A2143G 변이가 거의 100%라고 보고하였다[33]. 홍콩에서는 A2144G 변이 빈도가 높은 것으로 알려져 있고[34], 한국은 2004년 clarithromycin 내성인 10균주 중 7균주에서 A2143G 변이를 보고하였는데[16], 2005년에 실시한 연구에서는 clarithromycin 내성이 20.2%이면서 대부분이 A2142G라고 하여 이전 결과와는 다소 다르게 보고하였다[35]. 그러나 이후 여러 연구에서 대부분의 clarithromycin 내성은 대부분이 A2143G 변이로 확인되었다[36-38]. 이러한 PCR 방법은 82~90% 이상으로 상대적으로 높은 민감도 및 95% 이상의 특이도를 나타내는 우수성이 있는 검사이고[39-41], 더군다나 배양검사에서 제한되는 clarithromycin와 quinolone의 동시 내성을 확인할 수 있는 장점이 있다[42].
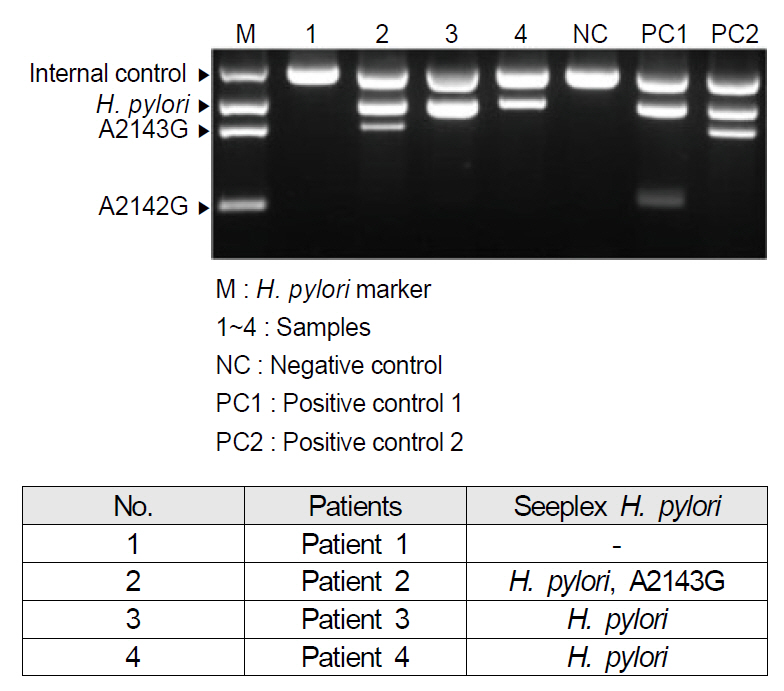
그러나 기대와는 달리 위양성 및 위음성률이 다소 기대에 미치지 못하고 또한 현실적으로 검사의 번거로움과 고가의 장비 그리고 검사 인력을 추가로 필요하게 하여 대형 병원이 아니면 감히 검사를 하기 힘든 실정이었다. 이외에도 MutaREAL H. pylori kit, ClariRes realtime PCR assay, Seeplex ClaR-H. pylori ACE detection system 등이 clarithromycin 내성 진단을 위하여 고안되었으며[43], 특히 최근에 소개된 DPO-based multiplex PCR (Seegene Inc., Seoul, Korea)은 기존의 PCR 검사에 비하여 polydeoxynosine linker로 연결된 길이가 다른 두 개의 primer를 사용하기 때문에 비특이적인 PCR 산물을 생성하지 않아 기존 PCR보다 위양성률을 낮추었다[38,44]. 연구에 따르면 DPO-PCR의 민감도와 특이도는 각각 87.5%, 91.3%였고 양성 예측률 및 음성 예측률, 정확도는 각각 84.0%, 93.3%, 90.0%였다[45]. 또한 규격화되어 검사를 간단하게 하였고 검사비용의 절감을 가져오게 하였다. DPO-PCR에서는 진단뿐만 아니라 clarithromycin 내성도 더불어 파악할 수 있게 설계되어 있는데, clarithromycin 내성의 80% 이상을 차지하여 주요 원인으로 알려진 A2142G와 A2143G 변이를 측정할 수 있게 고안되었다[46,47]. PCR 산물과 ClaR-HP marker를 각각 전기 영동한 후 자외선 투과 조명기에서 증폭된 유전자를 확인함으로써 내성을 예상하게 되는데, 증폭된 DNA 산물에서 621 bp 산물만 관찰되면 H. pylori wild-type으로 감염을 진단하고, 475 bp가 함께 관찰되면 A2143G 변이형, 194 bp가 함께 관찰되면 A2142G 변이형으로 해석할 수 있다(Fig. 2).
Clarithromycin에 대한 높은 수준의 내성인 경우는 H. pylori 감염을 치료하고 억제하는 넓은 의미의 새로운 치료법을 찾아내는 것이 중요하다. Maastricht V/Florence 진료지침에서는 clarithromycin 내성률이 15% 이상으로 높은 지역에서는 bismuth 사제요법이나 동시 치료법을 선택할 것을 추천하고 있는데[49], 최근 우리나라의 clarithromycin 내성이 약 30%라는 보고를 참고한다면[50] clarithromycin을 기본으로 한 기존의 삼제요법을 일차 치료로 유지하기보다는 항생제 감수성 검사 결과를 토대로 한 치료 계획 수립이 필요하다.
최근 국내의 보고에 따르면 제균 전 DPO-PCR 검사를 통하여 clarithromycin 내성에 대한 점 돌연변이를 미리 알고 맞춤제균을 하였을 때, per-protocol 분석 결과 91.0%의 제균 성공률을 보여주었다[51]. 하지만 현재까지 국내에서 clarithromycin 내성이 확인된 환자에서 일차 치료 약제에 대한 표준 가이드라인은 정립되지 않았다. 일반적으로는 제균 전 clarithromycin 내성을 확인한 경우에 선택할 수 있는 약제는 metronidazole을 근간으로 하는 삼제요법을 선택할 수 있으나 동시에 존재할 수 있는 다제 내성 균주, 특히 metronidazole의 내성을 동시에 가지고 있는 경우가 높은 지역에서는 14일 동안의 bismuth를 근간으로 하는 고전적인 사제요법을 일차 제균 요법으로 선택할 수 있다. 그러나 이 요법은 복용법이 복잡할 뿐만 아니라 약제 부작용도 많아서 환자의 순응도가 낮다는 단점이 있고, 일차 제균 치료에 실패하였을 때에 이차 치료 약제를 선정하는 데 어려움이 있다. 국내의 연구에서 clarithromycin 내성이 확인된 일차 치료로 metronidazole 포함 삼제요법은 기존의 bismuth 포함 사제요법에 비하여 제균에서 통계적으로 차이가 없고 부작용 측면에서도 우월한 것으로 보고되었다[52]. 그러나 이에 대해서는 향후 추가적인 대규모 연구가 필요하며 학회 차원에서 어떤 약제의 조합을 사용할 것인가에 대한 구체적인 가이드라인을 제시할 필요가 있겠다.
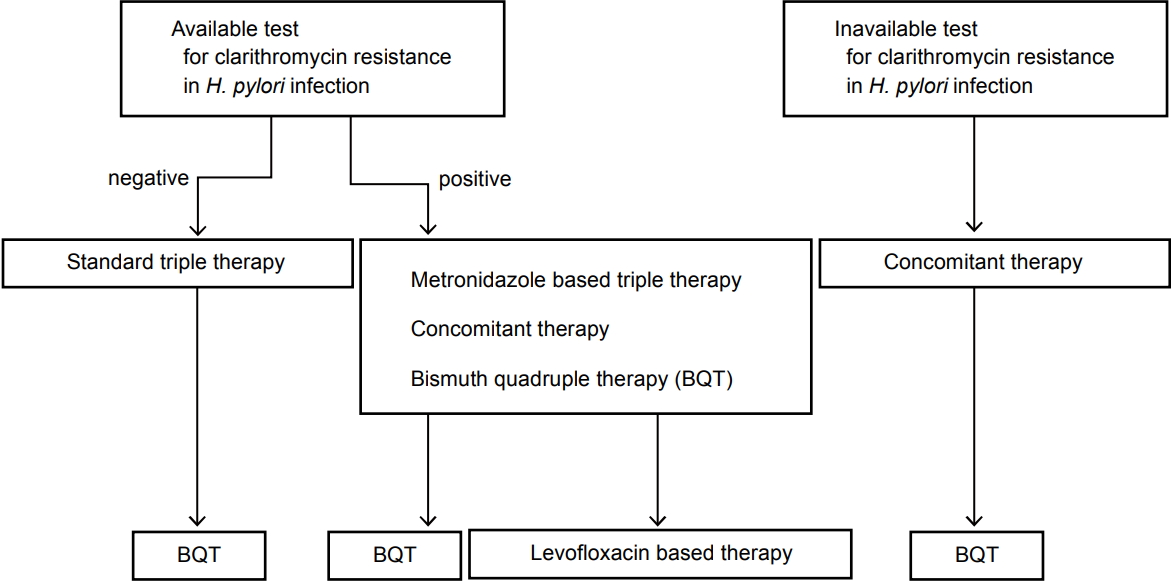
동시 치료는 PPI, amoxicillin, clarithromycin과 metronidazole의 4가지 약제를 동시에 투약하는 방법으로서, Maastricht V/Florence 진료지침 및 Toronto 지침, 미국 소화기학회 가이드라인 등에 따르면 일차 치료로서 우수하고, 특히 clarithromycin 내성률이 높은 지역에서 추천될 만한 치료로 알려져 있어서 고려할 수 있는 치료법이다[53-55]. 일차 치료로 성공적인 제균 치료가 되지 않은 경우 이차 치료로서 bismuth 사제요법 및 levofloxacin 기반의 삼제요법이 고려될 수 있으며, 빠른 시간 내에 levofloxacin 기반의 삼제요법이 삼차 제균 요법으로 국내의 요양급여 고시에 포함되어야 할 것으로 생각된다(Fig. 3) [53-55].
국내에서 H. pylori 균의 제균율이 감소하는 중요한 원인으로 clarithromycin에 내성 증가를 생각할 수 있다. 기존의 배양검사는 까다로운 조건과 연구자마다 다른 결과를 보고하여 임상에 적용하기 어려운 면이 있었고, 반면 PCR 검사는 번거로운 면이 있었다. 최근 DPO-PCR 검사는 여러 번의 검사를 해야할 필요를 줄임으로써 시간과 비용을 단축할 수 있게 되었고, 더욱이 신속 요소분해효소 검사를 통한 DPO-PCR test는 PCR의 불편함도 해결해 주었다. 하지만 이러한 시스템을 통하여 clarithromycin 내성을 완전히 다 파악할 수 있는가에 대한 의문을 가질 수 있고, 어떤 효과적인 약제를 선택해야 하는가에 대한 문제는 여전히 남아 있다. 향후 이런 점들을 보완하여 제균 전 이러한 시스템을 이용하여 적절한 제균 요법을 선택할 수 있게 하여 이상적인 제균율을 이룰 수 있어야 할 것이다.
Fig. 1.
Mutations arising in domain V of H. pylori 23S rRNA. H. pylori, Helicobacter pylori; rRNA, ribosomal RNA.
REFERENCES
1. Stanghellini V, Chan FK, Hasler WL, et al. Gastroduodenal disorders. Gastroenterology 2016;150:1380–1392.


2. Sugano K, Tack J, Kuipers EJ, et al. Kyoto global consensus report on Helicobacter pylori gastritis. Gut 2015;64:1353–1367.



3. Ahn JY, Jung HY. Current status of second-line and third-line therapy for Helicobacter pylori eradication in Korea. Korean J Helicobacter Up Gastrointest Res 2010;10:1–5.
4. Marin AC, McNicholl AG, Gisbert JP. A review of rescue regimens after clarithromycin-containing triple therapy failure (for Helicobacter pylori eradication). Expert Opin Pharmacother 2013;14:843–861.


5. Song M, Ang TL. Second and third line treatment options for Helicobacter pylori eradication. World J Gastroenterol 2014;20:1517–1528.



6. Byun YH, Jo YJ, Kim SC, et al. Clinical factors that predicts successful eradication of Helicobacter pylori. Korean J Gastroenterol 2006;48:172–179.

7. Nam TM, Lee DH, Kang KP, et al. Clinical factors that potentially affect the treatment outcome of Helicobacter pylori eradication therapy with using a standard triple regimen in peptic ulcer patients. Korean J Gastrointest Endosc 2008;36:200–205.
8. Lam SK, Talley NJ. Report of the 1997 Asia Pacific consensus conference on the management of Helicobacter pylori infection. J Gastroenterol Hepatol 1998;13:1–12.


9. Liou JM, Chang CY, Chen MJ, et al. The primary resistance of Helicobacter pylori in Taiwan after the national policy to restrict antibiotic consumption and its relation to virulence factors-a nationwide study. PLoS One 2015;10:e0124199.



10. Eun CS, Han DS, Park JY, et al. Changing pattern of antimicrobial resistance of Helicobacter pylori in Korean patients with peptic ulcer diseases. J Gastroenterol 2003;38:436–441.



11. Bang SY, Han DS, Eun CS, et al. Changing patterns of antibiotic resistance of Helicobacter pylori in patients with peptic ulcer disease. Korean J Gastroenterol 2007;50:356–362.

12. Kim JM, Kim JS, Jung HC, Kim N, Kim YJ, Song IS. Distribution of antibiotic MICs for Helicobacter pylori strains over a 16-year period in patients from Seoul, South Korea. Antimicrob Agents Chemother 2004;48:4843–4847.



13. Hwang TJ, Kim N, Kim HB, et al. Change in antibiotic resistance of Helicobacter pylori strains and the effect of A2143G point mutation of 23S rRNA on the eradication of H. pylori in a single center of Korea. J Clin Gastroenterol 2010;44:536–543.


14. Kim JY, Kim NY, Kim SJ, et al. Regional difference of antibiotic resistance of Helicobacter pylori strains in Korea. Korean J Gastroenterol 2011;57:221–229.


15. Kim N, Kim JM, Kim CH, et al. Institutional difference of antibiotic resistance of Helicobacter pylori strains in Korea. J Clin Gastroenterol 2006;40:683–687.


16. Kim JM, Kim JS, Jung HC, Kim N, Song IS. Antibiotic resistance of Helicobacter pylori isolated from Korean patients in 2003. Korean J Gastroenterol 2004;44:126–135.

17. An B, Moon BS, Kim H, et al. Antibiotic resistance in Helicobacter pylori strains and its effect on H. pylori eradication rates in a single center in Korea. Ann Lab Med 2013;33:415–419.



18. Versalovic J, Shortridge D, Kibler K, et al. Mutations in 23S rRNA are associated with clarithromycin resistance in Helicobacter pylori. Antimicrob Agents Chemother 1996;40:477–480.



19. Webber MA, Piddock LJ. The importance of efflux pumps in bacterial antibiotic resistance. J Antimicrob Chemother 2003;51:9–11.



20. Murakami K, Fujioka T, Okimoto T, Sato R, Kodama M, Nasu M. Drug combinations with amoxycillin reduce selection of clarithromycin resistance during Helicobacter pylori eradication therapy. Int J Antimicrob Agents 2002;19:67–70.


21. So S, Ahn JY, Na HK, et al. Efficacy of ecabet sodium for Helicobacter pylori eradication with sequential therapy. Korean J Helicobacter Up Gastrointest Res 2018;18:180–185.

22. Kim JG, Kim BJ. Antibiotic resistance in Helicobacter pylori infection. Korean J Helicobacter Up Gastrointest Res 2011;11:13–20.

23. Gong EJ, Ahn JY. Antimicrobial resistance of Helicobacter pylori isolates in Korea. Korean J Helicobacter Up Gastrointest Res 2018;18:82–88.

24. Zullo A, Hassan C, Lorenzetti R, Winn S, Morini S. A clinical practice viewpoint: to culture or not to culture Helicobacter pylori? Dig Liver Dis 2003;35:357–361.


25. McNulty CA, Lasseter G, Shaw I, et al. Is Helicobacter pylori antibiotic resistance surveillance needed and how can it be delivered? Aliment Pharmacol Ther 2012;35:1221–1230.


26. Mégraud F. H pylori antibiotic resistance: prevalence, importance, and advances in testing. Gut 2004;53:1374–1384.



27. Hultén K, Gibreel A, Sköld O, Engstrand L. Macrolide resistance in Helicobacter pylori : mechanism and stability in strains from clarithromycin-treated patients. Antimicrob Agents Chemother 1997;41:2550–2553.



28. Stone GG, Shortridge D, Versalovic J, et al. A PCR-oligonucleotide ligation assay to determine the prevalence of 23S rRNA gene mutations in clarithromycin-resistant Helicobacter pylori. Antimicrob Agents Chemother 1997;41:712–714.



29. Alarcón T, Domingo D, Prieto N, López-Brea M. Clarithromycin resistance stability in Helicobacter pylori : influence of the MIC and type of mutation in the 23S rRNA. J Antimicrob Chemother 2000;46:613–616.



30. van Doorn LJ, Glupczynski Y, Kusters JG, et al. Accurate prediction of macrolide resistance in Helicobacter pylori by a PCR line probe assay for detection of mutations in the 23S rRNA gene: multicenter validation study. Antimicrob Agents Chemother 2001;45:1500–1504.



31. Maeda S, Yoshida H, Matsunaga H, et al. Detection of clarithromycin-resistant Helicobacter pylori strains by a preferential homoduplex formation assay. J Clin Microbiol 2000;38:210–214.




32. Kato S, Fujimura S, Udagawa H, et al. Antibiotic resistance of Helicobacter pylori strains in Japanese children. J Clin Microbiol 2002;40:649–653.



33. Pan ZJ, Su WW, Tytgat GN, Dankert J, van der Ende A. Assessment of clarithromycin-resistant Helicobacter pylori among patients in Shanghai and Guangzhou, China, by primer-mismatch PCR. J Clin Microbiol 2002;40:259–261.



34. Wang WH, Wong BC, Mukhopadhyay AK, et al. High prevalence of Helicobacter pylori infection with dual resistance to metronidazole and clarithromycin in Hong Kong. Aliment Pharmacol Ther 2000;14:901–910.


35. Lee JH, Shin JH, Roe IH, et al. Impact of clarithromycin resistance on eradication of Helicobacter pylori in infected adults. Antimicrob Agents Chemother 2005;49:1600–1603.



36. An B, Moon BS, Kim H, et al. Antibiotic resistance in Helicobacter pylori strains and its effect on H. pylori eradication rates in a single center in Korea. Ann Lab Med 2013;33:415–419.



37. Lee JH, Sung IK, Kim JH, et al. Impact of clarithromycin resistance on the outcome of standard triple Helicobacter pylori eradication therapy. Korean J Helicobacter Up Gastrointest Res 2010;10:14–20.
38. Chung WC, Jung SH, Oh JH, et al. Dual-priming oligonucleotide-based multiplex PCR using tissue samples in rapid urease test in the detection of Helicobacter pylori infection. World J Gastroenterol 2014;20:6547–6553.



39. Schabereiter-Gurtner C, Hirschl AM, Dragosics B, et al. Novel real-time PCR assay for detection of Helicobacter pylori infection and simultaneous clarithromycin susceptibility testing of stool and biopsy specimens. J Clin Microbiol 2004;42:4512–4518.



40. Agudo S, Alarcón T, Urruzuno P, Martínez MJ, López-Brea M. Detection of Helicobacter pylori and clarithromycin resistance in gastric biopsies of pediatric patients by using a commercially available real-time polymerase chain reaction after NucliSens semiautomated DNA extraction. Diagn Microbiol Infect Dis 2010;67:213–219.


41. Vécsei A, Innerhofer A, Binder C, et al. Stool polymerase chain reaction for Helicobacter pylori detection and clarithromycin susceptibility testing in children. Clin Gastroenterol Hepatol 2010;8:309–312.


42. Malfertheiner P, Megraud F, O'Morain CA, et al. Management of Helicobacter pylori infection--the Maastricht IV/Florence consensus report. Gut 2012;61:646–664.


43. Smith SM, O'Morain C, McNamara D. Antimicrobial susceptibility testing for Helicobacter pylori in times of increasing antibiotic resistance. World J Gastroenterol 2014;20:9912–9921.



44. Shin SY, Kwon KC, Park JW, Kim JM, Shin SY, Koo SH. Evaluation of the Seeplex® Meningitis ACE Detection kit for the detection of 12 common bacterial and viral pathogens of acute meningitis. Ann Lab Med 2012;32:44–49.


45. Lee HJ, Kim JI, Cheung DY, et al. Eradication of Helicobacter pylori according to 23S ribosomal RNA point mutations associated with clarithromycin resistance. J Infect Dis 2013;208:1123–1130.



46. Kargar M, Ghorbani-Dalini S, Doosti A, Souod N. Real-time PCR for Helicobacter pylori quantification and detection of clarithromycin resistance in gastric tissue from patients with gastrointestinal disorders. Res Microbiol 2012;163:109–113.


47. Kuo CH, Kuo FC, Hu HM, et al. The optimal first-line therapy of Helicobacter pylori infection in year 2012. Gastroenterol Res Pract 2012;2012:168361.




48. Chung WC, Jeon EJ, Oh JH, et al. Dual-priming oligonucleotide-based multiplex PCR using tissue samples from the rapid urease test kit for the detection of Helicobacter pylori in bleeding peptic ulcers. Dig Liver Dis 2016;48:899–903.


49. Malfertheiner P, Megraud F, O'Morain CA, et al. Management of Helicobacter pylori infection-the Maastricht V/Florence consensus report. Gut 2017;66:6–30.


50. Hwang TJ, Kim N, Kim HB, et al. Change in antibiotic resistance of Helicobacter pylori strains and the effect of A2143G point mutation of 23S rRNA on the eradication of H. pylori in a single center of Korea. J Clin Gastroenterol 2010;44:536–543.


51. Jung YD, Kim YJ, Chung WC, et al. A pilot study of Helicobacter pylori eradication using a polymerase chain reaction-based test for clarithromycin resistance. Korean J Helicobacter Up Gastrointest Res 2017;17:200–207.

52. Seo MW, Jeong YJ, Kim JS, Kim BW. Optimal first-line eradication regimens for Helicobacter pylori infection in patients with clarithromycin resistance: a pilot study. Korean J Helicobacter Up Gastrointest Res 2018;18:242–246.

53. Fallone CA, Chiba N, van Zanten SV, et al. The Toronto consensus for the treatment of Helicobacter pylori infection in adults. Gastroenterology 2016;151:51–69; e14.


-
METRICS

-
- 6 Crossref
- 10,080 View
- 417 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
What Is the Optimal Drug Regimen for Helicobacter pylori Eradication Therapy?2024 June;24(2)
Vonoprazan-based Dual and Triple Therapy for Helicobacter pylori Eradication2023 September;23(3)
Antibiotic Resistance and Helicobacter pylori Eradication Therapy2023 September;23(3)