 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 21(3); 2021 > Article |
|

See editorial "Can the Combination of Famotidine and Prokinetics Have Additional Effects on Gastric Acid Suppression?" in Volume 21 on page 171.
Abstract
Background/Aims
Studies in healthy humans have reported that the addition of mosapride to acid suppressants resulted in higher intragastric pH than acid suppressant administration alone. We investigated the effect of the addition of mosapride to famotidine on the intragastric pH and gastric emptying rate (GER) in rats.
Materials and Methods
Sixty male Wistar rats were used in this study. Experimental groups were divided into control, famotidine-only, mosapride-only, and famotidine with mosapride (combination). The first experiment was performed in non-stressed rats. Mosapride was administered by oral gavage 1 hour before the meal, and famotidine was administered just before the meal. The rats were provided with food for 30 minutes. The intragastric pH was measured under isoflurane anesthesia, and the GER was measured after harvesting the stomach. In the stress experiment, rats were exposed to 1-hour restraint stress immediately after mosapride administration and subjected to the same process as in the experiment with the non-stressed rats.
Results
The famotidine-only and combination groups showed significantly higher gastric pH levels than the control group in non-stressed (P<0.01 and P<0.001, respectively) and stressed (P<0.001 and P<0.001, respectively) rats. The combination group also showed significantly higher intragastric pH levels than the famotidine-only group in non-stressed (P<0.01) and stressed (P<0.05) rats. Additionally, combination groups showed a significantly higher GER than the famotidine-only group in non-stressed (P<0.001) and stressed (P<0.01) rats.
위산은 위염, 소화성 궤양, 위식도역류질환 등에서 증상을 일으키는 주요 인자이며 이 질환들의 치료 방법으로 위산 분비를 억제시키는 히스타민-2 수용체(H2) 길항제나 양성자펌프억제제가 사용된다. H2 길항제는 외래에서 가장 많이 처방되는 약제들 중 하나로 시메티딘, 라니티딘, 파모티딘, 라퓨티딘, 니자티딘이 사용되고 있다[1]. 양성자펌프억제제가 충분한 위산 억제효과가 나타날 때까지 3~5일의 투여 기간이 필요한 반면 H2 길항제는 투여 1시간 직후로 위내 pH를 상승시킬 수 있으나[2,3] 내성 발현으로 위산 억제효과가 감소하는 단점이 있다[4,5]. 또한 복용 후 위 내에서 바로 위산을 중화시켜 즉각 증상을 개선시키는 제산제에 비해 H2 길항제나 양성자펌프억제제는 소장에서 흡수되어 혈중 이동을 통해 벽세포까지 도달해 작용하므로 효과 발현 시작까지 일정 시간이 필요하다. 그러므로 위배출을 촉진시키면 위산 억제제의 효과가 빨리 나타날 수 있는데, 라푸티딘이나 오메프라졸에 선택적 5HT4 작용제인 모사프리드를 병합 투여하면 단독 투여에 비해 위내 pH가 더 빨리 상승하는 것이 건강인 대상 연구에서 증명되었다[6,7]. 모사프리드는 선택적 5-HT4 작용제로 장신경계 내의 신호전달을 촉진시켜 위장관운 동성을 증가시킨다[8-11]. 그러므로 위산 억제제와 모사프리드를 병합하였을 때 위산 억제효과가 빨리 발현되는 것은 위배출 촉진에 의해 위산 억제제가 십이지장으로 빨리 이동되어 흡수가 빨라지는 기전으로 설명된다[6,7]. 그러나 파모티딘에서는 위장관 운동 촉진제 병합요법의 효과가 확인되지 않았고, 스트레스로 인한 위배출 감소상황에서도 병합요법이 효과가 있는지 연구된 바 없다[12]. 본 연구에서는 흰쥐에서 파모티딘과 모사프리드의 병합 투여가 정상 상태와 스트레스 상태에서 위내 pH 변화와 위배출에 미치는 영향을 평가하였다.
체중이 약 260 g의 수컷 8주령 Wistar rats (Sam Taco, Osan, Korea) 60마리를 사용하였으며, 모든 실험동물은 개별 케이지에서 사육하였다. 실험동물을 1주일간의 적응 기간 후 실험군에 따라 분류하고 비스트레스 및 스트레스 조건에 따라 2회에 걸쳐 실험을 진행하였다. 파모티딘과 모사프리드(Daewoong Pharmaceutical, Seoul, Korea)는 각각 3 mg/kg의 용량으로 투여되도록 식수에 녹여 금속으로 된 주입기를 통해 경구 주입하였다. 실험에 관련된 모든 사항은 원광대학교 실험동물 윤리위원회의 기준에 맞추어 진행하였다(IRB No. WKU20-14).
실험군은 식수만 처리한 대조군(n=6), 파모티딘만 투여한 군(F단독군; 파모티딘, 3 mg/kg, n=6), 모사프리드만 투여한 군(M단독군; 모사프리드, 3 mg/kg, n=6), 모사프리드와 파모티딘을 같이 투여한 군(MF병합군; 파모티딘 3 mg/kg+모사프리드 3 mg/kg, n=6)으로 분류하였다. 실험동물은 실험 하루 전날 금식을 시켰으며 금식 동안 물은 자유롭게 섭취하도록 하였다. 실험 당일 모사프리드 경구 투여 후 1시간을 기다렸다가 파모티딘을 경구 투여하였고, 파모티딘 투여 직후부터 30분간 사료를 제공하여 자유롭게 먹게 하고 섭식량을 측정하였다. 30분간의 사료 섭식 후 즉시 이소플루란 흡입마취하에서 복부를 4 cm 정도 절개하여 위를 노출시키고 위식도접합부와 위십이지장접합부를 실로 묶어 위내 음식물이 이동하는 것을 방지하였다. 노출된 위의 전정부, 체부에 각각 최소한의 크기로 절개한 후 절개공을 통해 pH 측정기(PH-220S; Lutron Electronic Enterprise Co. Ltd., Taipei, Taiwan)를 삽입하여 위내 음식물의 pH를 측정하였다. 위내 pH 측정 후 실험동물을 횡격막 절단을 통해 희생시키고 위를 적출하여 증류수를 담은 비커 안에서 절개하여 위내에 있는 사료를 분리하였다. 분리된 위내 사료는 거름종이를 통해 거른 후 이틀간 건조하여 무게를 측정하였다. 위배출능은 (섭식량-위에 남아있는 양)/섭식량×100으로 계산하였다[13]. 마취시간 및 측정시간은 모든 군에 동일하게 적용하였으며 모든 수술은 한 사람의 시술자에 의해 진행되었다(Fig. 1).
실험군은 비스트레스 실험과 동일하게 대조군, F단독군, M단독군, MF병합군으로 분류하였고 스트레스 실험의 변동성을 고려하여 각 군당 9마리의 동물을 배정하였다. 구속 스트레스는 기존 연구[13]와 같이 공기가 잘 통하는 반원통형 아크릴 튜브에 쥐를 넣고 고정판으로 막아 움직이지 못하게 하였다. 본 실험에서는 스트레스 노출시간을 단축하기 위해 튜브를 45° 기울여 스트레스 강도가 높아지도록 변형하였다. 실험 당일 먼저 모사프리드를 경구 투여하고 구속 스트레스를 1시간 동안 가하였고, 이후 파모티딘을 투여 직후 30분간 사료를 제공하였다. 이후의 과정은 비스트레스 실험과정과 동일하게 진행하였다(Fig. 1).
통계 분석을 위해 SPSS Windows version 22.0 (IBM, New York, NY, USA) 또는 R (version 4.0.1)을 사용하였다. 모든 실험 종료 후 섭식량이 1 g 미만이었던 비스트레스 M단독군 1마리와 스트레스 대조군 1마리의 이상값(outlier)을 제외한 58마리의 자료를 통계 분석하였다. 모든 자료의 분석은 정규분포와 등분산검정 후 이에 따라 ANOVA와 LSD post-hoc test 또는 Kruskal Wallis H Test 후 post hoc test를 통해 결과를 분석하였으며 P<0.05인 경우 유의한 것으로 판단하였다. 본문과 그림의 결과는 평균±표준 오차로 표기하였다.
30분간 섭식 후 측정한 위내 pH는 전반적으로 기저부보다 전정부가 더 낮은 경향을 보였다. 전정부의 경우 파모티딘이 포함된 F단독군(4.29±0.15)과 MF병합군(5.30±0.14)은 대조군(3.76±0.13)이나 M단독군(3.46±0.09)에 비해 pH가 유의하게 높았다. 기저부의 경우 파모티딘이 포함된 F단독군(5.27±0.09)과 MF병합군(5.70±0.11) 역시 대조군(4.54±0.10)이나 M단독군(4.62±0.33)에 비해 pH는 높았으나 MF병합군에서만 통계적 유의성을 보였다. 파모티딘이 포함된 군끼리의 비교에서는 MF병합군이 F단독군에 비해 높은 pH 값을 보였으나 전정부의 경우만 통계적 유의성을 보였다(Fig. 2A). 위배출능을 비교해본 결과 F단독군(23.53±2.17%)은 대조군(22.13±2.41%)과 차이가 없었으며, 모사프리드가 포함된 M단독군(35.75±1.56%)과 MF병합군(38.44±3.00%)에서는 대조군 또는 F단독군에 비해 유의하게 위배출능이 촉진된 것을 관찰하였다. 그러나 모사프리드가 포함된 군끼리 비교한 경우 M단독군과 MF병합군 사이에서 위배출능의 유의한 차이는 없었다(Fig. 2B).
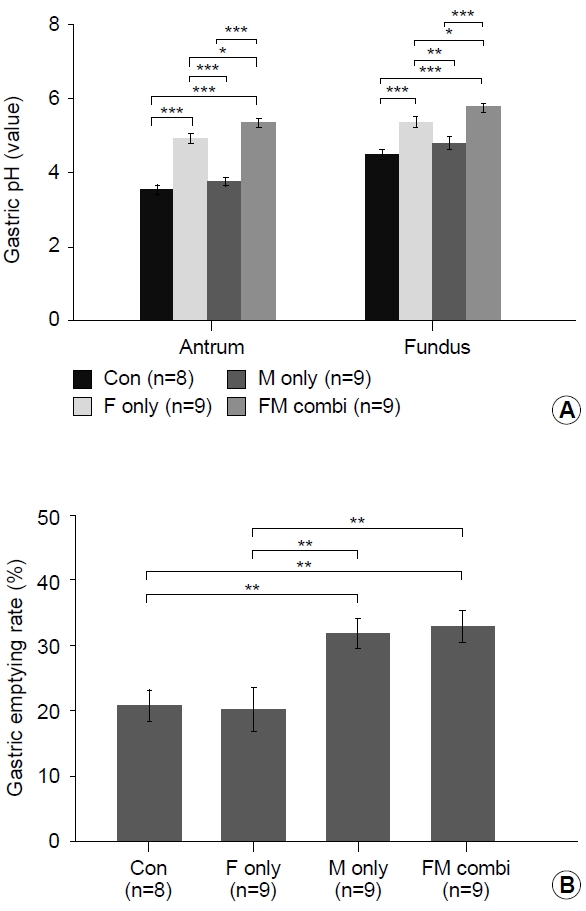
구속 스트레스에 노출된 동물에서도 비스트레스군과 유사하게 위내 pH가 기저부보다 전정부가 더 낮았고, 모사프리드 단독 투여는 pH에 영향을 주지 못하였다. 전정부와 기저부 모두 파모티딘이 포함된 F단독군(전정부 5.01±0.12, 기저부 5.45±0.14)과 MF병합군(전정부 5.43±0.13, 기저부 5.85±0.11)이 대조군(전정부 3.59±0.15, 기저부 4.57±0.13)과 M단독군(전정부 3.82±0.12, 기저부 4.88±0.18)에 비해 유의하게 pH가 높았다. 파모티딘이 포함된 군끼리 비교한 경우 MF병합군이 F단독군보다 높은 pH 값을 보였으며, 이러한 차이는 전정부와 기저부에서 모두 유의하게 관찰되었다(Fig. 3A). 위배출능은 M단독군(31.83±2.30%)과 MF 병합군(33.08±2.50%)이 대조군(20.72±2.42%)과 F단독군(20.18±3.37%)에 비해 유의하게 증가하여 비스트레스 실험과 동일한 결과를 보였다(Fig. 3B). 그러나 스트레스 대조군과 비스트레스 대조군 간 위배출능의 통계적 차이는 관찰되지 않았다.
흰쥐를 이용한 본 연구에서 파모티딘에 모사프리드를 병합한 경우 위내 pH가 더 높아지고 위배출능이 증가하는 것을 확인하였다. 기존 인간 대상 연구에서 라푸티딘이나 오메프라졸에 모사프리드를 병합 투여하면 위내 pH를 더 빨리 높인다는 보고가 있었으나 모두 정상인을 대상으로 한 연구였다[6,7]. 두 연구에서 첫 4시간 동안 평균 위내 pH가 모사프리드 병합군이 라푸티딘이나 오메프라졸을 단독으로 투여한 군에 비해 높았으나 시간별 비교에서는 3~4시간째 유의한 차이를 보였다.
본 연구의 비스트레스 실험에서 파모티딘은 대조군이나 모사프리드 단독군에 비해 기저부와 전정부에서 위내 pH를 상승시켰으며, 기존 연구와 유사하게 파모티딘에 모사프리드를 병합한 경우 파모티딘 단독 투여군보다 유의하게 위내 pH를 상승시켰다. 파모티딘은 제2세대 H2 수용체 길항제로 식사에 의해 자극되는 위산 분비를 효과적으로 저해한다[14]. 단회 경구 투여시 혈중 Cmax는 1.9~3.7시간 후에 도달하고 이는 음식물 섭취에 영향을 받지 않는다[14]. 경구 투여시 생체이용률(bioavailability)은 낮은 지용성 때문에 약 40~49%로 낮고 이는 투여되는 용량에 의존하지 않는다[14]. 파모티딘은 라푸티딘과 비교해 혈중 농도 상승은 느리지만 pH가 상승하는 시간은 비슷해 투여 후 1시간 내에 pH가 상승하기 시작한다[15]. 이것은 라푸티딘이 혈중 농도가 최고점에 도달한 후 감소되면서 위내 pH가 더 올라가는 지연 효과가 있기 때문이다. 이와 달리 파모티딘은 혈중 농도와 pH 상승이 비례하고 지연 효과가 없기 때문에 모사프리드를 병합한 경우 pH를 빠르게 상승시키는 효과가 더 명확할 것으로 생각된다[15].
본 연구의 장점은 파모티딘과 가스모틴의 병합요법시 위산 분비뿐만 아니라 위배출에 대한 영향을 같이 평가하였다는 점이다. 또한 정상 조건과 함께 스트레스 하에서도 가스모틴을 병합하면 위산 억제 증가와 위배출 증가효과가 모두 나타남을 확인할 수 있었다. 위배출 감소와 연관증상들은 기능성 소화불량이나 스트레스와 같은 상황에서 흔히 관찰되는데 위산 억제제 자체도 위배출능을 감소시킬 수 있다. 인간을 대상으로 한 연구에서 라니티딘, 파모티딘, 오메프라졸 같은 위산 분비 억제제는 식후 위배출을 감소시키고 전정부 운동성을 증가시켰다[16]. 국내에서 시행된 임상 연구에서도 위식도역류질환 환자에서 양성자 펌프억제제 사용 후 위배출 감소가 발생하는 것을 확인하였고, 모사프리드 병합 투여에 의해 위배출 감소 및 연관증상이 개선된다고 보고하였다[17]. 위산 분비가 증가되는 경우도 위배출이 감소할 수 있고 이때는 위산 억제제가 위배출능을 회복시는 효과가 있다. Keto 등[15]은 일반 쥐에서는 파모티딘이 위배출에 영향을 주지 못하였으나 pentagastrin 투여로 위산 분비가 자극되고 위배출이 감소한 상태에서는 파모티딘 투여로 위배출이 호전되는 것을 보고하였다. 모사프리드는 일반 쥐나 pentagastrin 자극 쥐 모두에서 위배출을 증가시켰다. 그러나 pentastrin으로 유발된 위 팽창에 대한 통증 과민성은 파모티딘 투여로만 개선되었고 모사프리는 영향을 주지 못하였다[15].
스트레스는 위장관운동성에 영향을 주는데 위배출은 감소시키고 대장 운동은 증가시켜 소화불량, 상복부 팽만, 통증이나 무른변, 급박변을 유발할 수 있다[18]. Nakade 등[13]은 Sprague-Dawley 쥐에 구속 스트레스를 가하면 위배출이 감소하는 것을 확인하였고 이는 중추 CRF2 수용체와 말초 교감신경계의 활성화를 통해 일어나는 것을 증명하였다. 그러나 선행 연구와는 다르게 본 실험에서는 스트레스군에서 비스트레스군에 비해 위배출이 감소하는 경향을 보이기는 하였지만 각 군의 F단독군과 대조군끼리 비교하였을 때 통계적으로 유의하지 않았다.
본 연구는 인간과 다른 특성을 보이는 동물실험이라는 근본적 한계를 고려하여 결과를 해석해야 한다. 본 실험에서 흰쥐의 위내 pH는 기저부보다 전정부에서 더 낮게 측정이 되었고 스트레스 실험에서 병합요법에 의한 위산 억제효과가 전정부에서 더 민감하게 관찰되었다. 이는 설치류 위의 해부학적 특성에 의한 것으로 사람의 위에서는 위산을 분비하는 벽세포가 체부에 주로 분포하고 있는 반면 쥐의 위에서는 분비샘이 분포하는 위치가 인간과 다르기 때문이다[19]. 쥐의 위는 육안적으로 인간의 위와 비슷하지만 인간의 기저부에 해당하는 부위가 얇은막으로 이루어진 nonglandular forestomach이며 이 부위는 편평 상피로 덮어져 있고 위산 분비샘이 없다. 육안적으로 인간의 위에서 체부와 전정부에 해당하는 부분이 근육층을 모두 포함하는 glandular corpus이며, 이 부분을 다시 전정부와 기저부로 구분한다[20]. 이번 실험에서 glandular corpus 중 기저부보다 원위부 전정부에서 더 낮은 pH가 측정되었기 때문에 향후 쥐를 이용한 위산 분비 평가 실험에서는 전정부를 기준으로 측정해야 할 것으로 생각된다.
본 연구의 제한점으로 이전 연구에서 관찰된 파모티딘에 의한 위배출 억제나 구속 스트레스에 의한 위배출 감소가 재현되지 않은 점을 들 수 있다. 이전 보고와 달리 본 연구에서 파모티딘이 위배출을 감소시키지 않았던 것은 단회 투여한 실험이었기 때문으로 생각된다. 또 위배출 결과가 Nakade 등[13]의 실험과 다른 결과를 보인 이유도 실험 설계의 차이를 들 수 있는데, 기존 실험에서는 같은 양의 먹이를 섭취하게 한 후 스트레스를 가했으나, 본 실험에서는 스트레스를 먼저 가하고 이후 자유롭게 먹게 하였기 때문에 기존 실험과 다른 조건이었다. 즉 스트레스가 식사 전에 가해지느냐 후에 가해지느냐에 따라 위 배출에 미치는 영향이 다르다고 추정할 수 있다.
H2 수용체 길항제 중에서 니자티딘은 아세틸콜린에스테라아제 활성을 억제시켜 아세틸콜린의 농도를 높이기 때문에 위운동성을 증가시키고 위배출능이 감소된 기능성소화불량증 환자에서 위배출과 연관증상을 개선시킨다[1,21,22]. 위산 억제제에 위장관운동 촉진 기능을 추가하면 위산 분비 억제에 더 효과적이라는 본 연구 결과를 고려할 때 니자티딘에 추가적으로 모사프리드와 같은 위장관운동 촉진제를 병합하면 그 효과가 극대화될 가능성을 추정해 볼 수 있는데 향후 이에 대한 탐색적 실험이 필요하다.
결론적으로, 기존 연구와 본 연구의 결과를 종합해보면 파모티딘에 모사프리드를 병합한 경우 위산 분비 억제효과 강화와 동시에 위배출 항진효과도 기대할 수 있으며, 특히 임상에서 흔히 경험하는 스트레스가 동반된 상황에서 이러한 병합요법이 유용하리라 생각된다.
Fig. 1.
Protocol for measuring intragastric pH and gastric emptying rate. In the non-stress experiment, rats wait without special manipulation for 1 hour after administration of mosapride. In the stress experiment, restraint stress is applied during this 1-hour period (n=6/group in non-stress experiment, n=9/group in stress experiment). Con, control group; F only, famotidine only group; M only, mosapride only group; FM combi, famotidine-mosapride combination group.
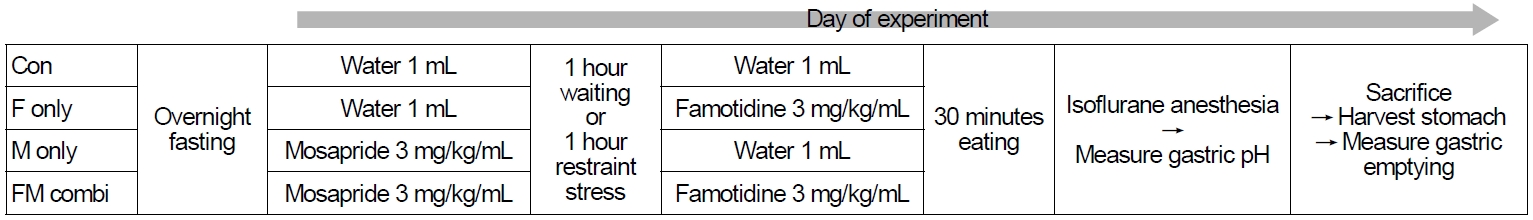
Fig. 2.
Comparison of intragastric pH and (B) gastric emptying rate in the non-stress study. (A) Intragastric pH after 30 minutes of feeding in two gastric segments. Famotidine-only and combination groups show significantly higher pH in the gastric antrum than the control and mosapride-only groups. Combination group shows significantly higher pH in the antrum than the famotidine-only group. Combination group shows a significantly higher pH in the fundus than the control and mosapride-only groups. (B) Gastric emptying rate in each group. Mosapride-only and combination groups show increased gastric emptying rate compared with the control and famotidine-only groups. Data are expressed as mean±standard error. Denotes the post hoc significance between groups (*P<0.05; **P<0.01; ***P<0.001). Con, control group; F only, famotidine only group; M only, mosapride only group; FM combi, famotidine-mosapride combination group.
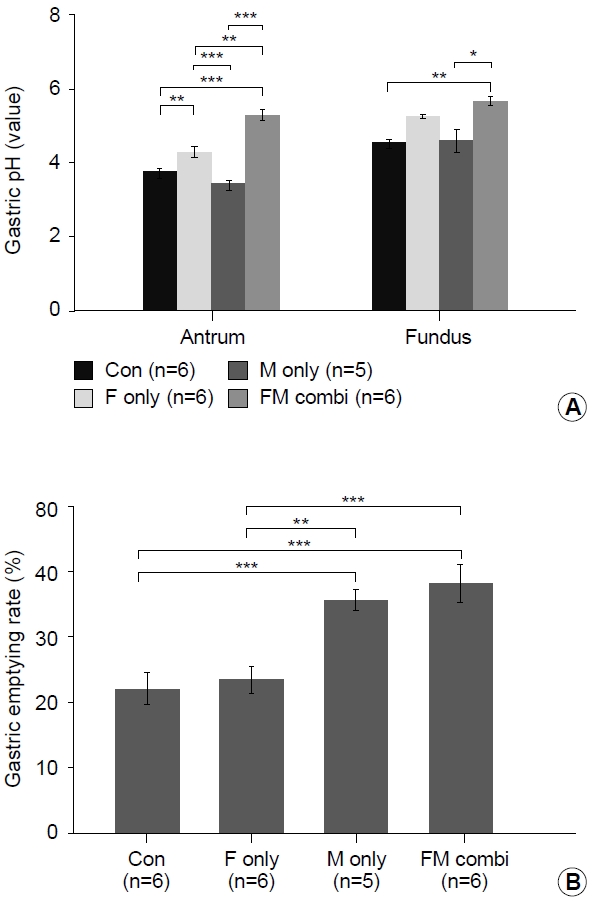
Fig. 3.
Comparison of intragastric pH and (B) gastric emptying rate in the stress study. (A) Intragastric pH after 30 minutes of feeding in two gastric segments. Famotidine-only and combination groups show significantly higher pH in the gastric antrum and fundus than the control and mosapride-only groups. Combination group shows a significantly higher pH in the antrum and fundus than the famotidine-only group. (B) Gastric emptying rate in each group. Mosapride-only and combination groups show increased gastric emptying rate compared with the control and famotidine-only groups. Data are expressed as mean±standard error. Denotes the post hoc significance between groups (*P<0.05; **P<0.01; ***P<0.001). Con, control group; F only, famotidine only group; M only, mosapride only group; FM combi, famotidine-mosapride combination group.
REFERENCES
1. Shim YK, Kim N. The effect of H2 receptor antagonist in acid inhibition and its clinical efficacy. Korean J Gastroenterol 2017;70:4-12.


2. Lubach JW, Chen JZ, Hau J, et al. Investigation of the rat model for preclinical evaluation of pH-dependent oral absorption in humans. Mol Pharm 2013;10:3997-4004.


3. Ikawa K, Shimatani T, Hayato S, Morikawa N, Tazuma S. Pharmacokinetic and pharmacodynamic properties of lafutidine after postprandial oral administration in healthy subjects: comparison with famotidine. Biol Pharm Bull 2007;30:1003-1006.


4. Sachs G, Shin JM, Munson K, Scott DR. Gastric acid-dependent diseases: a twentieth-century revolution. Dig Dis Sci 2014;59:1358-1369.



5. James LP, Kearns GL. Pharmacokinetics and pharmacodynamics of famotidine in paediatric patients. Clin Pharmacokinet 1996;31:103-110.


6. Iida H, Inamori M, Nozaki Y, et al. Early effects of oral administration of lafutidine with mosapride compared with lafutidine alone on intragastric pH values. BMC Gastroenterol 2009;9:52.




7. Iida H, Inamori M, Fujii T, et al. Early effect of oral administration of omeprazole with mosapride as compared with those of omeprazole alone on the intragastric pH. BMC Gastroenterol 2012;12:25.




8. Hongo M, Harasawa S, Mine T, et al. Large-scale randomized clinical study on functional dyspepsia treatment with mosapride or teprenone: Japan mosapride mega-study (JMMS). J Gastroenterol Hepatol 2012;27:62-68.


9. Cho YK, Choi MG, Han HW, et al. The effect of mosapride on esophageal motility and bolus transit in asymptomatic volunteers. J Clin Gastroenterol 2006;40:286-292.


10. Ida Y, Hosoe N, Imaeda H, et al. Effects of the oral administration of mosapride citrate on capsule endoscopy completion rate. Gut Live 2012;6:339-343.


11. Liu Z, Sakakibara R, Odaka T, et al. Mosapride citrate, a novel 5-HT4 agonist and partial 5-HT3 antagonist, ameliorates constipation in parkinsonian patients. Mov Disord 2005;20:680-686.


12. Tache Y, Bonaz B. Corticotropin-releasing factor receptors and stress-related alterations of gut motor function. J Clin Invest 2007;117:33-40.



13. Nakade Y, Tsuchida D, Fukuda H, Iwa M, Pappas TN, Takahashi T. Restraint stress delays solid gastric emptying via a central CRF and peripheral sympathetic neuron in rats. Am J Physiol Regul Integr Comp Physiol 2005;288:R427-R432.


14. Echizen H, Ishizaki T. Clinical pharmacokinetics of famotidine. Clin Pharmacokinet 1991;21:178-194.


15. Keto Y, Hirata T, Takemoto Y, Yamano M, Yokoyama T. Influence of gastric acid on gastric emptying and gastric distension-induced pain response in rats--effects of famotidine and mosapride. Neurogastroenterol Motil 2012;24:147-53, e88.


16. Parkman HP, Urbain JL, Knight LC, et al. Effect of gastric acid suppressants on human gastric motility. Gut 1998;42:243-250.



17. Lim HC, Kim JH, Youn YH, Lee EH, Lee BK, Park H. Effects of the addition of mosapride to gastroesophageal reflux disease patients on proton pump inhibitor: a prospective randomized, double-blind study. J Neurogastroenterol Motil 2013;19:495-502.




18. Ye Y, Wang XR, Zheng Y, et al. Choosing an animal model for the study of functional dyspepsia. Can J Gastroenterol Hepatol 2018;2018:1531958.




19. Sáenz JB, Mills JC. Acid and the basis for cellular plasticity and reprogramming in gastric repair and cancer. Nat Rev Gastroenterol Hepatol 2018;15:257-273.




20. Treuting PM, Arends MJ, Dintzis SM. Upper gastrointestinal tract. Treuting PM, Dintzis SM, Montine KS. In: Comparative anatomy and histology: a mouse, rat, and human atlas 2nd ed. London: Elsevier; 2018;191-211.
- TOOLS
-
METRICS

-
- 4 Crossref
- 4,388 View
- 77 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res






