 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 23(1); 2023 > Article |
|
Abstract
Indefinite-for-neoplasia is an expression used to describe lesions in which carcinoma or dysplasia cannot be clearly and conclusively established via biopsy. Gastric indefinite-for-neoplasia may represent a reactive change secondary to inflammation in some patients; however, some lesions are eventually diagnosed as dysplasia or carcinoma. Follow-up endoscopic biopsy is commonly performed in patients with gastric indefinite-for-neoplasia lesions. Nonetheless, patients may undergo resection based on a high index of clinical suspicion for dysplasia or carcinoma based on endoscopic findings. Accurate target biopsies of the lesion and effective communication with pathologists are required to improve diagnostic accuracy and avoid unnecessary re-examinations. It is important to establish endoscopic findings useful in differentiating lesions that require resection. In this review, we describe the approach for the management of indefinite-for-neoplasia lesions detected on gastric mucosal biopsy and the characteristics of lesions that require resection.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝(gastric indefinite for neoplasia)ņØĆ ļ│æļ”¼ ņ¦äļŗ©ņŚÉņä£ ņóģņ¢æņØĖņ¦Ć ņĢäļŗīņ¦Ć ļ¬ģĒÖĢĒĢśĻ▓ī Ļ▓░ļĪĀ ļé┤ļ”¼ĻĖ░ ņ¢┤ļĀżņÜ┤ Ļ▓ĮņÜ░ņŚÉ ņé¼ņÜ®ĒĢśļŖö ņÜ®ņ¢┤ņØ┤ļŗż. ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļ¬ģĒÖĢĒĢśĻ▓ī ņØ┤ĒśĢņä▒ņ”Ø(dysplasia)ņØ┤ļéś ņĢö(carcinoma)ņ£╝ļĪ£ ņ¦äļŗ©ļÉśņ¦Ć ņĢŖņĢśņ£╝ļéś ļ╣äņĀĢĒśĢ ņäĖĒż(atypical cell)ļéś ņ×¼ņāØ ļ╣äņĀĢĒśĢ(regenerative atypism)ņØ┤ Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ļĪ£ Ļ░£ņĀĢļÉ£ Vienna ļČäļźśņŚÉņä£ ļ▓öņŻ╝ 2ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö ļ│æļ│ĆņØ┤ļŗż[1]. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØĆ ļ│æļ”¼ Ļ▓░Ļ│╝ņ¦ĆņŚÉ ņ×¼ņāØ ņØ┤ĒśĢņä▒(regenerative atypia), ļ╣äņĀĢĒśĢ ņāüĒö╝(atypical epithelia), ļ╣äņĀĢĒśĢ ņāś(atypical gland) Ēś╣ņØĆ ļ╣äņĀĢĒśĢņäĖĒż(atypical cell)ļĪ£ ļ│┤Ļ│ĀļÉ£ļŗż. ņØ┤ļ¤░ Ēæ£ĒśäļōżņØĆ ņĀĢņāüņŚÉņä£ ļ▓Śņ¢┤ļéśņ¦Ćļ¦ī ņŗĀņāØļ¼╝(neoplasia)ņØä ņÖäņĀäĒ׳ ņ¦äļŗ©ĒĢśņ¦ĆļŖö ļ¬╗ĒĢśļŖö ņäĖĒż ĻĄ¼ņĪ░ņØś ņÖ£Ļ│Ī(cellular architectural distortion) Ēś╣ņØĆ ĒĢĄņØś ņØ┤ĒśĢņä▒(nuclear atypia)ņØä ļéśĒāĆļé┤ļŖö Ļ▓ĮņÜ░ņŚÉ ņé¼ņÜ®ĒĢśļŖö ļ│æļ”¼ĒĢÖ ņÜ®ņ¢┤ļōżņØ┤ļŗż[2,3]. ņĀĢĒÖĢĒĢ£ ņ¦äļŗ©ņŚÉ ĒĢäņÜöĒĢ£ ņĪ░ņ¦ü Ēæ£ļ│ĖņØś ņ¦łĻ│╝ ņ¢æņØ┤ ļČĆņĪ▒ĒĢśĻ│Ā ņĢöņØś Ļ░ĆļŖźņä▒ņØ┤ ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ĻČīĻ│ĀĒĢśĻ▓ī ļÉ£ļŗż[4,5]. ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś ņĄ£ņóģ ņĪ░ņ¦ü Ļ▓░Ļ│╝ļŖö ņĀĢņāü ņĪ░ņ¦ü Ēś╣ņØĆ ņŚ╝ņ”ØļČĆĒä░ ņØ┤ĒśĢņä▒ņ”Ø, ņ£äņĢöĻ╣īņ¦Ć ļŗżņ¢æĒĢśĻ▓ī ĒÖĢņØĖļÉĀ ņłś ņ׳ņ£╝ļ®░ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ņŚÉņä£ ņØ┤ĒśĢņä▒ņ”ØņØĆ 5~17%, ņ£äņĢöņØĆ 21~37%Ļ╣īņ¦Ć ļ│┤Ļ│ĀļÉśņŚłļŗż[6-10]. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØĆ ņĀäņĢö ļ│æļ│Ć Ēś╣ņØĆ ņØ┤ļ»Ė ņĢģņä▒ņØ╝ Ļ░ĆļŖźņä▒ņØ┤ ņ׳ļŖö ļ│æļ│ĆņØ┤ļéś ņĢäņ¦ü ņØ┤ņŚÉ ļīĆĒĢ£ ņ¦äļŻī ņ¦Ćņ╣©ņØ┤ ņŚåĻ│Ā ņČöņĀü ļé┤ņŗ£Ļ▓ĮņØś ņŗ£ĻĖ░ļéś Ēܤņłś ļśÉļŖö ļ░öļĪ£ ņĀłņĀ£ļź╝ ĒĢśļŖö ĻĖ░ņżĆņØ┤ ņŚåļŖö ņāüĒā£ņØ┤ļŗż. ļ│Ė ņóģņäżņŚÉņä£ļŖö ņ£äņĀÉļ¦ē ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØ┤ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī ņ×äņāüņĀüņ£╝ļĪ£ Ļ░ĆļŖźĒĢ£ ņĀæĻĘ╝ņŚÉ ļīĆĒĢ┤ ņ░ĖĻ│Āļ¼ĖĒŚīļōżņØä ĒåĄĒĢ┤ Ļ▓ĆĒåĀĒĢ┤ļ│┤Ļ│Ā ņØ┤ņŚÉ ļīĆĒĢ£ ĒĢ┤Ļ▓░ņ▒ģņØä ņĀ£ņŗ£ĒĢ┤ ļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ņ£äļé┤ņŗ£Ļ▓Į ņĪ░ņ¦ü ņāØĻ▓Ć Ļ▓░Ļ│╝ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØ┤ļØ╝ļŖö Ļ▓āņØĆ ņ£äņןĻ┤Ć ņāüĒö╝ ņóģņ¢æ(gastrointestinal epithelial neoplasia)ņŚÉ ļīĆĒĢ£ Ļ░£ņĀĢļÉ£ Vienna ļČäļźśņŚÉņä£ ļ▓öņŻ╝ 2ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö ļ│æļ│Ćņ£╝ļĪ£ ņĢöņóģņØ┤ļéś ņØ┤ĒśĢņä▒ņ”Øņ£╝ļĪ£ ļ¬ģĒÖĢĒ׳ ĒīÉņĀĢļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ļź╝ ņ¦Ćņ╣ŁĒĢ£ļŗż[1]. ņØ┤ ņ¦äļŗ©ņØĆ ņŚ╝ņ”Øņ£╝ļĪ£ ņØĖĒĢ£ ņĪ░ņ¦üņØś ļ░śņØæņä▒ ļ│ĆĒÖö(reactive change)ņŚÉņä£ļČĆĒä░ ņØ┤ĒśĢņä▒ņØ┤ļéś ņĢöņóģĻ╣īņ¦Ć ļ¬ģĒÖĢĒ׳ ĻĄ¼ļČäļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ļĪ£ ļ╣äņĀĢĒśĢņĀüņØĖ ņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ćļ¦ī ĻĘĖ ļČĆņ£äĻ░Ć ĻĄŁņåīņĀüņØ┤Ļ▒░ļéś ņĀĢĒÖĢĒĢ£ ņ¦äļŗ©ņØä ĒĢśĻĖ░ņŚÉ ņĪ░ņ¦üņØś ņ¢æņØ┤ ļ¦Äņ¦Ć ņĢŖĻ▒░ļéś ņĪ░ņ¦üņØś ņ¦łņØ┤ ļ¢©ņ¢┤ņĀĖ ņ¦äļŗ©ņØä ļé┤ļ”┤ ņłś ņŚåļŖö Ļ▓ĮņÜ░ņŚÉ ņé¼ņÜ®ĒĢ£ļŗż[2,3]. ĒŖ╣Ē׳ ĒĢ£ĻĄŁĻ│╝ Ļ░ÖņØĆ ņ£äņĢö ņ£Āļ│æļźĀņØ┤ ļåÆņØĆ ņ¦ĆņŚŁņŚÉņä£ ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØ┤ ļ│┤Ļ│ĀļÉśļ®┤ ņØśņé¼ļéś ĒÖśņ×ÉļōżņØ┤ Ļ▓ĮĻ░üņŗ¼ņØä Ļ░¢Ļ▓ī ļÉśĻ│Ā ļīĆļČĆļČä ļé┤ņŗ£Ļ▓Į ņ×¼Ļ▓ĆņØä ĒåĄĒĢ£ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśĻ▓ī ļÉ£ļŗż.
ņ£ä ņāüĒö╝ ņóģņ¢æņŚÉ ļīĆĒĢ£ ņāØĻ▓Ć Ļ▓Ėņ×Éļź╝ ņØ┤ņÜ®ĒĢ£ ļé┤ņŗ£Ļ▓Į ņĪ░ņ¦ü Ļ▓Ćņé¼ļŖö Ļ░äļŗ©ĒĢśļ®┤ņä£ ļ╣äĻĄÉņĀü ņĀĢĒÖĢĒĢ£ Ļ▓░Ļ│╝ļź╝ ņ¢╗ņØä ņłś ņ׳ļŖö ņ▓½ ļ▓łņ¦Ė ņ¦äļŗ© ļÅäĻĄ¼ņØ┤ļéś ņāØĻ▓Ć ņĪ░ņ¦üĻ│╝ ņĀäņ▓┤ ļ│æļ│ĆņŚÉ ļīĆĒĢ£ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ņłĀ Ēøä ņĄ£ņóģ ņĪ░ņ¦ü Ļ░äņØś ļČłņØ╝ņ╣śĻ░Ć ļŗżņ¢æĒĢśĻ▓ī ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[11-13]. ņŚ░ĻĄ¼ļōżņØĆ Ļ▓Ėņ×É ņāØĻ▓ĆņŚÉņä£ ņĀĆļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”ØņØ┤ņŚłņ£╝ļéś ņĄ£ņóģ ņĀłņĀ£ ņĪ░ņ¦üņØ┤ ņ£äņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉśļŖö Ļ▓ĮņÜ░ļŖö 6.1~8.7%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā ņØ┤ ņżæ ļ»ĖļČäĒÖöĒśĢ ņ£äņĢöļÅä 1.4%, ņĀÉļ¦ēĒĢś ņ╣©ļ▓ö ņĢöļÅä 0.1%Ļ╣īņ¦Ć ņ׳ņŚłļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż[11-13].
ļé┤ņŗ£Ļ▓Į Ļ▓Ėņ×É ņĪ░ņ¦ü Ļ▓Ćņé¼ņÖĆ ņĄ£ņóģ ņĀłņĀ£ Ēæ£ļ│Ė Ļ░äņØś ļČłņØ╝ņ╣śņØś ņØ┤ņ£ĀļŖö ņ▓½ ļ▓łņ¦ĖļĪ£ ļ│æļ│ĆņŚÉ ļīĆĒĢ£ ņĀĢĒÖĢĒĢ£ Ēæ£ņĀü ņāØĻ▓ĆņØ┤ ņĢł ļÉśņŚłņØä Ļ░ĆļŖźņä▒ņØ┤ ņ׳ļŗż. ļæÉ ļ▓łņ¦ĖļĪ£ ņĀĢĒÖĢĒĢ£ Ēæ£ņĀü ņāØĻ▓ĆņØ┤ ļÉśņŚłļŗż ĒĢ┤ļÅä ļ│æļ│ĆņØ┤ ļäłļ¼┤ ņ×æņĢäņä£ Ēś╣ņØĆ ĒĢĄņŗ¼ ļ│æļ│ĆņØ┤ ņ┤łņĀÉ ĒśĢĒā£ļĪ£ ņØ╝ļČĆļ¦ī ņ׳ņØä Ļ░ĆļŖźņä▒ņØ┤ ņ׳Ļ│Ā ņśłļĪ£ Ļ│Āļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”ØņØ┤ļéś ņĪ░ĻĖ░ ņ£äņĢöņØ┤ ņĀĆļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”Ø ļ░░Ļ▓ĮņŚÉ ņØ╝ļČĆļ¦ī ņĪ┤ņ×¼ĒĢĀ ņłś ņ׳ļŗż[14]. ņäĖ ļ▓łņ¦ĖļĪ£ ņ£ä ļ░śņ¦ĆņäĖĒżņĢöņóģņ▓śļ¤╝ ņāüĒö╝ĒĢśļĪ£ ĒŹ╝ņ¦ĆļŖö ļ│æļ│ĆņØś Ļ▓ĮņÜ░ Ēæ£ņĀü ņāØĻ▓ĆņØ┤ ņ¢┤ļĀżņÜĖ ņłś ņ׳ļŗż[15]. ļäż ļ▓łņ¦ĖļĪ£ ņāØĻ▓Ć Ļ▓Ėņ×ÉņØś Ēü¼ĻĖ░ļéś ņāØĻ▓Ć ĒܤņłśņŚÉ ļö░ļØ╝ ņ¦äļŗ©ņ£©ņØ┤ ļŗżļź╝ ņłś ņ׳ļŗż[16,17].
ņ£ä ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ņ¦äļŗ©ļÉ£ ļ│æļ│ĆļōżņØĆ ņĄ£ņóģņĀüņ£╝ļĪ£ ĒŖ╣ļ│äĒĢ£ ņØ┤ņāü ņåīĻ▓¼ņØ┤ ņĢäļŗłņŚłĻ▒░ļéś(non-neoplasm) ņØ┤ĒśĢņä▒ņ”Ø, ņĪ░ĻĖ░ ņ£äņĢö ĻĘĖļ”¼Ļ│Ā ļō£ļ¼╝Ļ▓ī ņ¦äĒ¢ēņä▒ ņ£äņĢöĻ╣īņ¦Ć ņ¦äļŗ©ļÉĀ ņłś ņ׳ļŗż. ņ£äĻČżņ¢æ ņŚŁņŗ£ ņŚ╝ņ”ØņØ┤ ņŗ¼ĒĢĀ ļĢī ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļ╣äņĀäĒśĢņäĖĒż ĒśĢĒā£Ļ░Ć Ļ┤Ćņ░░ļÉśņ¢┤ ņĢģņä▒ņ£╝ļĪ£ Ēś╝ļÅłņØä ņżä ņłś ņ׳ļŗż. ņ£ä ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ņ¦äļŗ©ļÉ£ ļ│æļ│ĆļōżņØś ņĄ£ņóģ Ļ▓░Ļ│╝ļź╝ ļ╣äĻĄÉĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ׳ņŚłĻ│Ā ņØ┤ļōż ņżæ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ņłĀņØä ņŗ£Ē¢ēĒĢ£ ĒÖśņ×Éļōżļ¦ī ļīĆņāüņ£╝ļĪ£ ĒĢ£ ņŚ░ĻĄ¼ļōżņØĆ ņØ┤ĒśĢņä▒ņ”ØņØ┤ļéś ņ£äņĢöņØś ļ╣äņ£©ņØ┤ ļäłļ¼┤ ļåÆņĢä ņĀ£ņÖĖļź╝ ĒĢśļ®┤ ņ┤Ø 5ĒÄĖņØś ņŚ░ĻĄ¼ļōżņØ┤ ņ׳ņŚłļŗż. ņØ┤ļōż ņŚ░ĻĄ¼ļōżņØĆ ļ¬©ļæÉ ņĄ£ņóģ ņ¦äļŗ© Ļ▓░Ļ│╝ļĪ£ ņØ┤ĒśĢņä▒ņ”Ø, ņĢö ĻĘĖļ”¼Ļ│Ā ņóģņ¢æņØ┤ ņĢäļŗī Ļ▓ĮņÜ░ļĪ£ ļéśļłäņ¢┤ ļČäņäØĒĢśņśĆļŗż(Table 1) [6-10]. ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņ£╝ļéś ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ļéś ņłśņłĀļĪ£ ņĢö Ēś╣ņØĆ ņØ┤ĒśĢņä▒ņ”Øņ£╝ļĪ£ ņĄ£ņóģ ņ¦äļŗ©ļÉ£ Ļ░üĻ░üņØś ņ”ØļĪĆ ņé¼ņ¦äļōżņØä ņ▓©ļČĆĒĢśņśĆļŗż(Fig. 1,-4).
ņ£äņØś ņŚ╝ņ”Øņ£╝ļĪ£ ņØĖĒĢ┤ ņäĖĒżņØś ļ¬©ņ¢æņØ┤ ļ│ĆĒĢĀ ņłś ņ׳ņ£╝ļ®░, ņØ┤ļ¤░ ļ│æļ│ĆļōżņØä ņĪ░ņ¦ü Ļ▓Ćņé¼ĒĢśņśĆņØä ļĢī ļ│æļ”¼ĒĢÖņĀüņ£╝ļĪ£ ļ╣äņĀäĒśĢņäĖĒż(atypia)ļĪ£ ļ│┤Ļ│ĀļÉĀ ņłś ņ׳Ļ│Ā ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś 52~73% ņĀĢļÅäĻ╣īņ¦Ć non-neoplasmņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢśĻ│Ā ņ׳ļŗż[6-10]. ņØ┤ļ¤░ ļ│æļ│ĆļōżņØĆ ļīĆļČĆļČä ņČöņĀü ļé┤ņŗ£Ļ▓ĮņŚÉņä£ ņ×ÉņŚ░ ĒśĖņĀäļÉśĻ▒░ļéś ņĢĮņĀ£, ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ Ļ░ÉņŚ╝ ļō▒ņØś ņøÉņØĖņØĖņ×Éļź╝ ņĀ£Ļ▒░ĒĢśļ®┤ ĒśĖņĀäļÉśļŖö Ļ▓ĮĻ│╝ļź╝ ļ│┤ņØ┤ļéś ļé┤ņŗ£Ļ▓Į ņĀłņĀ£Ļ╣īņ¦Ć ņŗ£Ē¢ēĒĢśņŚ¼ ņĪ░ņ¦üĒĢÖņĀüņ£╝ļĪ£ ņØīņä▒ņ£╝ļĪ£ ĒīÉļ¬ģļÉśļŖö Ļ▓ĮņÜ░ļōżņØ┤ ļō£ļ¼╝Ļ▓ī ņ׳ļŗż.
ņ£äĻČżņ¢æņØś ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļ╣äņĀäĒśĢņäĖĒżļĪ£ ļ│┤Ļ│ĀļÉśļŖö Ļ▓ĮņÜ░ ņĢģņä▒ņØś Ļ░ĆļŖźņä▒ņØ┤ ņ׳ņ¢┤ ņŻ╝ņØśļź╝ ņÜöĒĢśĻ▓ī ļÉ£ļŗż. ņØ┤ļ¤░ Ļ▓ĮņÜ░ ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØ┤ ņżæņÜöĒĢ£ļŹ░ ņĀäĒåĄņĀüņ£╝ļĪ£ ĻČżņ¢æ ņŻ╝ļ│Ć ņŻ╝ļ”äņØś ĒśĢĒā£ņÖĆ ļ│ĆņŚ░ņØś ĒśĢĒā£, ĻČżņ¢æ ļ░öļŗźņØś ĒśĢĒā£ļĪ£ ņ¢æņä▒ ņ£äĻČżņ¢æĻ│╝ ņĢģņä▒ ņ£äĻČżņ¢æņØä Ļ░Éļ│äĒĢĀ ņłś ņ׳ļŗż. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØä ĒåĄĒĢ£ ņĢģņä▒ ņśłņĖĪļÅäļź╝ ņ£ĄĻĖ░ļÉ£ ļ│ĆņŚ░ņØĆ 94%, ļČłĻĘ£ņ╣ÖĒĢ£ ļ│ĆņŚ░ņØĆ 91%, ņ¦ĆņĀĆļČäĒĢ£ ĻČżņ¢æ ļ░öļŗźņØĆ 79%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż. ņØ┤ ņŚ░ĻĄ¼ņŚÉņä£ ņ▓½ ļ▓łņ¦Ė ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼Ļ│╝ ņĪ░ņ¦üĻ▓Ćņé¼ Ļ▓░Ļ│╝Ļ░Ć ļ¬©ļæÉ ņ¢æņä▒ ņ£äĻČżņ¢æņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī ņĄ£ņóģņĀüņ£╝ļĪ£ ņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ Ļ▓ĮņÜ░ļŖö ņŚåņŚłņ£╝ļéś ņ▓½ ļ▓łņ¦Ė ļé┤ņŗ£Ļ▓ĮņŚÉņä£ ņ¢æņä▒ ņ£äĻČżņ¢æņØś ņåīĻ▓¼ņØä ļ│┤ņśĆļŹś ĒÖśņ×Éļōż ņżæ 2.5%ļŖö ņĄ£ņóģņĀüņ£╝ļĪ£ ņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż[18]. ļŗżļźĖ ĻĄŁļé┤ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļČłĻĘ£ņ╣ÖĒĢ£ ļ│ĆņŚ░Ļ│╝ ņ£ĄĻĖ░ļÉ£ ļ│ĆņŚ░ņØ┤ ņĢģņä▒ ņ£äĻČżņ¢æņØś ņØśļ»Ė ņ׳ļŖö ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØ┤ņŚłĻ│Ā ņĢģņä▒ ņ£äĻČżņ¢æņØś 37.5%ņØ┤ ņĄ£ņ┤ł ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļ¬©ĒśĖĒĢ£ ļ│æļ”¼ ņ¦äļŗ©ņ£╝ļĪ£ ņČöņĀü ļé┤ņŗ£Ļ▓ĮņØ┤ ĒĢäņÜöĒ¢łļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż[19].
ņĄ£ņ┤ł ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ņ¦äļŗ©ļÉ£ ļ│æļ│ĆļōżņØś ņĄ£ņóģ Ļ▓░Ļ│╝ļź╝ ĒÖĢņØĖĒĢ£ ņŚ░ĻĄ¼ļōżņŚÉņä£ ņØ┤ĒśĢņä▒ņ”Øņ£╝ļĪ£ ņ¦äļŗ©ļÉśļŖö ļ╣äņ£©ņØĆ 5.0~17.9%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż(Table 1) [6-10]. ņØ┤ ņżæ ļæÉ ņŚ░ĻĄ¼ņŚÉņä£ Ļ│Āļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”ØĻ╣īņ¦Ć ļČäļźśĒĢśņśĆĻ│Ā, ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØ┤ Ļ│Āļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”Øņ£╝ļĪ£ ļéśņśżļŖö Ļ▓ĮņÜ░ļŖö Ļ░üĻ░ü 6.5%, 4.6%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż[8,10]. ņ£äņäĀņóģ Ēś╣ņØĆ ņØ┤ĒśĢņä▒ņ”ØņØś ļ│æļ”¼ĒĢÖņĀü ņĀĢņØśļŖö ņ£äņØś ņäĀ ĻĄ¼ņĪ░(glandular structure)ļź╝ ņ£Āņ¦ĆĒĢśļ®┤ņä£ Ļ┤Ćņāü(tubular) Ēś╣ņØĆ ņ£ĀļæÉņāü(papillary) ĻĄ¼ņĪ░ļź╝ Ļ░Ćņ¦ĆĻ│Ā ņ׳ļŖö ņäĀņóģņä▒ ņāüĒö╝ņäĖĒż(adenomatous epithelium)ņØś ņ”ØņŗØņ£╝ļĪ£ ņĀĢņØśĒĢĀ ņłś ņ׳ļŗż[20]. ĒĢśņ¦Ćļ¦ī ņ£äņØś ņØ┤ĒśĢņä▒ņ”Ø Ēś╣ņØĆ ņĪ░ĻĖ░ ņ£äņĢöņŚÉ ļīĆĒĢ£ ņä£ĻĄ¼ņÖĆ ņØ╝ļ│ĖņØś ļ│æļ”¼ĒĢÖņĀü ļČäļźś ņ▓┤Ļ│äĻ░Ć ļŗ¼ļØ╝ Ēś╝ņäĀņØ┤ ņ׳ņ£╝ļ®░, Ļ│Āļō▒ĻĖē ņØ┤ĒśĢņä▒ņ”ØņØś Ļ▓ĮņÜ░ ņØ╝ļ│ĖņØś ļČäļźśļź╝ ļö░ļź┤ļ®┤ ņ£äņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉĀ ņłś ņ׳ņ¢┤ ĒĢ┤ņäØņŚÉ ņŻ╝ņØśļź╝ ņÜöĒĢ£ļŗż.
ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ņ¦äļŗ©ļÉ£ ļ│æļ│ĆļōżņØĆ ņĄ£ņóģņĀüņ£╝ļĪ£ 21.8~37.6%Ļ╣īņ¦Ć ņ£äņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż[6-10]. ļīĆļČĆļČä T1aņØś ļ│æĻĖ░ņśĆņ£╝ļéś ņłśņłĀ Ēś╣ņØĆ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ Ēøä T1b ņØ┤ņāüņØś ļ│æĻĖ░ļź╝ 7.3% (9/123)ļĪ£ ļ│┤Ļ│ĀĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ņ׳ņŚłļŗż[8]. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļ»ĖļČäĒÖöĒśĢ ņ£äņĢöņØä 2.2% (10/461)ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż[7]. ņĢöņ£╝ļĪ£ ņ¦äļŗ© ļÉśļŖö ņ£äĒŚśņØĖņ×Éļź╝ ļČäņäØĒĢśņśĆņØä ļĢī 1 cm ņØ┤ņāüņØś Ēü¼ĻĖ░ļŖö ļ¬©ļōĀ ņŚ░ĻĄ¼ļōżņŚÉņä£ ņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉśļŖö ņ£äĒŚśņØĖņ×ÉņśĆĻ│Ā ĻĘĖ ņÖĖ ņĀÉļ¦ē ļ░£ņĀü, ĒĢ©ļ¬░, ņ×Éļ░£ ņČ£ĒśłņØ┤ ļæÉ Ļ░Ćņ¦Ć ņŚ░ĻĄ¼ņŚÉņä£ Ļ│ĄĒåĄļÉśļŖö ņ£äĒŚśņØĖņ×ÉņśĆļŗż[6,7,9,10]. ļ│æļ”¼ĒĢÖņĀüņ£╝ļĪ£ļŖö ļ│æļ”¼ ņåīĻ▓¼ļ¦ī ļČäņäØĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ĻĄ¼ņĪ░ņĀü ļ╣äņĀĢĒśĢ(structural atypia)ņØ┤ ĒĢĄņØś ļ╣äņĀĢĒśĢ(nuclear atypia)ļ│┤ļŗż ņĢģņä▒ņØä ņ¦äļŗ©ĒĢśļŖö ļŹ░ ļŹö ļÅäņøĆņØ┤ ļÉśņ¢┤ ĻĄ¼ņĪ░ņĀü ļ╣äņĀĢĒśĢņØś ļ▓öņ£ä(structural atypia area, SAA)Ļ░Ć 25% ņØ┤ņāüņØ┤ ņĢģņä▒ ņ¦äļŗ©ņŚÉ Ļ░Ćņן ĒÜ©Ļ│╝ņĀüņØĖ ļ│æļ”¼ ņåīĻ▓¼ņØ┤ļØ╝Ļ│Ā ņŻ╝ņןĒĢśņśĆļŗż[8]. ļ╣äņŖĘĒĢśĻ▓ī ļŗżļźĖ ņŚ░ĻĄ¼ņŚÉļÅä ņ×¼ņāØ ļ╣äņĀĢĒśĢ(regenerative atypia)ļ│┤ļŗżļŖö ļ╣äņĀĢĒśĢ ņāüĒö╝(atypical epithelium)Ļ░Ć ļŹö ņĢģņä▒ ņ£äĒŚśļÅäĻ░Ć ļåÆļŗżĻ│Ā ņŻ╝ņןĒĢśņśĆĻ│Ā ļ░śļ│ĄĒĢ┤ņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ņ¦äļŗ©ļÉśļŖö Ļ▓ĮņÜ░ņŚÉ ņĢģņä▒ ņ£äĒŚśļÅäĻ░Ć ļŹö ļåÆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż[7]. ļé┤ņŗ£Ļ▓ĮņØ┤ļéś ļ│æļ”¼ ņåīĻ▓¼ņŚÉņä£ ņĢģņä▒ņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉśļ®┤ ņĀüĻĘ╣ņĀüņØĖ ņĀłņĀ£ļź╝ Ļ│ĀļĀżĒĢ┤ņĢ╝ ĒĢśņ¦Ćļ¦ī ņČöņĀü Ļ┤Ćņ░░ ĻĖ░Ļ░äļ│äļĪ£ ļČäņäØĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ņĢģņä▒ņØä ņØśņŗ¼ĒĢĀ ļ¦īĒĢ£ ņåīĻ▓¼ņØ┤ ņŚåļŖö Ļ▓ĮņÜ░ņŚÉ ņ¦äļŗ©ņØ┤ ļŖ”ņ¢┤ņĀĖļÅä 1ļģä ņØ┤ļé┤ļ®┤ ņśłĒøäņŚÉ ņ░©ņØ┤Ļ░Ć ņŚåļŗżĻ│Ā ņŻ╝ņןĒĢśņśĆļŗż[7].
ņ¦äĒ¢ēņä▒ ņ£äņĢöļÅä ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśļŖö Ļ▓ĮņÜ░ļōżņØ┤ ņ׳Ļ│Ā ņ¦äĒ¢ēņä▒ ņ£äņĢöņØś Ļ▓ĮņÜ░ ĻČżņ¢æņØä ļÅÖļ░śĒĢ£ Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄņĢä ņ¢æņä▒ ĻČżņ¢æĻ│╝ Ļ░Éļ│äņØ┤ ņ¢┤ļĀżņÜĖ ņłś ņ׳Ļ│Ā ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉņä£ ņĢöņäĖĒżĻ░Ć ĒÖĢņØĖļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░Ļ░Ć ļō£ļ¼╝ņ¦Ć ņĢŖĻ▓ī ņ׳ļŗż. ņ¦äĒ¢ēņä▒ ņ£äņĢöņØĆ ņĪ░ĻĖ░ ņ£äņĢöĻ│╝ ļŗżļź┤Ļ▓ī ļ╣Āļź┤Ļ▓ī ņ¦äĒ¢ēĒĢśĻ│Ā ņĀäņØ┤Ļ░Ć ļ░£ņāØĒĢĀ ņłś ņ׳ņ¢┤ ņŻ╝ņØśļź╝ ņÜöĒĢśĻ│Ā ņ×¼Ļ▓ĆļÅä ņĄ£ļīĆĒĢ£ ļ╣©ļ”¼ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗż. ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś ņĄ£ņóģ Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢ£ ņŚ░ĻĄ¼ļōżņŚÉņä£ ņ£äņĢöņØĆ ļīĆļČĆļČä ņĪ░ĻĖ░ ņ£äņĢöņØ┤ņŚłņ£╝ļéś ņ¦äĒ¢ēņä▒ ņ£äņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ ĒÖśņ×ÉĻ░Ć 3.1% (3/96) ņ׳ņŚłļŹś ņŚ░ĻĄ¼Ļ░Ć ņ׳ņŚłļŗż[9]. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ņŻ╝ļ”äņØś ļ│ĆĒÖöĻ░Ć ļ»ĖļČäĒÖöĒśĢ ņ£äņĢöņØ┤ļéś ņĀÉļ¦ēĒĢśņĖĄ ņØ┤ņāü ņ╣©ļ▓öņØś ņ£äĒŚśņØĖņ×ÉļĪ£ ņĀ£ņŗ£ĒĢśņśĆļŗż[7].
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī ņĀæĻĘ╝ņŚÉ ļīĆĒĢ£ ĻČīĻ│ĀņĢłņØ┤ ņŚåĻ│Ā Ļ┤ĆļĀ© ļ®öĒāĆļČäņäØņØ┤ļéś ņóģņäżļÅä ņŚåļŖö ņāüĒā£ņØ┤ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśĻ▓ī ļÉśĻ│Ā ņĄ£ĻĘ╝ņŚÉļŖö ļé┤ņŗ£Ļ▓Į Ļ┤Ćņ░░ ņåīĻ▓¼ņØ┤ ļ░£ņĀäĒĢśņŚ¼ ņĢöņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ņŚÉļŖö ņĀĢĒÖĢĒĢ£ ņ¦äļŗ© ņŚåņØ┤ļÅä ņĀüĻĘ╣ņĀüņØĖ ņĀłņĀ£ļź╝ Ļ│ĀļĀżĒĢśĻĖ░ļÅä ĒĢ£ļŗż. ĻĘĖļÅÖņĢłņØś ņŚ░ĻĄ¼ļōżņØä ņ░ĖĻ│ĀĒĢśņŚ¼ ņĀæĻĘ╝ ļ░®ļ▓ĢņØä ņĀĢļ”¼ĒĢ┤ ļ│┤ņĢśļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī Ļ░Ćņן ļ©╝ņĀĆ ņāØĻ░üĒĢśĻ│Ā Ļ░äļŗ©ĒĢśĻ▓ī ĒĢ┤ļ│╝ ņłś ņ׳ļŖö Ļ▓āņØĆ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ņØ┤Ļ▓Āļŗż. ņāØĻ▓Ć Ļ▓Ėņ×Éļź╝ ņØ┤ņÜ®ĒĢ£ ļé┤ņŗ£Ļ▓Į ņĪ░ņ¦ü Ļ▓Ćņé¼ļŖö Ļ░äļŗ©ĒĢśļ®┤ņä£ ļ╣äĻĄÉņĀü ņĀĢĒÖĢĒĢ£ Ļ▓░Ļ│╝ļź╝ ņ¢╗ņØä ņłś ņ׳ļŖö ņ▓½ ļ▓łņ¦Ė ņ¦äļŗ© ļÅäĻĄ¼ņØ┤ļéś ņĢ×ņä£ ņäżļ¬ģņ▓śļ¤╝ ĒĢ£Ļ│äĻ░Ć ņ׳ļŗż. ņĢ×ņäĀ ņĪ░ņ¦ü Ļ▓Ćņé¼ņŚÉ ļ╣äĒĢ┤ ņĀĢĒÖĢļÅäļź╝ ļåÆņØ┤ĻĖ░ ņ£äĒĢ£ ļ░®ļ▓Ģņ£╝ļĪ£ Ēü¼ĻĖ░Ļ░Ć Ēü░ Ļ▓Ėņ×Éļź╝ ņé¼ņÜ®ĒĢśĻ▒░ļéś Ļ░ÖņØĆ ļ│æļ│ĆņŚÉ ļīĆĒĢ┤ ņĪ░ņ¦ü Ļ▓Ćņé¼ Ēܤņłśļź╝ ņŚ¼ļ¤¼ ļ▓ł ĒĢĀ ņłś ņ׳Ļ▓Āļŗż. ĒĢśņ¦Ćļ¦ī Ēü░ Ļ▓Ėņ×Éļź╝ ņé¼ņÜ®ĒĢśļŖö Ļ▓āņØĆ ņĀĢĒÖĢļÅäļź╝ ļåÆņØ╝ ņłś ņŚåļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[17]. ļ░śļ®┤ņŚÉ ņŚ¼ļ¤¼ ļ▓ł ņĪ░ņ¦ü Ļ▓Ćņé¼ĒĢśļŖö Ļ▓āņØĆ ņ¦äļŗ©ņ£©ņØä ļåÆņØ╝ ņłś ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż. ņ£äņĢöņØś ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ ĒĢ£ ļ▓łņØś ņĪ░ņ¦ü Ļ▓Ćņé¼ņØś ņ¦äļŗ©ņ£©ņØ┤ 70%ņśĆļŹś ļ░śļ®┤ņŚÉ 3ĒÜī ļŹö ņČöĻ░ĆļĪ£ ņĪ░ņ¦ü Ļ▓Ćņé¼ ņŗ£ņŚÉļŖö ņ¦äļŗ©ņ£©ņØ┤ 95% ņØ┤ņāüņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[16]. ĒĢśņ¦Ćļ¦ī ņŚ¼ļ¤¼ ļ▓ł ņĪ░ņ¦ü Ļ▓Ćņé¼ ņŗ£ņŚÉ ņČ£ĒśłņØ┤ļéś ņĪ░ņ¦üņØś ļ│ĆĒśĢ Ēś╣ņØĆ ņä¼ņ£ĀĒÖöĻ░Ć ļ¼ĖņĀ£Ļ░Ć ļÉĀ ņłś ņ׳ļŗż. ņ×äņāüņŚÉņä£ ņČ£ĒśłņØ┤ ļ¼ĖņĀ£Ļ░Ć ļÉśļŖö Ļ▓ĮņÜ░ļŖö ĻĘ╣Ē׳ ļō£ļ¼╝ņ¦Ćļ¦ī ļ│æļ│ĆņŚÉ ļīĆĒĢ┤ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ļź╝ Ļ│ĀļĀżĒĢ£ļŗżļ®┤ ņŚ¼ļ¤¼ ļ▓ł ņĪ░ņ¦ü Ļ▓Ćņé¼ļĪ£ ņØĖĒĢ£ ņä¼ņ£ĀĒÖöļŖö ļ¼ĖņĀ£Ļ░Ć ļÉĀ ņłś ņ׳ļŗż. ļö░ļØ╝ņä£ ņĀĢĒÖĢĒĢ£ ņ▓½ ļ▓łņ¦Ė ņĪ░ņ¦ü Ļ▓Ćņé¼Ļ░Ć Ļ░Ćņן ņżæņÜöĒĢśĻ▓Āļŗż. ņĀĢĒÖĢĒĢ£ ņĪ░ņżĆ ņāØĻ▓ĆņØ┤ ļÉ£ļŗżļ®┤ ņ¦äļŗ©ņ£©ņØä 92.3%Ļ╣īņ¦Ć ļ│┤Ļ│ĀĒĢśĻ│Ā ņ׳ļŗż[21]. ņČöĒøä ļé┤ņŗ£Ļ▓Į ņĀłņĀ£Ļ╣īņ¦Ć Ļ│ĀļĀżĒĢśņŚ¼ ņ▓½ ļ▓łņ¦Ė ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ņāēņĪ░ ļ│ĆĒÖöļéś ĒĢ©ļ¬░ņØ┤ ņ׳ļŖö ļČĆņ£äņŚÉ ņĄ£ļīĆĒĢ£ ņĀĢĒÖĢĒĢśĻ▓ī ĒĢśĻ│Ā 1~2ĒÜī ņĀĢļÅä ņČöĻ░ĆļĪ£ ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ĒĢśļŖö Ļ▓āņØ┤ ĒśäņŗżņĀüņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
ņČöņĀü ļé┤ņŗ£Ļ▓Į Ļ▓Ćņé¼ņØś ņŗ£ĻĖ░ ņŚŁņŗ£ ņĀĢĒĢ┤ņ¦ä ļ░öĻ░Ć ņŚåņ£╝ļéś ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØ┤ļéś ņĪ░ņ¦ü Ļ▓Ćņé¼ Ļ▓░Ļ│╝ņŚÉņä£ ņĢģņä▒ņØ┤ ņØśņŗ¼ļÉ£ļŗżļ®┤ ņĄ£ļīĆĒĢ£ ļ╣©ļ”¼ ņČöņĀü ļé┤ņŗ£Ļ▓ĮņØä ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢśĻ│Ā, ĻĘĖļĀćņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ ņŗżņĀ£ ņ×äņāüņŚÉņä£ļŖö 3Ļ░£ņøö Ēś╣ņØĆ 6Ļ░£ņøö ļÆż ņŗ£Ē¢ēĒĢśĻ│Ā ņ׳ļŗż. ņČöņĀü Ļ┤Ćņ░░ ĻĖ░Ļ░äņØ┤ ļ¬ģņŗ£ļÉśņ¢┤ ņ׳ļŖö ņŚ░ĻĄ¼ļōżņŚÉņä£ļÅä 3Ļ░£ņøö Ēś╣ņØĆ 6Ļ░£ņøö ļÆż ļé┤ņŗ£Ļ▓ĮņØä ņŗ£Ē¢ēĒĢśņśĆļŗż[6,7,22]. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĢöņØś ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö ļ│æļ│ĆņØĆ 3Ļ░£ņøö ļÆż, ņŚåļŖö ļ│æļ│ĆņØĆ 6Ļ░£ņøö ļÆżļĪ£ ņČöņĀü Ļ▓Ćņé¼ĒĢĀ Ļ▓āņØä ĻČīĻ│ĀĒĢśņśĆĻ│Ā ņĢģņä▒ņØä ņØśņŗ¼ĒĢĀ ļ¦īĒĢ£ ņåīĻ▓¼ņØ┤ ņŚåļŖö Ļ▓ĮņÜ░ņŚÉ ņ¦äļŗ©ņØ┤ ļŖ”ņ¢┤ņĀĖļÅä 1ļģä ņØ┤ļé┤ļ®┤ ņśłĒøäņŚÉ ņ░©ņØ┤Ļ░Ć ņŚåļŗżĻ│Ā ņŻ╝ņןĒĢśņśĆļŗż[7]. ņÜöņĢĮĒĢśļ®┤ ļé┤ņŗ£Ļ▓Į ņ×¼Ļ▓ĆņØĆ ņĢģņä▒ņØ┤ ņØśņŗ¼ļÉ£ļŗżļ®┤ ņĄ£ļīĆĒĢ£ ļ╣©ļ”¼ ņŗ£Ē¢ēĒĢśĻ│Ā ĻĘĖļĀćņ¦Ć ņĢŖļŗżļ®┤ 3Ļ░£ņøö Ēś╣ņØĆ 6Ļ░£ņøö ļÆżņŚÉ ņŗ£Ē¢ēĒĢśļ®░ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ ņŗ£ņŚÉļŖö ņ▓½ ļ▓łņ¦Ė ņāØĻ▓ĆņØä ņĄ£ļīĆĒĢ£ ņĀĢĒÖĢĒĢśĻ▓ī ņĪ░ņżĆ ņāØĻ▓ĆĒĢ┤ņĢ╝Ļ▓Āļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī Ļ▓░Ļ│╝ļź╝ ĻĖ░Ļ│äņĀüņ£╝ļĪ£ ļ░øņĢäļōżņØ┤ĻĖ░ļ│┤ļŗż ļ│æļ”¼Ļ│╝ņÖĆņØś ņåīĒåĄņØ┤ ņżæņÜöĒĢśĻ▓Āļŗż. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØĆ ļ│æļ”¼ņĀüņ£╝ļĪ£ ņ×¼ņāØ ļ╣äņĀĢĒśĢ(regenerative atypia)Ļ│╝ ļ╣äņĀĢĒśĢ ņāüĒö╝(atypical epithelium)ļĪ£ ĻĄ¼ļČäĒĢĀ ņłś ņ׳ļŗż. ņ×¼ņāØ ļ╣äņĀĢĒśĢņØĆ Ļ│╝ņŚ╝ņāēņä▒ ĒĢĄ(hyperchromatic nucleus), ļŗżņ¢æĒĢ£ ĒĢĄņØś Ēü¼ĻĖ░ņÖĆ ļ¬©ņ¢æ, ĒĢĄņØś ņ£äņ╣ś ļ│ĆĒÖö, ĒĢĄ-ņäĖĒżņ¦ł ļ╣äņ£©ņØś ņ”ØĻ░Ć ļō▒ ņŻ╝ļĪ£ ĒĢĄņØś ņØ┤ņāüņØä Ēæ£ĒśäĒĢśļŖö ņÜ®ņ¢┤ņØ┤ļ®░ ļ╣äņĀĢĒśĢ ņāüĒö╝ļŖö ĻĄŁņåīĒÖöļÉ£ ņäĖĒż ĻĄ░ņ¦æ Ēś╣ņØĆ ļČłĻĘ£ņ╣ÖĒĢ£ ĒśĢĒā£ņØś ņāś ļō▒ ĻĄ¼ņĪ░ņĀüņØĖ ņÖ£Ļ│ĪņØ┤ Ļ┤Ćņ░░ļÉĀ ļĢī ņé¼ņÜ®ĒĢśļŖö ņÜ®ņ¢┤ņØ┤ļŗż[23]. ĒĢĄņØś ņØ┤ņāüņØĖ ņ×¼ņāØ ļ╣äņĀĢĒśĢļ│┤ļŗż ĻĄ¼ņĪ░ņØś ņØ┤ņāüņØĖ ļ╣äņĀĢĒśĢ ņāüĒö╝Ļ░Ć ņĢģņä▒ Ļ░ĆļŖźņä▒ņØ┤ ļŹö ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[7,8]. ņĪ░ņ¦ü Ļ▓░Ļ│╝ņŚÉņä£ ņ×¼ņāØ ļ╣äņĀĢĒśĢņØś Ļ▓ĮņÜ░ ņČöņĀü ļé┤ņŗ£Ļ▓Į ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ 6Ļ░£ņøö ļÆżņŚÉ, ļ╣äņĀĢĒśĢ ņāüĒö╝ņØś Ļ▓ĮņÜ░ 3Ļ░£ņøö ļÆżņŚÉ ĒĢĀ Ļ▓āņØä ĻČīĻ│ĀĒĢ£ ņŚ░ĻĄ¼ļÅä ņ׳ņŚłļŗż[7]. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│Āļ░øņĢśņØä ļĢī ļ│æļ”¼Ļ│╝ņÖĆ ņåīĒåĄĒĢ┤ņä£ ņĪ░ņ¦ü ņŖ¼ļØ╝ņØ┤ļō£ļź╝ ļŗżņŗ£ ļČäņäØĒĢśņŚ¼ ļŹö ņĢģņä▒ Ļ░ĆļŖźņä▒ņØ┤ ļåÆņØĆ ņåīĻ▓¼ņØ┤ ņŚåļŖöņ¦Ć ĒÖĢņØĖĒĢ┤ļ│┤Ļ│Ā ņāüņØśĒĢśļŖö Ļ▓āņØ┤ ĒÖśņ×ÉņØś ņČöņĀü ļé┤ņŗ£Ļ▓Į ņŗ£ĻĖ░ Ļ▓░ņĀĢņØ┤ļéś ņ╣śļŻī ļ░®Ē¢ź Ļ▓░ņĀĢņŚÉ ļÅäņøĆņØ┤ ļÉĀ ņłś ņ׳Ļ▓Āļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØĆ ņ¦äļŗ©ņØ┤ ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņ£╝ļ»ĆļĪ£ ņĀĢĒÖĢĒĢ£ ņ¦äļŗ©ņØä ņ£äĒĢ£ ļé┤ņŗ£Ļ▓Į ņ×¼Ļ▓Ć, ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼Ļ░Ć ņøÉņ╣ÖņØ┤Ļ▓Āņ£╝ļéś ņāüĒÖ®ņŚÉ ļö░ļØ╝ ņĀłņĀ£ļź╝ ļ░öļĪ£ ņŗ£Ē¢ēĒĢśļŖö Ļ▓ĮņÜ░ļōżņØ┤ ņóģņóģ ņ׳ļŗż. ĒŖ╣Ē׳ ĒĢ£ĻĄŁņ▓śļ¤╝ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ļź╝ ļ¦ÄņØ┤ ņŗ£Ē¢ēĒĢśĻ│Ā ņ׳ļŖö ņ¦ĆņŚŁņŚÉņä£ļŖö ņĢģņä▒ņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉĀ ļĢī ņĀłņĀ£ļź╝ ĒĢ┤ ļ│╝ ņłś ņ׳Ļ▓Āļŗż. ĒĢśņ¦Ćļ¦ī ņĀĢĒÖĢĒĢ£ ņ¦äļŗ© ņŚåņØ┤ ļ░öļĪ£ ņĀłņĀ£ļŖö ļ░śļō£ņŗ£ ņĢģņä▒ņØ┤ ņØśņŗ¼ļÉśļŖö ņāüĒÖ®ņŚÉņä£ ņŗ£Ē¢ēĒĢ┤ņĢ╝Ļ▓Āļŗż. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņŚÉņä£ ņĢģņä▒ņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ļŖö ņĢ×ņä£ ņ¢ĖĻĖēĒĢ£ Ļ▓āņ▓śļ¤╝ 1 cm ņØ┤ņāüņØś Ēü¼ĻĖ░ņÖĆ ļ░£ņĀü, ņ×Éļ░£ ņČ£Ēśł, ĒĢ©ļ¬░ Ļ░ÖņØĆ ĒŖ╣ņ¦ĢļōżņØ┤ ņ׳Ļ▓Āļŗż[6,7,9,10]. ņŗżņĀ£ ņŚ░ĻĄ¼ļōżņŚÉņä£ 5.7~34.6%ņØś ĒÖśņ×ÉļōżņØ┤ ņĢöņØ┤ļéś ņØ┤ĒśĢņä▒ņ”ØņØś ĒÖĢņŗżĒĢ£ ņ¦äļŗ© ņŚåņØ┤ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ļź╝ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā ņØ┤ ņżæ 71.4~87%Ļ░Ć ņĢöņØ┤ļéś ņØ┤ĒśĢņä▒ņ”Øņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż[6,7,9,10]. ļé┤ņŗ£Ļ▓Į ņĀłņĀ£ņłĀ ņĀäņŚÉļŖö ņĪ░ĻĖ░ ņ£äņĢöņØä ņŗ£ņé¼ĒĢśļŖö ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØä ļ░śļō£ņŗ£ ņłÖņ¦ĆĒĢśĻ│Ā ņ׳ņ¢┤ņĢ╝Ļ▓Āļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉ£ ļ│æļ│Ćļōż ņżæņŚÉ ņ¦äĒ¢ēņä▒ ņ£äņĢöņØ┤ļéś ņĀÉļ¦ēĒĢśņĖĄ ņ╣©ļ▓ö ņĢöņ£╝ļĪ£ ņłśņłĀņĀü ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢ£ ļ│æļ│ĆļōżņØ┤ ņ׳ņØä ņłś ņ׳ļŗż. ņłśņłĀņØĆ ņ£äļź╝ ņĀłņĀ£ĒĢśļŖö ņ╣©ņŖĄņĀüņØĖ ņ╣śļŻī ļ░®ļ▓Ģņ£╝ļĪ£ ņŗĀņżæĒĢśĻ▓ī Ļ▓░ņĀĢĒĢ┤ņĢ╝ĒĢśļ®░ ņĄ£ļīĆĒĢ£ ņĪ░ņ¦üĒĢÖņĀüņ£╝ļĪ£ ņĢöņØ┤ ņ¦äļŗ©ļÉ£ ĒøäņŚÉ ņ¦äĒ¢ēĒĢśļŖö Ļ▓āņØ┤ ļ░öļ×īņ¦üĒĢśļŗż. ĒĢśņ¦Ćļ¦ī ņ¦äĒ¢ēņä▒ ņ£äņĢöņØś Ļ▓ĮņÜ░ ļ╣ĀļźĖ ņ¦äĒ¢ēĻ│╝ ņĀäņØ┤ļź╝ ņØ╝ņ£╝Ēé¼ ņłś ņ׳Ļ│Ā ļ░śļ│ĄļÉśļŖö ņĪ░ņ¦ü Ļ▓Ćņé¼Ļ░Ć ņŗ£Ļ░äņØä ņ¦ĆņŚ░ņŗ£Ēé¼ ņłś ņ׳ņ¢┤ ļ░öļĪ£ ņłśņłĀņØä ņŗ£Ē¢ēĒĢśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦żņÜ░ ļō£ļ¼╝Ļ▓ī ņ׳ļŗż. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś ņĄ£ņóģ Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢ£ ņŚ░ĻĄ¼ļōżņŚÉņä£ļÅä ņłśņłĀņØä ņŗ£Ē¢ēĒĢ£ ĒÖśņ×ÉļōżņØ┤ 3.7~20.8%Ļ╣īņ¦Ć ņ׳ņŚłĻ│Ā ņĀĢĒÖĢĒĢ£ ņĢö ņ¦äļŗ© ņŚåņØ┤ ļ░öļĪ£ ņłśņłĀņØä ņ¦äĒ¢ēĒ¢łļŹś ĒÖśņ×ÉļōżļÅä Ļ░ü ņŚ░ĻĄ¼ļ│äļĪ£ 4~11ļ¬ģ ņĀĢļÅä ņ׳ņŚłļŗż[6-10]. ņŚ░ĻĄ¼ļōż ņżæņŚÉ ņłśņłĀņØä ņŗ£Ē¢ēĒĢśņśĆņ£╝ļéś ņĢöņäĖĒżļéś ņØ┤ĒśĢņä▒ņ”ØņØ┤ ĒÖĢņØĖļÉśņ¦Ć ņĢŖņØĆ ĒÖśņ×ÉļÅä ņ׳ņŚłļŗż[10]. ņĀĢĒÖĢĒĢ£ ņĪ░ņ¦ü Ļ▓Ćņé¼ņÖĆ ņ¦äļŗ©ņØ┤ ņżæņÜöĒĢśĻ▓Āņ£╝ļéś ņ¦äĒ¢ēņä▒ ņ£äņĢöņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉ£ļŗżļ®┤ ņ×¼Ļ▓ĆĻ│╝ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ļĪ£ ņØĖĒĢ┤ ņŗ£Ļ░äņØä ņ¦Ćņ▓┤ĒĢśļ®┤ ņĢłļÉśĻ▓Āļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī ļ│æļ│ĆņØä ĒÖĢļīĆ ļé┤ņŗ£Ļ▓Į(magnifying endoscopy)ņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢ┤ ļ│╝ ņłś ņ׳Ļ▓Āļŗż. ņĪ░ĻĖ░ ņ£äņĢöņØś ņ¦äļŗ©ņŚÉ ĒÖĢļīĆ ļé┤ņŗ£Ļ▓ĮņØś ņ£ĀņÜ®ņä▒ņØĆ ņØ┤ļ»Ė ņל ņĢīļĀżņĀĖ ņ׳ļŗż[24,25]. ņØ┤ļź╝ ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś ņ¦äļŗ©ņŚÉļÅä ņĀüņÜ®ĒĢśņŚ¼ demarcation lineņØä ĒÖĢņØĖĒĢśĻ│Ā ļ»ĖņäĖĒśłĻ┤ĆņØś ĻĄ¼ņĪ░(microvascular architecture)ņÖĆ ļ»ĖņäĖĒæ£ļ®┤ ĒśĢĒā£(microsurface structure)ļź╝ Ļ┤Ćņ░░ĒĢśņŚ¼ ņĢģņä▒ņØś Ļ░ĆļŖźņä▒ņØä ĒīÉļŗ©ĒĢśļŖö ļŹ░ ļÅäņøĆņØä ņ¢╗ņØä ņłś ņ׳Ļ▓Āļŗż. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņŚÉ ĒÖĢļīĆ ļé┤ņŗ£Ļ▓ĮņØä ņĀüņÜ®ĒĢ£ ņŚ░ĻĄ¼ļŖö ņŚåņŚłņ£╝ļéś ĒÖĢļīĆ ļé┤ņŗ£Ļ▓Įņ£╝ļĪ£ ņĪ░ĻĖ░ ņ£äņĢöņŚÉņä£ ļ╣äņĀĢĒśĢņØś ņĀĢļÅäņÖĆ ļ▓öņ£äļź╝ ĒÖĢņØĖĒĢ£ ņ”ØļĪĆļ│┤Ļ│ĀĻ░Ć ņ׳ņŚłĻ│Ā[26] ņĄ£ĻĘ╝ņŚÉ ĒÖĢļīĆ ļé┤ņŗ£Ļ▓ĮņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĪ░ĻĖ░ ņ£äņĢöĻ│╝ ņäĀņóģņØä Ļ░Éļ│äĒĢśļŖö ņŚ░ĻĄ¼Ļ░Ć ņ׳ņŚłļŗż[27]. ļ│æļ│ĆņØś Ļ░Éļ│äļ┐Éļ¦ī ņĢäļŗłļØ╝ ĒÖĢļīĆ ļé┤ņŗ£Ļ▓ĮņØĆ ņØ┤ņāü ņ׳ļŖö ļČĆņ£äļź╝ ņĀĢĒÖĢĒ׳ ņĪ░ņżĆ ņāØĻ▓ĆņØä ĒĢśļŖö ļŹ░ļÅä ņé¼ņÜ®ĒĢĀ ņłś ņ׳Ļ▓Āļŗż.
ļŗżņØīņ£╝ļĪ£ ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņØä ļĢī ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ ņĀ£ĻĘĀ ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳Ļ▓Āļŗż. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØ┤ ĒÖĢņØĖļÉśņŚłņØä ļĢī ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ ņĀ£ĻĘĀ ņ╣śļŻīļź╝ ĒĢ┤ņĢ╝ĒĢ£ļŗżļŖö ĻČīĻ│Ā ņé¼ĒĢŁņØĆ ņŚåļŗż. ĒĢśņ¦Ćļ¦ī ņØ┤ļĪĀņĀüņ£╝ļĪ£ ļ╣äņĀĢĒśĢņØĆ ņŚ╝ņ”ØĻ│╝ Ļ┤ĆļĀ© ņ׳ņØä ņłś ņ׳Ļ│Ā ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ Ļ░ÉņŚ╝ņØĆ ĻĖē, ļ¦īņä▒ ņŚ╝ņ”ØņØś ņøÉņØĖņØ┤ ļÉĀ ņłś ņ׳ņ£╝ļ®░ ņ£äņĢöņØś ņøÉņØĖņØ┤ ļÉĀ ņłś ņ׳ļŗż. ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ņÖĆ ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś Ļ┤ĆļĀ©ņä▒ņØä ļ│┤Ļ│ĀĒĢ£ ņŚ░ĻĄ¼ļōżņØ┤ ņ׳Ļ│Ā[9,28] ņØ┤ ņżæ ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ ņĀ£ĻĘĀ ņ╣śļŻī ĒøäņŚÉ ņ×¼ņāØ ļ╣äņĀĢĒśĢņØ┤ ĒśĖņĀäļÉ©ņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż[28]. ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ ņĀ£ĻĘĀ ņ╣śļŻī ĒøäņŚÉ ņ£äņäĀņóģņØś Ēć┤ĒÖöļź╝ ļ│┤Ļ│ĀĒĢ£ ņŚ░ĻĄ¼ļÅä ņ׳ņŚłļŗż[29]. ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØś ļé┤ņŗ£Ļ▓Į ņČöņĀü Ļ▓Ćņé¼ ņé¼ņØ┤ņŚÉ ĒŚ¼ļ”¼ņĮöļ░ĢĒä░ ĻĘĀ Ļ░ÉņŚ╝ņØ┤ ņ׳ļŗżļ®┤ ņĀ£ĻĘĀ ņ╣śļŻīļź╝ ĒĢśļŖö Ļ▓āļÅä ĒĢśļéśņØś ņĀäļץņØ┤ ļÉĀ ņłś ņ׳Ļ▓Āļŗż.
ņ£äņØś ļČłļ¬ģĒÖĢĒĢ£ ņŗĀņāØļ¼╝ņØĆ ļ│æļ”¼ ņ¦äļŗ©ņŚÉņä£ ņóģņ¢æņØĖņ¦Ć ņĢäļŗīņ¦Ć ļ¬ģĒÖĢĒĢśĻ▓ī Ļ▓░ļĪĀ ļé┤ļ”¼ĻĖ░ ņ¢┤ļĀżņÜ┤ Ļ▓ĮņÜ░ņŚÉ ņé¼ņÜ®ĒĢśļŖö ņÜ®ņ¢┤ļĪ£ ņŗżņĀ£ ļ│æļ│ĆņØĆ ņŚ╝ņ”ØļČĆĒä░ ņ¦äĒ¢ēņä▒ ņ£äņĢöĻ╣īņ¦Ć ļŗżņ¢æĒĢĀ ņłś ņ׳Ļ│Ā ņŗżņĀ£ ņĀ£Ļ▒░Ļ░Ć ĒĢäņÜöĒĢ£ ņØ┤ĒśĢņä▒ņ”ØņØ┤ļéś ņ£äņĢöņ£╝ļĪ£ ņĄ£ņóģ ņ¦äļŗ©ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦Äļŗż. ņĢäņ¦ü ĒŖ╣ļ│äĒĢ£ Ļ░ĆņØ┤ļō£ļØ╝ņØĖņØ┤ļéś ĻČīĻ│ĀņĢłņØ┤ ņŚåņ¢┤ ļé┤ņŗ£Ļ▓Į ņ×¼Ļ▓ĆĻ│╝ ņ×¼ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ĒĢśĻ│Ā ņ׳ņ£╝ļéś ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ņØ┤ļéś ļ│æļ”¼ņĀüņ£╝ļĪ£ ņĢģņä▒ņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ ņĀĢĒÖĢĒĢ£ ņ¦äļŗ© ņŚåņØ┤ ļ░öļĪ£ ļé┤ņŗ£Ļ▓Į ņĀłņĀ£, ĻĘ╣Ē׳ ņØ╝ļČĆņŚÉņä£ ņłśņłĀĻ╣īņ¦Ć ļ░öļĪ£ ņŗ£Ē¢ēĒĢśĻĖ░ļÅä ĒĢ£ļŗż. ļé┤ņŗ£Ļ▓Į ņ×¼Ļ▓Ć ņŗ£ņŚÉļŖö Ļ░Ćņן ņØ┤ĒśĢņä▒ņØ┤ ņŗ¼ĒĢĀ ļČĆņ£äļź╝ ņĀĢĒÖĢĒĢśĻ▓ī ņĪ░ņżĆĒĢśņŚ¼ ņŗ£Ē¢ēĒĢśļŖö ņ▓½ ņĪ░ņ¦ü Ļ▓Ćņé¼Ļ░Ć Ļ░Ćņן ņżæņÜöĒĢśĻ▓Āļŗż. ņ×¼Ļ▓ĆņŚÉņä£ļÅä ļ¬ģĒÖĢĒĢśĻ▓ī ņ¦äļŗ©ņØ┤ ļé┤ļĀżņ¦Ćņ¦Ć ņĢŖņ£╝ļéś ņĢöņØ┤ Ļ░ĢļĀźĒ׳ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ ļ░öļĪ£ ņĀłņĀ£ļź╝ Ļ│ĀļĀżĒĢĀ ņłś ņ׳Ļ▓Āņ£╝ļéś ņØ┤ļ¤░ Ļ▓ĮņÜ░ ņĢöņØä ņØśņŗ¼ĒĢśĻ▓ī ĒĢśļŖö ļé┤ņŗ£Ļ▓Į ņåīĻ▓¼ļōżņØä ņłÖņ¦ĆĒĢśĻ│Ā ņ׳ņ¢┤ņĢ╝ ļÉśĻ│Ā ļŗżņ¢æĒĢ£ ļ│æļ│ĆļōżņØä Ļ┤Ćņ░░ĒĢśļŖö Ļ▓ĮĒŚśņØ┤ ĒĢäņÜöĒĢśĻ▓Āļŗż. ļ│æļ”¼Ļ│╝ ņØśņé¼ņÖĆ ņāüņØśĻ░Ć ņżæņÜöĒĢśļ®░ ļ│æļ”¼ĒĢÖņĀüņ£╝ļĪ£ ņĢöņØś ņ£äĒŚśņØ┤ ļåÆņØĆ Ļ▓ĮņÜ░ ļ╣ĀļźĖ ņ×¼Ļ▓Ć Ēś╣ņØĆ ņĀłņĀ£Ļ░Ć ĒĢäņÜöĒĢĀ ņłś ņ׳ļŗż. ņ×¼Ļ▓ĆņØś ņŗ£ĻĖ░Ļ░Ć ļ¬ģĒÖĢĒ׳ ņĀĢĒĢ┤ņĀĖ ņ׳ņ¦Ć ņĢŖņ£╝ļéś ņŻ╝ļ”äņØś ļ│ĆĒÖö ļō▒ ņ¦äĒ¢ēņä▒ ņ£äņĢöņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ ņ×¼Ļ▓ĆņŚÉ ņŗ£Ļ░äņØä ņ¦Ćņ▓┤ĒĢśļ®┤ ņĢł ļÉśĻ▓Āļŗż.
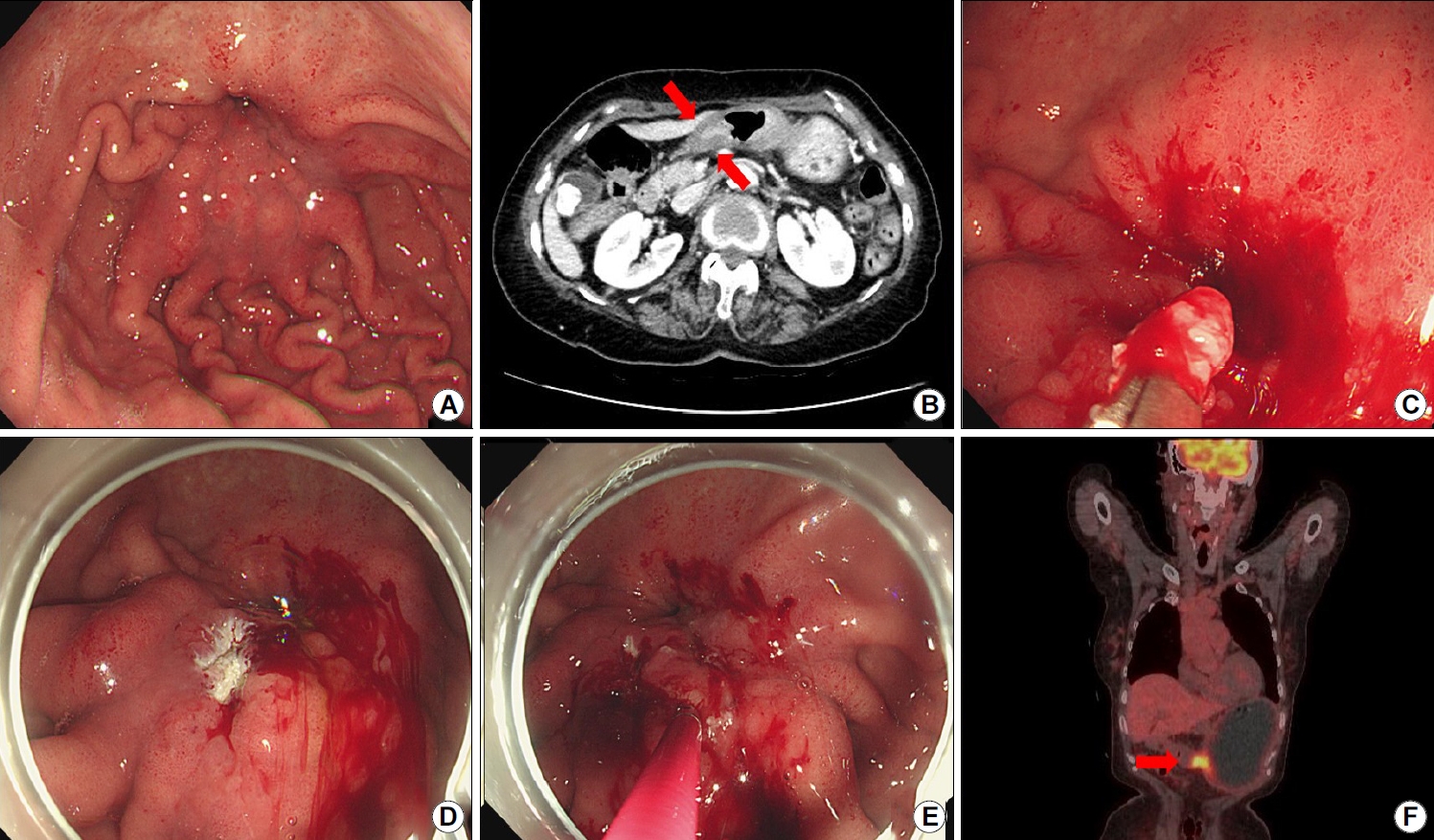
Fig.┬Ā1.
Representative case of a 66-year-old woman with a suspected malignant ulcer, which was reported as showing atypia on endoscopic forceps biopsy. Endoscopic submucosal dissection was performed for the diagnosis and treatment of this lesion. The lesion was diagnosed as submucosal invasive cancer. Depth of invasion was 2000 ╬╝m; hence, additional surgery was done. (A-C) Images showing an ulcer (20 mm) with an irregular border and a dirty base, located at the greater curvature of the distal antrum. (D-F) Images showing endoscopic submucosal dissection and resected specimen after en-bloc resection.
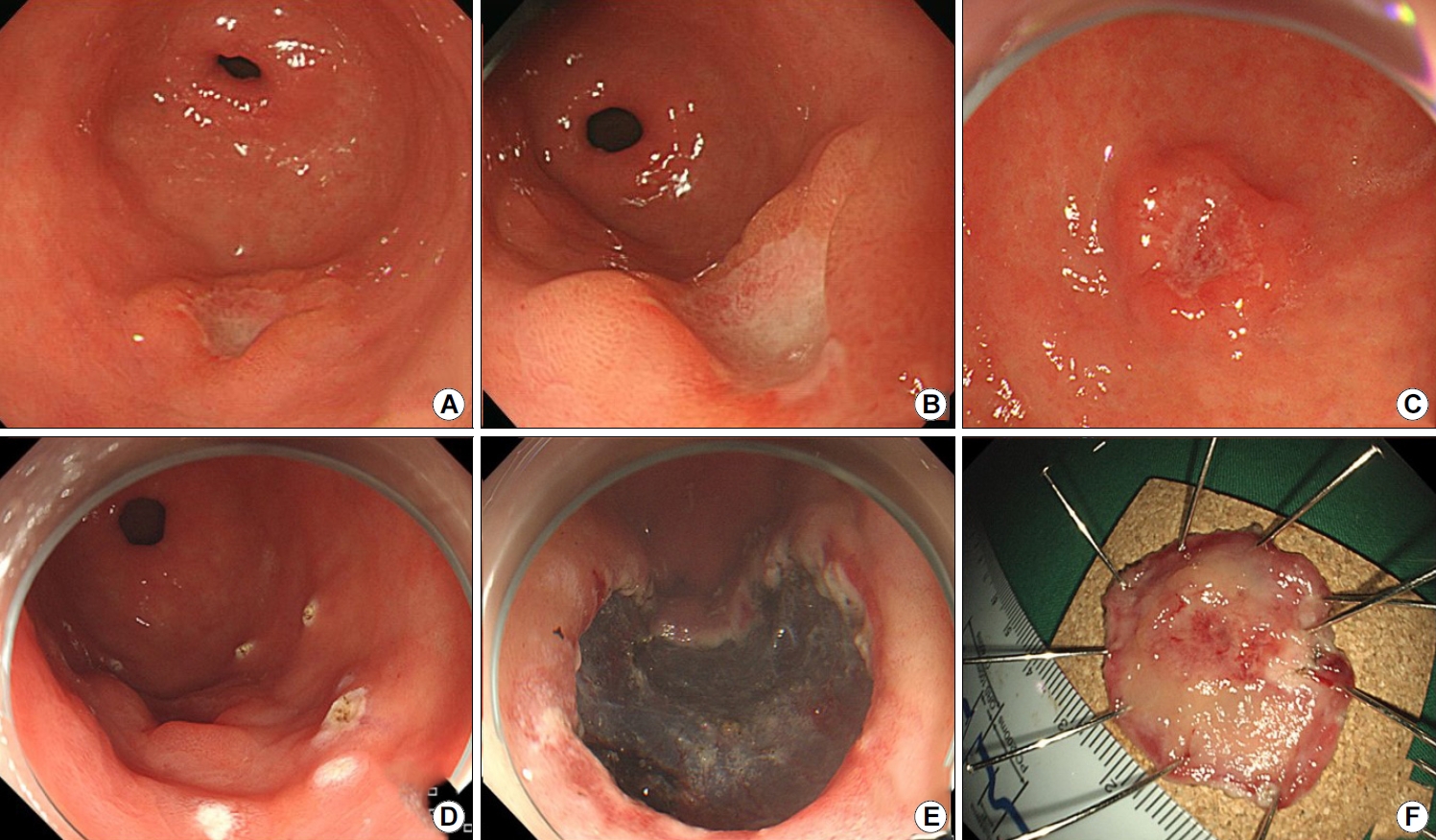
Fig.┬Ā2.
Representative case of a 68-year-old man initially diagnosed with an indefinite-for-neoplasia lesion . After the resection, the lesion was diagnosed as adenoma with low-grade dysplasia. (A, B) Images showing a flat, elevated mucosal lesion (10 mm) located at the lesser curvature of the antrum (arrow). (C, D) Images showing endoscopic submucosal dissection-induced ulcer and resected specimen after en-bloc resection.
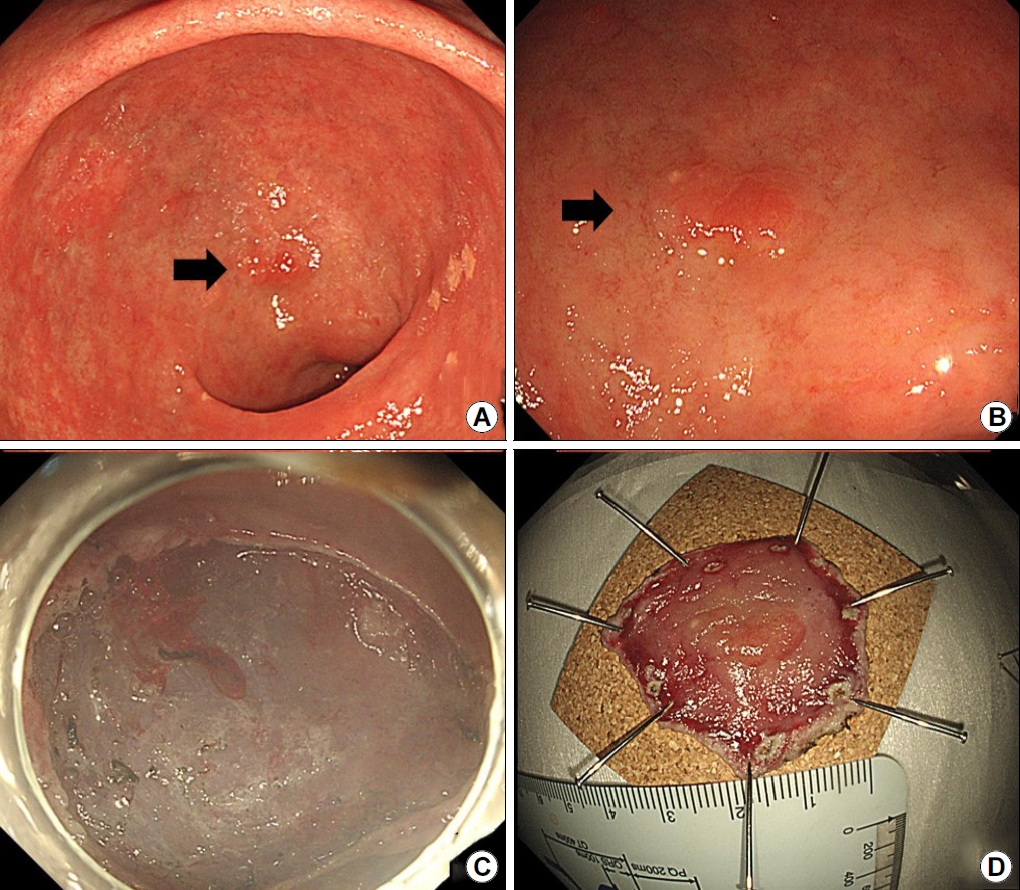
Fig.┬Ā3.
Representative case of a 61-year-old man initially diagnosed with indefinite-for-neoplasia, who was definitively diagnosed as having an early gastric cancer. (A, B) Images showing a flat mucosal lesion with unclear margins and scar-induced changes at the lesser curvature of the gastric body (arrow). (C, D) Images showing endoscopic biopsy procedure and an artificial ulcer after the biopsy. (E-G) Images showing endoscopic submucosal dissection and resected specimen after en-bloc resection. (H) Image showing carcinoma (circle) and defects (arrow) secondary to previous biopsies near the cancer (H&E staining ├Ś40).
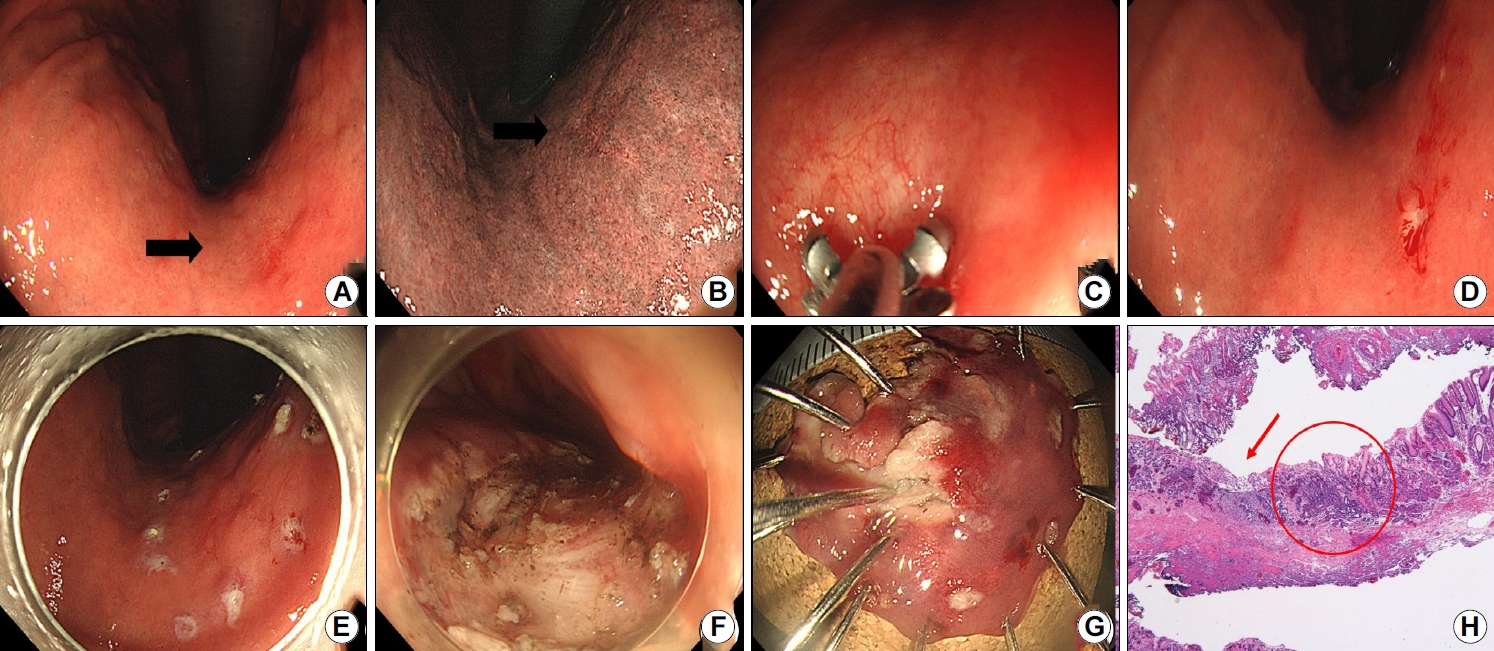
Fig.┬Ā4.
Representative case of a 72-year-old woman who initially underwent endoscopic forceps and unroofing biopsies. The lesion was diagnosed as atypia; however, final diagnosis after gastrectomy was gastric cancer. (A) Image showing convergence of gastric folds in the antrum associated with a high suspicion for gastric cancer. (B) Abdominal computed tomography scan showing diffuse wall thickening in the antrum (arrows). (C) Image showing endoscopic biopsy procedure. (D, E) Endoscopic images of an unroofing biopsy technique. (F) Positron emission tomography scan showing high uptake which is suspicious for malignancy (arrow). The patient underwent gastrectomy, and gastric cancer was confirmed.
Table┬Ā1.
Final Histopathological Findings of Gastric Indefinite-for-neoplasia Related Studies
| Study | Number | Cancer (%) | Dysplasia (%) | Non-neoplasm (%) | Risk factors related cancer |
|---|---|---|---|---|---|
| Yu et al. [9] (2014) | 96 | 37.6 | 9.4 | 53.0 | Ōēź1 cm |
| Depression | |||||
| Goo et al. [6] (2015) | 119 | 21.9 | 5.0 | 73.1 | Ōēź1 cm |
| Redness | |||||
| Kwon et al. [7] (2019) | 461 | 22.6 | 8.9 | 68.5 | Ōēź1 cm |
| Single lesion | |||||
| Spontaneous bleeding | |||||
| Repeated IFND | |||||
| Atypical epithelium | |||||
| Yim et al. [8] (2020) | 123 | 29.3 | 17.9 (high grade 6.5) | 52.8 | >25% |
| SAA | |||||
| Cho et al. [10] (2021) | 457 | 28.0 | 11.4 (high grade 4.6) | 60.6 | Ōēź1 cm |
| Erythema | |||||
| Spontaneous bleeding | |||||
| Depression |
REFERENCES
2. Goldstein NS, Lewin KJ. Gastric epithelial dysplasia and adenoma: historical review and histological criteria for grading. Hum Pathol 1997;28:127ŌĆō133.


3. Kim JM, Cho MY, Sohn JH, et al. Diagnosis of gastric epithelial neoplasia: dilemma for Korean pathologists. World J Gastroenterol 2011;17:2602ŌĆō2610.



4. Stolte M. The new Vienna classification of epithelial neoplasia of the gastrointestinal tract: advantages and disadvantages. Virchows Arch 2003;442:99ŌĆō106.



6. Goo JJ, Choi CW, Kang DH, et al. Risk factors associated with diagnostic discrepancy of gastric indefinite neoplasia: who need en bloc resection? Surg Endosc 2015;29:3761ŌĆō3767.



7. Kwon MJ, Kang HS, Kim HT, et al. Treatment for gastric 'indefinite for neoplasm/dysplasia' lesions based on predictive factors. World J Gastroenterol 2019;25:469ŌĆō484.



8. Yim K, Shin JH, Yoo J. Novel pathologic factors for risk stratification of gastric "indefinite for dysplasia" lesions. Gastroenterol Res Pract 2020;2020:9460681.




9. Yu CH, Jeon SW, Kim SK, et al. Endoscopic resection as a first therapy for gastric epithelial atypia: is it reasonable? Dig Dis Sci 2014;59:3012ŌĆō3020.



10. Cho YS, Chung IK, Jung Y, et al. Risk stratification of patients with gastric lesions indefinite for dysplasia. Korean J Intern Med 2021;36:1074ŌĆō1082.



11. Kang DH, Choi CW, Kim HW, et al. Predictors of upstage diagnosis after endoscopic resection of gastric low-grade dysplasia. Surg Endosc 2018;32:2732ŌĆō2738.



12. Kim YJ, Park JC, Kim JH, et al. Histologic diagnosis based on forceps biopsy is not adequate for determining endoscopic treatment of gastric adenomatous lesions. Endoscopy 2010;42:620ŌĆō626.


13. Lee CK, Chung IK, Lee SH, et al. Is endoscopic forceps biopsy enough for a definitive diagnosis of gastric epithelial neoplasia? J Gastroenterol Hepatol 2010;25:1507ŌĆō1513.


14. Choi CW, Kim HW, Shin DH, et al. The risk factors for discrepancy after endoscopic submucosal dissection of gastric category 3 lesion (low grade dysplasia). Dig Dis Sci 2014;59:421ŌĆō427.



15. Kim GH. Understanding growth patterns of signet ring cell carcinoma of the stomach is necessary for successful endoscopic resection. Gut Liver 2015;9:695ŌĆō696.



16. Graham DY, Schwartz JT, Cain GD, Gyorkey F. Prospective evaluation of biopsy number in the diagnosis of esophageal and gastric carcinoma. Gastroenterology 1982;82:228ŌĆō231.


17. Jeon HK, Ryu HY, Cho MY, et al. A randomized trial to determine the diagnostic accuracy of conventional vs. jumbo forceps biopsy of gastric epithelial neoplasias before endoscopic submucosal dissection; open-label study. Gastric Cancer 2014;17:661ŌĆō668.



18. Gielisse EA, Kuyvenhoven JP. Follow-up endoscopy for benign-appearing gastric ulcers has no additive value in detecting malignancy: it is time to individualise surveillance endoscopy. Gastric Cancer 2015;18:803ŌĆō809.



19. Lee YB, Han J, Cho JH, Lee HS. Clinical outcomes of endoscopic surveillance for gastric ulcers in populations with a high prevalence of gastric cancer. Turk J Gastroenterol 2016;27:421ŌĆō427.


20. Nakamura K, Sakaguchi H, Enjoji M. Depressed adenoma of the stomach. Cancer 1988;62:2197ŌĆō2202.


21. Iishi H, Tatsuta M, Okuda S. Endoscopic diagnosis of minute gastric-cancer of less than 5 mm in diameter. Cancer 1985;56:655ŌĆō659.


22. Nam HS, Choi CW, Kim SJ, et al. Endoscopic submucosal dissection for gastric indefinite for neoplasia: which lesions should be resected? Surg Endosc 2019;33:3976ŌĆō3983.



23. Rosai J. Rosai and AckermanŌĆÖs Surgical Pathology. 9th ed. Clay County: Mosby, 2004.
24. Doyama H, Nakanishi H, Yao K. Image-enhanced endoscopy and its corresponding histopathology in the stomach. Gut Liver 2021;15:329ŌĆō337.


25. Yao K. Clinical application of magnifying endoscopy with narrow-band imaging in the stomach. Clin Endosc 2015;48:481ŌĆō490.




26. Hirasawa D, Fujita N, Yamagata T, Suzuki T, Noda Y. A case of early gastric cancer in which the degree of histological atypia was correctly predicted by magnifying endoscopy combined with narrow band imaging. Dig Endosc 2011;23 Suppl 1:92ŌĆō94.


27. Tamura N, Sakaguchi Y, Furutani W, et al. Magnifying endoscopy with narrow-band imaging is useful in differentiating gastric cancer from matched adenoma in white light imaging. Sci Rep 2022;12:8349.











