 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 23(2); 2023 > Article |
|
See editorial "Evidence-based Therapy: A Rational Approach to Helicobacter pylori Eradication" in Volume 23 on page 81.
Abstract
Background/Aims
Standard triple therapy (STT; proton pump inhibitor [PPI]+clarithromycin+amoxicillin) used for Helicobacter pylori (H. pylori) eradication has shown low treatment success rates in recent years, which is most likely attributable to increased clarithromycin resistance. In this study, we compared treatment success rates of tailored therapy (TT) using real-time polymerase chain reaction (RT-PCR) and empirical STT.
Methods
This retrospective study included 650 patients with H. pylori infection, who visited Eunpyeong St. Mary’s Hospital in Korea; 343 patients received TT based on RT-PCR assays, and 307 patients received STT. Eradication success was defined as a negative 13C-urea breath test result 4~8 weeks after treatment completion. Patients who failed first-line therapy and those with clarithromycin resistance received bismuth-containing quadruple therapy (BQT; PPI+bismuth+metronidazole+tetracycline).
Results
Intention-to-treat analysis showed that H. pylori eradication rates were higher in patients who received RT-PCR-based TT than in those who were treated using empirical STT (80.5% [190/236] vs. 70.4% [216/307], P=0.069). Per-protocol (PP) analysis showed similar results (84.4% [190/225] vs. 74.7% [216/289], P=0.007). PP analysis showed that 7-day TT treatment was associated with a higher eradication rate than that observed with 10- to 14-day STT (85.2% [178/209] vs. 73.8% [59/80], P=0.029). The clarithromycin resistance rate was 27.9% (87/312). The eradication success rate was 89.2% (74/83) in patients with clarithromycin resistance, who received BQT as first-line therapy.
대한민국에서 헬리코박터 파일로리(Helicobacter pylori, H. pylori) 감염률은 50% 내외이며[1], H. pylori 감염은 소화성 궤양, 기능성 소화불량, 특히 위암과 관련이 있어 이에 대한 적극적인 진단과 치료가 필요하다. 국가검진에서 40세 이상의 성인을 대상으로 조기위암의 선별을 위해 상부위장관 내시경을 2년에 한 번씩 시행받을 것을 권유하고 있다. 최근에 조기위암이나 고등급 위선종의 내시경 절제술 이후 H. pylori 제균 치료를 받는 것이 이시성 위암의 발생을 예방한다는 것이 확인되었고[2], 또한 1촌 관계의 위암 가족력이 있는 경우 H. pylori를 제균하였을 때 위암 발생이 감소하여 H. pylori 제균 치료의 필요성이 더욱 부각되고 있다[3,4]. 2018년부터 위암 직계 가족력, 위축성 위염, 환자가 처방에 동의하는 경우에 대해 환자 전액 본인 부담이긴 하지만 치료에 대한 적응이 확대되었다[5]. 그러나 H. pylori균의 clarithromycin 내성률이 증가함에 따라, 우리나라에서 표준 3제 요법(proton pump inhibitor [PPI]+clarithromycin+amoxicillin)의 제균 성공률은 감소하여 70% 정도이다[6,7]. Maastricht VI 가이드라인에서는 clarithromycin 내성률이 15%를 초과하면 표준 3제요법은 1차 치료로 부적절하여 사용하지 않을 것을 권고하였고[8], 이 가이드라인에 따라 clarithromycin 내성률이 높은 우리나라에서는 bismuth 포함 4제요법을 1차 치료로 선택해야 하나 이 약제를 복용할 때 부작용을 호소하는 환자들이 많고 이 치료에 실패하였을 때 다음 단계의 구제 요법이 확립되어 있지 않아 임상에서는 여전히 표준 3제요법을 경험적으로 사용하고 있는 상황이다.
Clarithromycin 내성 검출 PCR은 H. pylori 감염 여부를 확인함과 동시에 clarithromycin 내성 여부도 확인할 수 있어 표준 3제요법의 경험 치료보다 치료 성공률이 우월하다[9].2020년에 제안된 근거 기반 임상진료지침 개정안에서는 표준 3제요법을 경험적 치료로 할 경우 2주 치료를 권고하고 있다[10]. 이 연구에서는 real-time (RT)-PCR법으로 H. pylori 감염이 진단된 환자와 은 염색(silver stain)법을 기반으로 진단된 환자에서 제균 치료 성공률을 비교하였으며, 치료 기간을 7일군과 10~14일군으로 나눠서 성공률을 비교하였다.
은평성모병원에서 2019년 4월부터 2020년 6월까지 은 염색법 또는 clarithromycin 내성 검출 PCR법으로 확인된 총 680명 중 과거 치료력이 확인된 30명을 제외한 650명의 H. pylori 감염 환자를 대상으로 후향적으로 분석하였다. 20세 미만과 85세 이상인 환자는 연구에서 제외하였고, 심한 전신 질환(심장 질환, 호흡기 질환), 심한 혈소판 저하, 말기 신부전, 1년 이내 급성관동맥증후군의 병력이 있는 환자도 연구 대상에서 제외하였다. Clarithromycin 내성에 대한 점 돌연변이(A2142G 및 A2143G) 평가를 위해 RT-PCR법으로 U-TOP HPy-ClaR Detection Kit (SEASUN BIOMATERIALS, Daejeon, Korea)를 사용하였다. 은 염색법으로 H. pylori 감염이 확인된 289명의 환자와 RT-PCR법으로 확인된 312명의 환자 중 clarithromycin 내성이 없는 225명의 환자를 7~14일 동안의 표준 3제요법으로 치료하였으며, 치료 종료 후 4~8주 사이에 요소호기 검사(13C-urea breath test [POCone®; Otsuka Electronics Co., Ltd., Osaka, Japan])로 제균 성공 여부를 확인하였다. 표준 3제요법으로 제균 치료에 실패한 환자와 clarithromycin 내성으로 확인된 87명의 환자에 대해서는 bismuth 포함 4제요법(PPI+bismuth+metronidazole+ tetracyclin)으로 치료하였으며, 치료 종료 후 4~8주에 요소호기 검사로 제균 성공 여부를 확인하였다(Fig. 1). 높은 순응도는 약제를 80% 이상 복용하였을 경우로 하였고, 제균 치료약을 처방받았으나 요소호기 검사 결과가 없는 경우를 추적 탈락으로 하였다. 이 연구는 은평성모병원의 기관생명윤리위원회의 승인을 받았다(IRB No. PC21RISI0130).
통계는 SAS ver 9.4 (SAS Institute Inc., Cary, NC, USA)를 이용해서 분석하였다. 명목변수에 대해서는 chi-square test 또는 Fisher's exact test를 연속형 변수에 대해서는 independent t-test (T) 또는 Wilcoxon's rank-sum test를 이용하였다. P값 0.05 이하에 대해 통계적으로 의미 있다고 판단하였다.
총 650명의 환자에서 맞춤 치료군은 343명, 경험 치료군은 307명이었다. 49명이 요소호기 검사 결과를 알 수 없어 제외되어서, 601명 중 맞춤 치료군 312명과 경험 치료군 289명을 분석하였다. 맞춤 치료군 312명 중 clarithromycin 내성이 없는 환자(clarithromycin 비내성군)는 225명(72.1%)이었고, clarithromycin 내성이 있는 환자(clarithromycin 내성군)는 87명(27.9%)이었다. RT-PCR법으로 H. pylori 감염이 진단된 clarithromycin 비내성군에서 표준 3제요법으로 치료를 한 군(맞춤 치료군)과 은 염색법으로 확인된 환자군(경험 치료군)에서 남/여 비율, 신장, 체중, 체질량 지수, 음주력, 흡연력, 동반 질환 유무(고혈압, 당뇨병, 만성 신질환, 만성 간질환)에서 유의한 차이를 보이지 않았고, 내시경 진단에서 위염, 위궤양, 위 신생물의 비율도 유의한 차이를 보이지 않았다. 맞춤 치료군의 평균 나이가 경험 치료군보다 더 젊었다(Table 1). 맞춤 치료군(clarithromycin 비내성군[n=225])과 경험 치료군(n=289)의 1차 제균 성공률을 비교하였을 때 intention-to-treat (ITT) 분석에서 맞춤 치료군은 80.5% (95% CI, 75.5~85.6; n=190/236)였고, 경험 치료군은 70.4% (95% CI, 65.3,~75.5; n=216/307)였다(P=0.0069, Fig. 2A). Per-protocol (PP) 분석에서 맞춤 치료군은 84.4% (95% CI, 79.7~89.2; n=190/225)였고, 경험 치료군은 74.7% (95% CI, 69.7~79.8; n=216/289)였다(P=0.0074, Fig. 2B). 치료 기간에 따라 비교하였을 때 7일 치료군에서 맞춤 치료군은 85.2% (178/209)였고, 경험 치료군은 75.1% (157/209)였다(P=0.010). 10~14일 치료군을 비교하였을 때 양 군 간에 치료 성공률 차이를 보이지 않았다(75.0% [12/16] vs. 73.8% [59/80], P=1.00). 맞춤 치료 7일군과 경험 치료 10~14일군의 치료 성공률을 비교하였을 때 ITT 분석에서 81.3% (95% CI, 76.1~86.4; n=178/219)와 72.8% (95% CI, 63.2~82.5; n=59/81)였고(P=0.111, Fig. 3A), PP 분석에서 85.2% (95% CI, 80.4~90.0; n=178/209)와 73.8% (95% CI, 64.1~83.4; n=59/80)였다(P=0.024, Fig. 3B).
맞춤 치료군 중 clarithromycin 비내성군에서 표준 3제요법에 실패한 환자(n=35)와 경험 치료군에서 표준 3제요법으로 실패한 환자(n=67)의 bismuth 포함 4제요법 2차 제균 성공률을 비교하였다. 맞춤 치료군 35명 중 7명이 추적 탈락이 되었고, 경험 치료군 67명 중 4명이 추적 탈락되었다. 2차 제균 치료 성공률은 맞춤 치료군과 경험 치료군에서 통계학적인 차이가 없었다(92.9% [26/28] vs. 95.2% [60/63], P=0.614). 치료 기간을 7일과 10~14일로 세분하였을 때도 PP 분석에서 양 군 간의 통계학적인 차이는 없었다(Table 2).
Clarithromycin 내성률은 27.9% (87/312)였으며, 87명의 내성 균주의 분포를 보면 A2142G 돌연변이가 13.8% (12/87), A2143G 돌연변이가 81.6% (71/87), A2142G+A2143G 돌연변이가 4.6% (4/87)였다. 이 중 A2143G 돌연변이군에서 4명이 추적 탈락되었다. Clarithromycin 내성이 있는 환자에서 bismuth 포함 4제요법을 1차 치료로 하였을 때 제균 성공률은 89.2% (74/83)였다. 돌연변이에 따른 제균율은 A2142G군에서 75.0% (9/12), A2143G군에서 92.5% (62/67), A2142G+A2143G 군에서 75.0% (3/4)로 돌연변이군에 따른 제균율의 차이는 없었다(P=0.104, Table 3). 기간에 따른 제균율에서 7일군은 83.3% (25/30)였고, 10~14일군에서 92.5% (49/53)로 통계학적인 차이는 없었다(P=0.273).
이 연구에서는 RT-PCR법으로 맞춤 치료를 하였을 때 경험 치료보다 H. pylori 제균 성공률이 높음을 확인하였다. 특히, 최근 가이드라인에서 권고하는 2주 동안의 clarithromycin을 포함한 경험적 표준 3제요법[10]과 RT-PCR로 clarithromycin에 내성이 없는 환자를 1주일 맞춤 치료를 비교하였을 때 1주 동안의 맞춤 치료가 2주 동안의 경험 치료보다 제균 성공률이 우수하였음을 보여주었다. 지난 10년 동안 clarithromycin의 내성률은 점차 증가해왔고, 최근 연구에서도 clarithromycin 내성률은 17.8~31.0%였다[6,11]. 국내 연구를 분석한 메타분석에서도 clarithromycin을 포함한 표준 3제요법의 제균 성공률은 점점 감소하고 있어, 감수성 검사를 기반으로 하는 맞춤 치료를 권유하고 있다[12]. 우리 연구에서도 clarithromycin 내성이 28% 정도로 높음을 확인하여 표준 3제요법을 경험적으로 사용하기에는 무리가 있다고 생각한다. 2주 동안으로 치료 기간을 늘리는 것이 제균 성공률을 높일 수 있느냐가 관건인데, 최근 연구의 국내 표준 3제요법의 제균 성공률은 1주 치료와 2주 치료를 비교하였을 때 PP 분석에서 78.5%와 79.7%였고 ITT 분석에서 64.0%와 66.0%로[13], 치료 기간을 늘려서 얻는 장점을 기대하기는 어려울 것으로 보인다. 이것을 대신할 1차 치료로 bismuth를 포함하지 않는 순차 치료 또는 동시 치료를 고려할 수 있으나 성공률이 만족스럽지 않고, 1차 치료에 실패하였을 때 그 다음의 구제요법이 아직 정립되지 않은 상황이라 표준 3제요법을 여전히 일선 진료 현장에서 많이 사용하고 있는 실정이다. 은 염색 또는 Giemsa 염색법에서 양성이 확인되었을 때 추가로 clarithromycin 내성 검출 PCR법을 통해 clarithromycin 내성 여부를 확인하여 맞춤 치료를 하는 것이 치료의 성공률을 높을 수 있을 것이다[10,14]. 또한, 최근 연구에서는 맞춤 치료의 비용-효과가 우월함을 보여주었고[7,15], 제균 치료 실패에 따른 2차 약 복용을 줄일 수 있다는 장점도 기대할 수 있다. 우리 연구에서 clarithromycin 내성 중 A2143G가 82%로 90%를 보인 국내 연구와 비슷하였고[11] bismuth 포함 4제요법을 통한 치료 성공률도 A2143G 돌연변이가 A2142G 돌연변이보다 높아서 A2143G 돌연변이를 가지고 있는 내성 환자의 경우에는 치료 성공의 가능성이 높음을 예상할 수 있다. 이 연구의 단점은 후향적인 연구라는 것이다. 그러나 항생제 내성 검사를 통한 맞춤 치료와 경험 치료를 비교하는 연구는 전향적으로 시행하기가 쉽지 않고, 오히려 이 연구는 진료의사의 선호도에 따라 경험 치료와 맞춤 치료를 하였던 기록을 통한 결과이므로 현재 일선 현장에서의 헬리코박터의 치료 성공률을 잘 반영한다고 할 수 있다. 또한, 맞춤 치료를 하였음에도 치료 성공률이 90%에 이르지 못한 것은 clarithromycin 내성 점 돌연변이가 다양하지만[16], 이 연구에서 사용된 clarithromycin 내성 검출 PCR법으로 A2143G와 A2142G의 2개의 돌연변이만 알아낼 수 있기 때문으로 생각한다.
우리 연구에서는 65세를 기준으로 나이에 따른 치료 성공률의 차이를 조사하였는데, 65세 이상에서는 65세 미만과 치료 성공률의 차이는 없었다. 고령의 환자는 항생제 내성이 있을 가능성이 높아 더욱 맞춤 치료가 필요하다고 예상했으나 맞춤 치료와 경험 치료 사이에 차이는 없었다. 대상 환자수가 많지 않았기 때문에 65세 이상의 환자를 대상으로 한 연구가 필요하겠다.
현재 clarithromycin의 내성률이 높은 상황에서 표준 3제요법의 1주 치료는 성공률이 높지 않으므로 다른 접근이 필요하다. 2주로 치료 기간을 늘리는 것이 clarithromycin의 내성률이 높은 현 상황을 만족스럽게 해결하지는 못할 것 같다. 또한, 우리 연구에서 보여주었듯이 bismuth 포함 4제요법을 바로 1차 치료로 하기에는 부작용의 빈도가 높아, 제균 치료를 통한 위암 발생 예방이라는 국민건강증진의 목표를 이루기는 어렵다. 이 연구는 내성 검사를 통해 1주일의 표준 3제요법 치료가 현재 가이드라인에서 제시하는 1주일보다 긴 기간의 경험적 치료보다 높은 치료 성공률을 보여줌으로써, 내성 검사를 통한 맞춤 치료가 효과적이라는 사실을 확인하였다. 현재 제균 치료의 허가 사항도 확대되고 있고, 위선종의 내시경 치료 후에도 요양급여가 적용되는 등 헬리코박터 진단과 치료에 대한 요양급여가 확대되고 있다. 그러나 진단과 치료에 대한 요양급여의 적용이 달라 여전히 일선 의사들이 헬리코박터를 치료하는 데 혼란스러운 상황이다[5]. 또한 요소호기 검사의 수가를 현실화하여 의사들이 치료 후 적극적인 결과 확인을 환자가 편하게 받을 수 있도록 유도하는 정책이 필요하겠다. 결론적으로 우리 연구는 내성 검사를 통한 7일 맞춤 치료가 10~14일 동안의 경험 치료보다 치료 성공률이 우수함을 보여주었다. Clarithromycin 내성 검출 PCR법을 기반으로 한 맞춤 치료는 clarithromycin 내성 균주에 대해 불필요한 표준 3제요법의 치료를 막게 되어 항생제 남용을 방지할 수 있다. Clarithromycin 비내성 균주의 경우 기존 가이드라인의 14일 치료에 비해 짧은 치료 기간으로도 우월한 제균 성공률을 보였기 때문에, 이 연구를 통해 내성 검사에 대한 요양급여의 확대와 요소호기 검사의 적절한 수가 개정을 통해 일선 현장에서 제균 치료로 위암의 1차 예방을 하고 있는 의사들이 더 적극적으로 헬리코박터를 치료하여 국민의 위암 발생률이 감소할 수 있기를 기대한다.
Fig. 1.
Flowchart of the study. H. pylori, Helicobacter pylori; RT-PCR, real-time polymerase chain reaction; PPI, proton pump inhibitor.
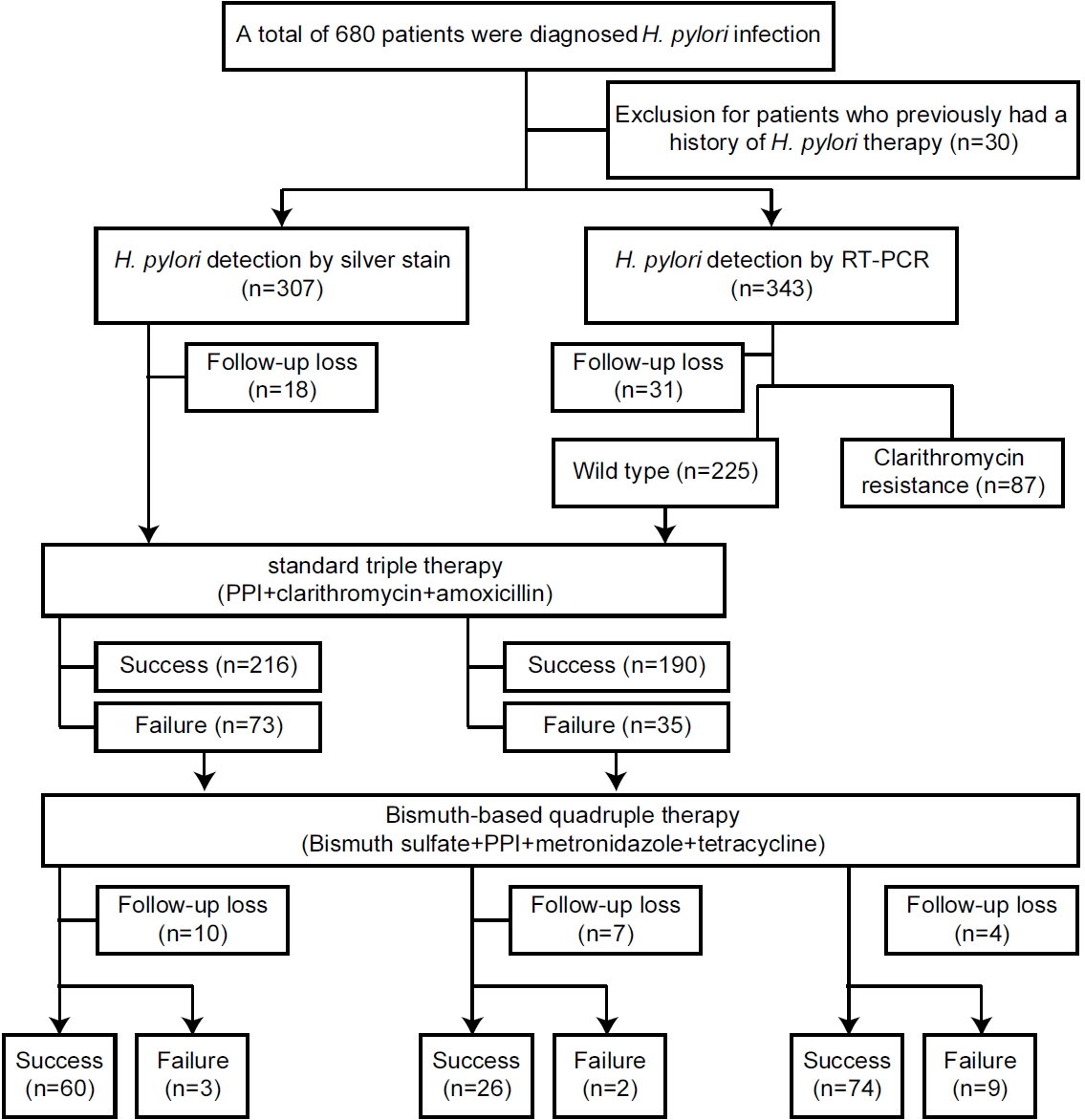
Fig. 2.
Comparison of eradication rates between the tailored therapy (TT) and empirical therapy (ET) groups based on ITT analysis (A) and PP analysis (B). ITT, intention-to-treat; PP, per-protocol. *P < 0.05.
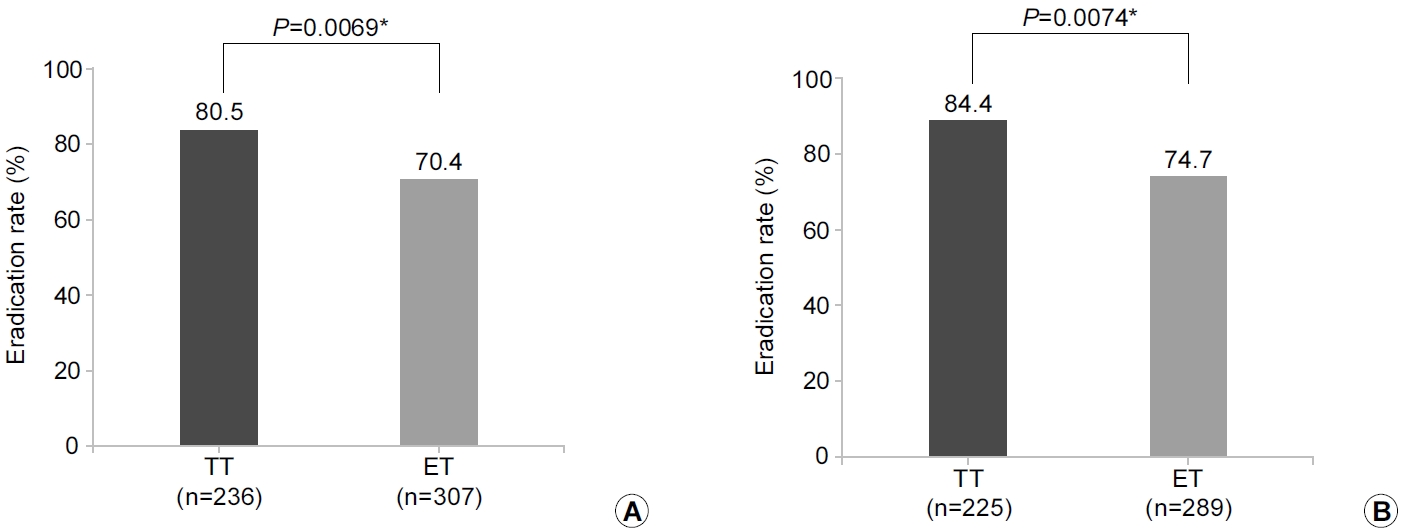
Fig. 3.
Comparison of eradication rates between the 7-day tailored therapy (TT) and 14-day empirical therapy (ET) groups based on ITT analysis
(A) and PP analysis (B). ITT, intention-to-treat; PP, per-protocol. *P < 0.05.

Table 1.
Baseline Characteristics
Table 2.
Eradication Rates Following Bismuth-based Quadruple Therapy
Table 3.
Eradication Rates Associated with Bismuth-based Quadruple Therapy Used as First-line Therapy in Patients with Clarithromycin Resistance Based on the 23S Ribosomal RNA Point Mutations
REFERENCES
1. Kim SY. Time trends in the prevalence of Helicobacter pylori infection and future directions in Korea. Korean J Helicobacter Up Gastrointest Res 2016;16:123-128.


2. Choi IJ, Kook MC, Kim YI, et al. Helicobacter pylori therapy for the prevention of metachronous gastric cancer. N Engl J Med 2018;378:1085-1095.


3. Choi IJ, Kim CG, Lee JY, et al. Family history of gastric cancer and Helicobacter pylori treatment. N Engl J Med 2020;382:427-436.


4. Park CH. Helicobacter pylori eradication and gastric cancer prevention. Korean J Helicobacter Up Gastrointest Res 2021;21:267-274.


5. Kim YI, Choi IJ. Criteria for the national health insurance service medical care benefit of Helicobacter pylori treatment. Korean J Helicobacter Up Gastrointest Res 2022;22:235-239.


6. Lee JH, Ahn JY, Choi KD, et al. Nationwide antibiotic resistance mapping of Helicobacter pylori in Korea: a prospective multicenter study. Helicobacter 2019;24:e12592.



7. Cho JH, Jeon SR, Kim HG, Jin SY, Park S. Cost-effectiveness of a tailored Helicobacter pylori eradication strategy based on the presence of a 23S ribosomal RNA point mutation that causes clarithromycin resistance in Korean patients. J Gastroenterol Hepatol 2019;34:700-706.

8. Malfertheiner P, Megraud F, Rokkas T, et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report. Gut 2022;71:1724-1762.

9. Lee HJ, Kim JI, Cheung DY, et al. Eradication of Helicobacter pylori according to 23S ribosomal RNA point mutations associated with clarithromycin resistance. J Infect Dis 2013;208:1123-1130.


10. Jung HK, Kang SJ, Lee YC, et al. Evidence-based guidelines for the treatment of Helicobacter pylori infection in Korea: 2020 revised edition. Korean J Helicobacter Up Gastrointest Res 2020;20:261-287.


11. Kim SY, Park JM, Lim CH, et al. Types of 23S ribosomal RNA point mutations and therapeutic outcomes for Helicobacter pylori. Gut Liver 2021;15:528-536.



12. Kang SJ, Jung HK, Lee YC, et al. Eradication rates of clarithromycin triple therapy in Korea: a systematic review and meta-analysis. Korean J Helicobacter Up Gastrointest Res 2021;21:35-47.


13. Kim TH, Park JM, Cheung DY, Oh JH. Comparison of 7- and 14-day eradication therapy for Helicobacter pylori with firstand second-line regimen: randomized clinical trial. J Korean Med Sci 2020;35:e33.




14. Park H, Lee JH. Recent trends in tailored treatments for Helicobacter pylori infection. Korean J Helicobacter Up Gastrointest Res 2021;21:115-121.


-
METRICS

-
- 1 Crossref
- 1,601 View
- 57 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
What Is the Optimal Drug Regimen for Helicobacter pylori Eradication Therapy?2024 June;24(2)
Is Helicobacter pylori Infection Associated With Ulcerative Colitis Activity?2024 March;24(1)
Can Helicobacter pylori Infection Reduce the Efficacy of Cancer Immunotherapy?2023 December;23(4)
The Recurrence of Helicobacter pylori Infection: Recrudescence Versus Reinfection2023 December;23(4)






