|
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 22(1); 2022 > Article |
|
Abstract
Gastric subepithelial tumors (SETs) are often discovered incidentally and are usually benign. Their subepithelial location complicates accurate diagnosis; however, most lesions can be differentiated using either endoscopy or endoscopic ultrasonography. Gastric SETs location, color, surface change, size, consistency, and movability are evaluated during endoscopy. Endoscopic ultrasound assesses their originating layer, echogenicity, and homogeneity. Common gastric SETs in Koreans include ectopic pancreas, lipoma, leiomyoma, other benign lesions, neuroendocrine tumors, and gastrointestinal stromal tumors with malignant potential. Furthermore, extraluminal compression by normal organs or benign lesions as well as other malignant tumors may have a similar appearance to gastric SET. Understanding the endoscopic and endoscopic ultrasound characteristics of common gastric subepithelial lesions can reduce the rate of unnecessary examinations and excessive treatment. In this article, these characteristics are reviewed through various images that are common in the Korean population.
위의 상피하 병변(subepithelial lesion)은 병변이 상피(epithelium)보다 하부에 위치하고 주위와 동일한 상피로 덮여 있으면서 내강으로 융기된 병변을 총칭한다. 상피하 병변 중에 위 압박을 제외한 병변들을 위 상피하 종양(subepithelial tumors, SETs)이라 표현할 수 있다. 상피하 종양은 점막근층(muscularis mucosa)에서부터 그 아래쪽에서 발생하는 종양을 이르는데, 점막하 종양(submucosal tumor)으로 불리기도 했지만 점막하층 외에서 발생하는 종양들이 더 많아 상피하 종양이라는 용어가 보다 적절하다. 국내 연구에서는 8만여 명의 검진 내시경 환자들을 대상으로 조사하였을 때 상부 위장관 전체에서 상피하 종양은 1.94%, 위 상피하 종양은 0.74%로 보고하였다[1]. 위 상피하 종양은 무증상인 상태로 검진 내시경 혹은 다른 목적으로 시행하는 검사 중에 발견되는 경우가 대부분이며, 이렇게 발견된 상피하 종양은 대부분 양성 병변이고 일부에서 위장관간질 종양(gastrointestinal stromal tumor, GIST), 신경내분비 종양(neuroendocrine tumor, NET), 림프종(lymphoma), 점막하 종양 유사 위암(SET like adenocarcinoma)과 같은 악성 병변이 발견될 수 있다[2]. 위 상피하 종양의 자연경과는 명확하게 알려져 있지 않지만, 국내 연구에 의하면 대부분 10 mm 미만의 크기이고 이중에서 3.6~8.5%의 환자에서 경과 관찰 중에 크기 변화를 보였다[1,3,4]. 하지만 위 상피하 종양은 정상 상피 아래에 위치하기 때문에 정상점막으로 덮인 융기성 병변으로 대부분 발견되고, 상피 아래에 위치함으로 해서 내시경 겸자 생검만으로는 조직의 진단이 어려워 진단 내시경만으로는 감별진단에 어려움이 있다. 본 종설에서는 한국인에서 흔한 위 상피하 종양의 진단을 다양한 내시경 사진들과 함께 검토해 보겠다.
위 상피하 종양은 주위 점막과 동일한 점막으로 덮여 융기를 이루는 형태로 일반적으로 내시경 육안 사진만으로는 감별 진단이 어려우나 여러 내시경 소견을 기초로 환자의 향후 처치 계획을 정하는 데 도움을 받을 수 있기 때문에 면밀한 관찰이 필요하다. 내시경 검사에서 상피하 종양을 관찰할 때는 기본적으로 위치, 색조, 크기, 표면의 변화, 단단한 정도, 이동성을 평가한다.
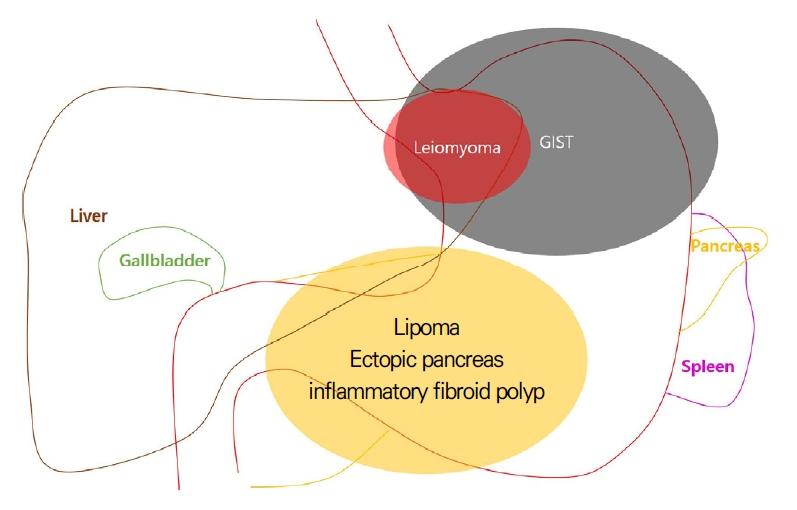
상피하 종양은 위의 어디에서든 발생할 수 있으나 상피하 종양의 종류에 따라 호발하는 부위가 있다. 위장관간질 종양, 평활근종은 궁륭부, 분문부를 포함한 상부 체부에 주로 발생하며, 그중에서도 평활근종은 분문부에 가장 호발한다. 전정부에서는 이소성 췌장, 지방종, 염증성 섬유양 용종(inflammatory fibrinoid polyp)이 호발한다[5]. 신경내분비 종양의 경우 1형은 위축성 위염의 분포와 비슷하게 체부 소만에 호발하며 3형은 위의 어느 부위에서나 발생할 수 있다[6]. 외부 압박 역시 장기의 위치에 따라 추정할 수 있는데 간으로 인한 압박은 체부 전벽과 소만으로, 췌장과 비장의 압박은 체부 후벽과 대만으로 관찰되며 담낭은 확장되면 전정부 전벽으로 압박이 관찰된다(Fig. 1).
상피하 종양은 주변과 동일한 상피로 덮여 있어 대부분 색조의 차이가 없다(Fig. 2A). 하지만 일부 상피하 종양은 색조의 차이를 보여 감별 진단에 도움이 될 수 있다. 대표적으로 지방종이 황색조를 보이며(Fig. 2B) 지방종 외에도 과립세포종(granular cell tumor)이나 신경내분비 종양도 황색조를 보일 수 있다. 단순낭종(cyst), 중복낭종(duplication cyst), 림프관종(lymphangioma), 심재성 낭종성 위염(gastritis cystica profunda) 같은 낭성 병변들은 투명하게 보이며(Fig. 2C) 정맥류나 혈관종은 투명한 청색으로 관찰될 수 있다(Fig. 2D).
상피하 종양은 상피보다 아래에서 발생하기 때문에 갑작스러운 크기 증가나 상피 바로 아래의 점막 근층에서 발생하여 상피에 영향을 주는 경우가 아니면 표면의 변화가 없다. 하지만 일부에서 표면의 변화를 보일 수 있고 이는 상피하 종양의 감별 진단에 도움이 될 수 있다. 대표적으로 이소성 췌장의 경우 표면에 개구부(opening)나 함몰(umbilication, dimpling)이 동반되어 진단에 큰 도움이 된다(Fig. 2E, F). 염증성 섬유양 용종이나 심재성 낭종성 위염의 경우 발생 기전이 만성 자극과 관련이 있어 표면의 변화가 동반된 경우가 흔하다(Fig. 2G, H) [7,8]. 표면에 발적이나 궤양 같은 깊은 변화가 보이는 경우 신경내분비 종양(Fig. 2I)이나 위장관간질 종양(Fig. 2J) 같은 악성의 가능성을 가지는 상피하 종양의 가능성이 있다. 상피하 종양에서 표면의 변화가 보이는 경우 악성의 가능성도 있고 내시경 겸자 생검에서 조직학적인 진단이 될 가능성이 있어 낭종이나 혈관이 의심되지 않으면 단순 내시경 조직 검사를 고려해야 한다.
상피하 종양의 크기는 치료 방침 결정이나 추가 검사나 추적 내시경 검사 시기를 결정하는 데 매우 중요한 요소이다. 상피하 종양은 상피 속에 매몰되어 있고 병변과 내시경의 거리와 각도에 따라 크기가 다르게 보여 육안적 크기 측정은 부정확하다. 하지만 생검 겸자를 이용하여 크기를 유추할 수 있다. 제품에 따라 다르겠지만 생검 겸자는 닫았을 때는 대략 2 mm, 최대한 열었을 때는 제품마다 다르나 5~7 mm 정도의 크기이다(Fig. 3A, B). 한 전향적 연구에서 생검 겸자를 벌렸을 때 크기와 내시경 초음파로 측정한 크기를 비교하였을 때 강한 상관관계(r=0.88)를 보였다[9]. 상피하 종양이 분문부나 체부 소만에 위치할 경우 내시경을 반전하여 내시경의 직경이나 내시경 자체에 표시되어 있는 눈금으로 크기를 가늠해 볼 수 있겠다(Fig. 3C, D). 하지만 크기가 20 mm 이상이거나 위장관간질 종양이나 신경내분비 종양 같은 악성의 가능성이 있는 병변이 의심될 때는 복부 전산화단층촬영이나 내시경 초음파를 이용한 정확한 크기 측정이 필요하다. 20 mm 미만의 정상점막으로 덮혀 있는 위 상피하 종양은 주기적인 내시경 검사 또는 초음파내시경을 검사를 통해서 치료 방향을 결정할 수 있으나, 크기가 20 mm 이상이거나 크기가 작더라도 악성이 의심되는 변화가 있는 경우(크기 증가, 표면의 발적, 표면의 궤양)에는 내시경 초음파 유도하 세침 생검이나 점막 절개술 같은 방법을 이용하여 적극적인 조직 검사가 권고된다[10,11]. 악성의 가능성이 높거나 추적 검사 중에 크기 증가가 보이면 적극적인 절제술을 고려한다.
생검 겸자를 이용하여 상피하 종양을 눌러 딱딱한 정도 및 이동성을 평가할 수 있다. 대표적으로 상피하 종양을 눌렀을 때 모양이 쉽게 변형되어 함몰되는 경우(pillow sign 혹은 cushion sign)에는 지방, 액체, 림프액과 같은 부드러운 성상의 물질로 구성되어 있다고 판단할 수 있으며 지방종, 중복 낭종, 심재성 낭종성 위염, 림프관종 등에서 관찰된다(Fig. 3E). 반면 생검 겸자로 눌렀을 때 단단하여 함몰되지 않는 경우에는 대신 밀었을 때 움직이는 소견(rolling sign)으로 가동성을 평가할 수 있고 rolling sign이 양성이면 종양이 점막근층이나 점막하층에 위치함을 의미한다(Fig. 3F). 하지만 rolling sign은 상피하 종양은 고정되어 있고 표면의 점막만 움직이는 경우와 혼동되기 쉽고 종양이 고유근층에 넓게 부착된 경우에도 음성이다. 생검 겸자로 상피 부분을 잡아 올렸을 때 상피만 들어 올려지며 종양과 분리되는 소견(tenting sing)도 상피하 종양이 점막근층이나 그 아래층에 위치함을 의미한다(Fig. 3G). 하지만 tenting sign은 상피하 종양에 섬유화가 있거나 크기가 증가하여 상피까지 침범하는 경우에는 음성이다.
내시경 초음파 검사는 외부 압박 병변과 상피하 종양의 감별의 정확도가 90% 이상이고 발생 층과 에코 양상의 감별의 정확도는 80% 정도로 비교적 높다[9,12]. 그러나 내시경 초음파는 관찰자 간의 진단 일치도가 낮고, 특히 점막하층과 고유근층에 위치하는 저에코성 병변에서는 병리학적 진단과 비교하여 정확도가 43% 정도로 더욱 낮은 것으로 알려져 있다[9,13].
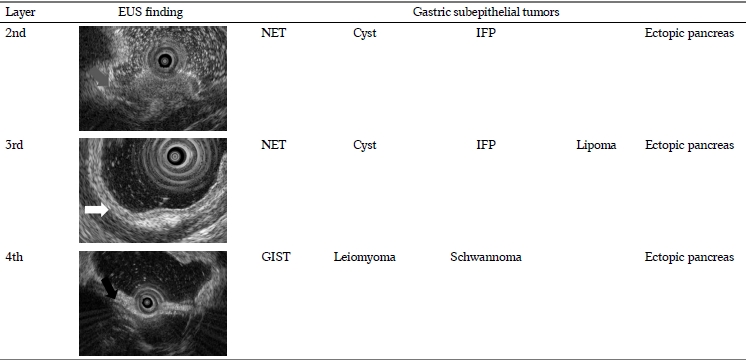
위 벽의 층에 따라 빈발하는 상피하 종양이 달라 내시경 초음파를 이용하여 어느 층에서 종양이 발생하였는지를 확인하면 감별 진단의 범위를 좁힐 수 있다. 하지만 호발하는 층이지 절대적으로 발생하는 층은 아니며 종양의 성장에 따라 여러 층을 함께 침범하는 경우도 있어 주의해야 한다. 일반적으로 내시경 초음파에서 위벽은 5개 층으로 관찰되는데 두 번째 층인 저에코의 점막근층에 위치하는 상피하 종양에는 신경내분비 종양, 염증성 섬유양 용종, 림프관종, 낭종성 병변들이 있다. 세 번째 층인 고에코의 점막하층에 주로 위치하는 상피하 종양에는 지방종, 이소성 췌장이 대표적이며 신경내분비 종양, 염증성 섬유양 용종, 낭종성 병변들은 2층과 3층 둘 다에 위치할 수 있다. 신경내분비 종양은 주로 점막하층에서 기원하여 점막근층으로 침범하는 형태이다. 네 번째 층인 저에코의 고유 근층에 위치하는 상피하 종양에는 평활근종, 위장관간질 종양, 신경초종(schwanomma) 등의 감별이 필요하다. 이소성 췌장은 점막하층에 주로 위치하지만 2, 3, 4층 모두에 위치할 수 있다(Table 1).
내시경 초음파에서 에코의 반향 정도는 무에코(anechoic), 저에코(hypoechoic), 동등에코(isoechoic), 고에코(hyperechoic)로 나누어 평가할 수 있다. 물 성분이 내시경 초음파에서 무에코로 관찰되며, 저에코는 고유근층, 동등에코는 정상 간 그리고 고에코는 점막하층 정도의 에코로 비교할 수 있겠다. 내시경 초음파에서 무에코를 보이는 상피하 종양에는 낭종성 병변들과 림프관종이 있겠으며 고에코를 보이는 상피하 종양에는 지방종이 있겠다. 그 외 나머지 대부분의 상피하 종양들은 저에코를 보인다(Table 2).
내시경 초음파에서 에코의 균질성은 상피하 종양의 구성 성분들에 따라 동일한 성분으로 구성되어 있으면 균질한(homogeneous) 에코를 보이며 낭종성 병변들, 림프관종, 평활근종, 지방종이 균질하게 관찰된다. 구성 성분이 다양한 성분으로 되어 있으면 불균질한(heterogeneous) 에코를 보이며 이소성 췌장, 염증성 섬유양 용종 등이 대표적이다. 위장관간질 종양의 경우 저위험도(low risk) 종양은 균질하게, 고위험도(high risk) 종양은 불균질하게 관찰된다(Table 2).
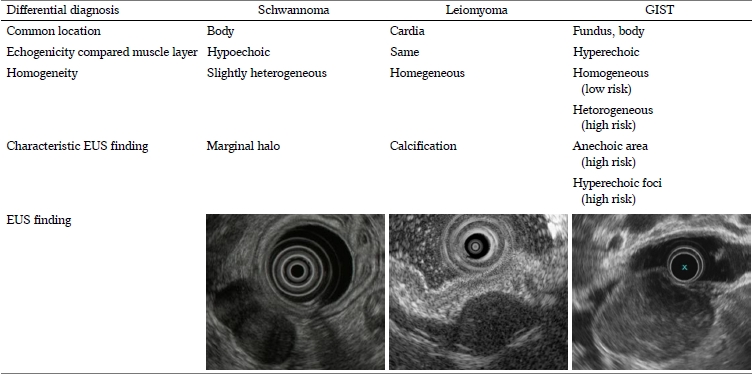
내시경 초음파로 상피하 종양의 진단에 있어 가장 어려우면서 중요한 점은 고유근층의 저에코 종양들의 감별이다. 이 병변들은 내시경 초음파 진단의 정확도가 낮으며 악성인 위장관간질 종양이 포함되어 있어 감별이 중요하다. 고유근층의 저에코 병변은 대표적으로 평활근종, 신경초종(schwannoma), 위장관간질 종양 있다. 먼저 내시경 초음파에서 네 번째 층인 고유근층을 비교할 수 있는데 평활근종은 고유근층과 같은 에코로 자연스럽게 연결되는 소견이며 신경초종은 고유근층보다 더 저에코로, 위장관간질 종양은 보다 더 고에코로 관찰된다. 그리고 평활근종과 신경초종은 균질한 에코로 관찰되나 위장관간질 종양은 크기가 크거나 악성도가 높을수록 불균질하게 관찰된다. 그 외에도 신경초종은 종양의 경계가 비치는 듯한 소견(marginal halo), 평활근종은 내부에 석회화(calcification), 위장관간질 종양은 악성도가 높아 질수록 무에코 영역(anechoic area)이나 고에코 점(hyperechoic foci)이 관찰될 수 있다(Table 3).
각각 종양들의 발생 빈도에 대한 정확한 연구는 없으나 국내 임상에서 흔하게 관찰되는 상피하 종양들로는 양성 병변인 이소성 췌장, 지방종, 평활근종과 악성의 가능성이 있으면서 비교적 흔하게 접할 수 있는 신경내분비 종양, 위장관간질 종양을 꼽을 수 있겠다.
위의 이소성 췌장은 전정부와 하부 체부에 주로 발생하고 크기는 다양하며 표면에 개구부가 관찰되는 경우가 종종 있는데(Fig. 4A) 생검 겸자로 누를 때 부드럽게 느껴지나 지방종 정도로 쉽게 눌러지지는 않는다. 내시경 초음파에서 주로 3층에서 기원하는 불균질한 저에코로 관찰되며 경계가 불명확하여 침습적인 악성 종양처럼 관찰될 수도 있으나 관이나 낭성 형태의 무에코로 관찰되는 췌관 구조가 특징적이다(Fig. 4B). 보통 특별한 치료없이 내시경 추적 관찰을 하나 드물게 염증, 출혈이 발생하거나 아주 드물게 악성의 보고가 있어 절제가 필요한 경우도 있다.
위의 위장관간질 종양은 궁륭부를 포함한 상체부에 주로 발생하며 크기는 다양하며 크기가 커질수록 악성의 위험도가 높아진다. 대부분 정상점막으로 덮여 있으나(Fig. 4G) 크기가 커지거나 진행하면 표면에 미란이나 궤양이 발생할 수 있다. 내시경 초음파에서 대부분 4층에서 기원하며 저위험도 위장관간질 종양은 비교적 균질한 저에코로 관찰되어 평활근종과 감별이 어려우나 고위험도 위장관간질 종양은 불균질한 에코와 무에코 영역이 관찰되며 불규칙한 변연 소견이 관찰된다(Fig. 4H). 위장관간질 종양의 내시경 초음파에서 3 cm 이상의 크기, 불균질한 에코, 내부에 무에코 혹은 고에코 영역의 포함, 변연의 불규칙성은 악성 고위험 소견들이다[14,15].
위 신경내분비 종양은 1형은 위축성 위염의 분포와 비슷하게 체부 소만에 호발하며 3형은 위의 어느 부위에서나 발생할 수 있다[6]. 1형은 1 cm 미만으로 다발성으로 관찰될 수 있으며 3형은 2 cm 이상의 큰 단일 병변으로 관찰될 수 있다[16]. 점막하층이나 점막근층에서 기원해서 점막으로 침범하는 경우에 표면에 발적이나 미란을 동반할 수 있다(Fig. 4I). 내시경 초음파에서 2층과 3층에 위치한 균질한 저에코로 관찰되며 경계는 비교적 명확한 편이다(Fig. 4J). 위 신경내분비 종양에서 내시경 초음파는 내시경 절제 전에 침윤 깊이를 파악하는 데 필요하다. 1형 혹은 2형 위 신경내분비 종양이 림프절 전이 소견이 없고 2 cm 이하이면서 점막하층에 국한되어 있을 때 내시경 절제를 권고하고 있다[17].
외부 압박들은 상피하 종양은 아니나 임상에서 흔히 관찰될 수 있다. 외부 압박은 상피하 종양에 비해 경계가 모호한 완만한 경계의 융기성 병변으로 관찰되며 상피하 종양들에 비해 크기가 크고 넓은 편이다. 환자의 자세 변경, 호흡, 공기주입에 따라 병변이 소실되거나 위치가 변할 수 있으며 혈관성 구조물인 경우 박동성이 관찰된다. 가장 흔하게 관찰될 수 있는 위를 압박하는 정상 장기는 간과 비장으로 간의 압박은 보통 체부 전벽과 소만으로(Fig. 5A, B), 비장의 압박은 체부 후벽과 대만으로 관찰된다(Fig. 5C, D). 담낭은 정상적으로 위를 압박하지 않으나 확장이 되면 전정부 혹은 하체부 전벽으로 압박할 수 있다. 그 외 흔하게 양성이면서 위를 압박하는 병변들에는 간좌엽의 낭종이 궁륭부나 상체부를 압박할 수 있고(Fig. 5E, F) 비장 혈관이 상체부 대만에서 관찰될 수 있으며(Fig. 5G, H) 췌장 가성 낭종이 체부 후벽을 압박할 수 있다(Fig 5I, J).
상피하 종양은 아니지만 악성 종양이 상피하 종양의 형태로 관찰되는 경우도 종종 마주치게 된다. 상피하 종양 형태의 조기 위암이나 진행성 위암이 있고(Fig. 6A, B) 이때는 조직 검사에서 음성으로 나오기도 하며 위장관간질 종양이나 신경내분비 종양과 같은 악성 상피하 종양과 감별이 어렵기도 하다. 상피하 종양 형태의 위 말트림프종(gastric MALT lymphoma)이 있으며(Fig. 6C) 내시경 초음파에서 특징적인 격자 모양의 망 형태가 관찰될 수 있다(Fig. 6D). 그 외 간암, 췌장암 같이 위에 인접한 장기의 암이 위에서 상피하 종양의 형태로 관찰될 수 있고(Fig. 6E, F) 다른 장기의 암이 위 내부나 위에 인접한 부위로 원격 전이를 하면 상피하 종양 형태로 관찰되기도 한다(Fig. 6G, H).
위 상피하 종양은 거의 대부분이 증상없이 우연히 발견되며 발견된 상피하 종양도 조직 검사를 통한 확진이나 제거없이 추적 관찰만 요하는 양성 병변들이 많다. 이런 양성 병변임을 판단할 수 있도록 각각 위 상피하 종양들의 특징들을 숙지하고 다수의 위 상파하 종양들을 내시경이나 내시경 초음파로 관찰하는 경험이 필요하다. 내시경에서 위치, 색조, 크기, 표면의 변화, 경도 및 가동성을 평가하고 내시경 초음파를 할 수 있다면 발생층, 에코의 반향 정도, 에코의 균질성을 평가하여 최대한 감별 진단을 할 수 있도록 노력하면 과도한 검사를 줄일 수 있고 침습적인 조직 검사나 불필요한 수술을 피할 수 있다. 상피하 종양처럼 보일 수 있는 정상 장기나 양성 병변들로 인한 외부 압박에 의한 소견을 알고 있다면 불필요한 검사들을 줄일 수 있고 드물지만 상피하 종양처럼 보일 수 있는 악성 종양을 인지하고 있다면 내시경 검사만으로도 추정할 수 있다. 진단이 어려울 때는 조직 검사를 통해서 진단 및 향후 절제의 필요성을 결정할 수도 있다.
Fig. 2.
Colors and surface changes of gastric subepithelial tumors. (A) Normal color; leiomyoma, (B) yellowish color; lipoma, (C) translucent; cyst, (D) bluish color; hemangioma, (E) opening; ectopic pancreas, (F) dimpling; ectopic pancreas, (G) erosion; inflammatory fibroid polyp, (H) nipple like projection; gastritis cystica profunda, (I) erythema; neuroendocrine tumor, (J) ulcer; gastrointestinal stromal tumor.

Fig. 3.
Size, consistency, and movability of gastric subepithelial tumors. (A, B) Size measurement of a subepithelial tumor using biopsy forceps. It is about 5 mm in size when the forceps is opened. (C, D) Size measurement of a subepithelial tumor using endoscopic shaft. A line is displayed every 5 cm in the endoscope. (E) The subepithelial tumor is easily pressed when compressed using biopsy forceps (pillow sign). (F) The subepithelial tumor moves easily when pushed using biopsy forceps (rolling sign). (G) When the tip of the subepithelial tumor is grasped using biopsy forceps, the epithelium is easily separated from the tumor (tenting sign).
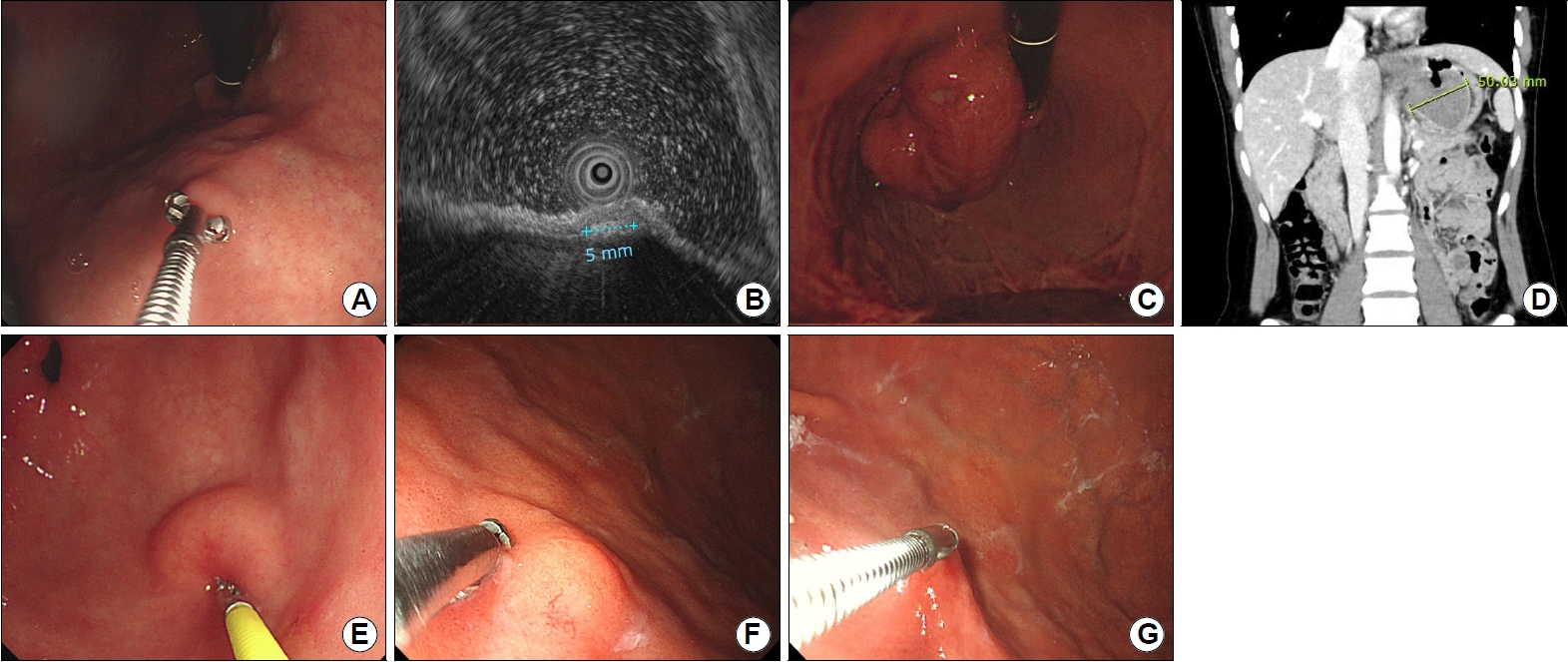
Fig. 4.
Common subepithelial tumors in Koreans. (A) A soft subepithelial tumor 20 mm (yellow arrow) in size is observed on the greater curvature of the antrum. A depression is observed in the center of the lesion. (B) On endoscopic ultrasound, a heterogeneous, mixed-echoic lesion is located in the third submucosal layer. Anechoic dots and lines (green arrow) considered ducts are observed within the tumor. (C) A soft subepithelial tumor 9 mm (white arrow) in size is observed on the greater curvature of antrum. (D) On endoscopic ultrasound, a homogeneous, intensive hyperechoic lesion with distinct border is located in the third submucosal layer. (E) A hard subepithelial tumor 8 mm (black arrow) in size is observed on the posterior wall of the upper body. (F) On endoscopic ultrasound, a homogeneous, hypoechoic, oval lesion that seems thickened by connecting the fourth proper muscle layers is observed. (G) A hard mass with a size of 70 mm (blue arrow) is observed on the greater curvature of the upper body. (H) On endoscopic ultrasound, a heterogeneous, hypoechoic lesion is observed originating from the fourth layer. The tumor has irregular borders and contains anechoic lesions. (I) A hard subepithelial tumor with a size of 7 mm (red arrow) is observed on the greater curvature of the mid-body. Erythema is observed on the surface of the lesion. (J) On endoscopic ultrasound, a heterogeneous, hypoechoic lesion is seen located in the second and third layer.

Fig. 5.
Extraluminal compressions of normal organs and benign lesions. (A, B) Liver, (C, D) spleen (purple arrow), (E, F) hepatic cyst, (G, H) splenic artery (red arrow), (I, J) pancreatic pseudocyst (green arrow).
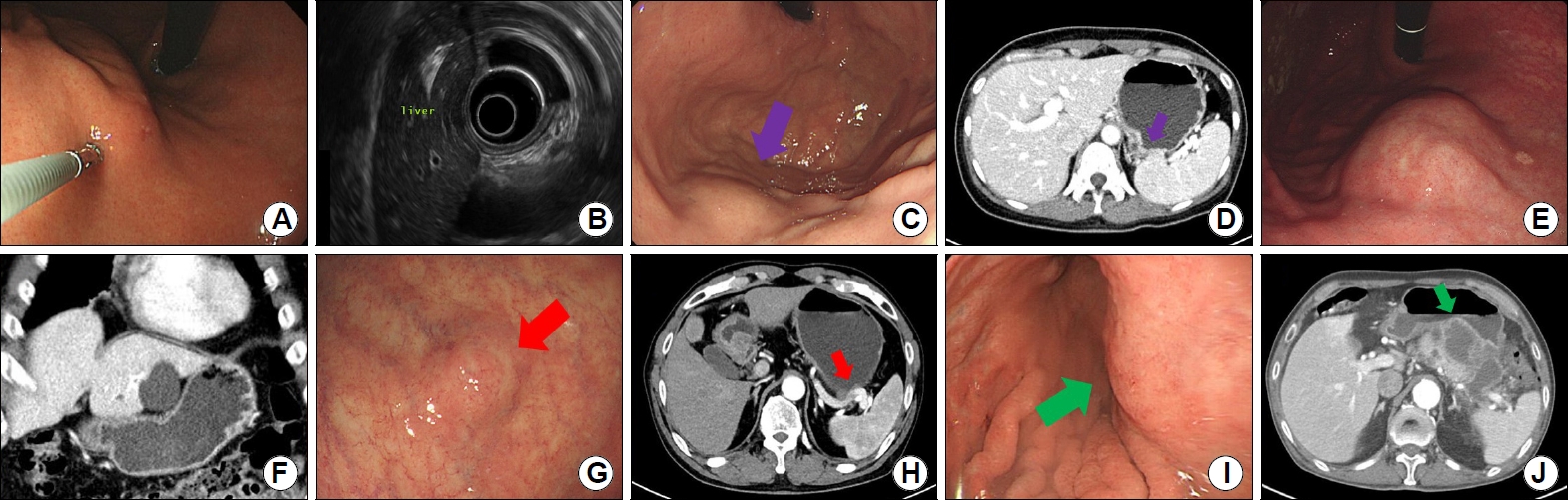
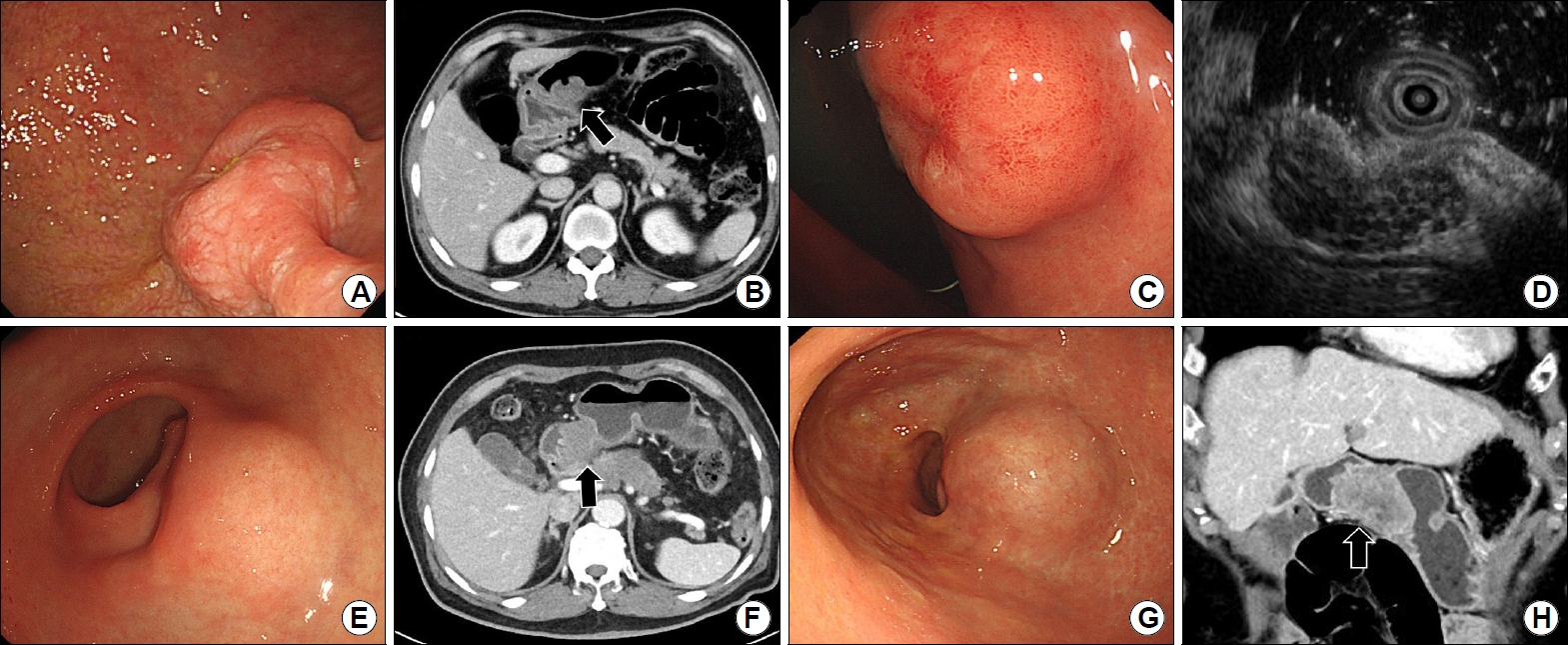
Fig. 6.
Gastric subepithelial tumor-like cancers. (A, B) A 3 cm-sized SET-like mass with a central depression was observed on the posterior wall of the antrum (arrow). After subtotal gastrectomy with lymph node dissection, a poorly differentiated adenocarcinoma with deep submucosal invasion and lymph node metastasis was confirmed. (C) A 2 cm-sized SET-like mass was observed on the posterior wall of the lower body. The biopsy in the central depression was diagnosed as gastric MALT lymphoma. (D) Latticework structure is observed inside the tumor in endoscopic ultrasound. (E) A mass was observed, and the boundary is unclear as it seemed to be pressed outside in the antrum. (F) Stomach invasion of the pancreatic cancer was confirmed in abdominal CT (arrow). (G, H) Peritoneal metastasis was observed in the form of SET-like mass in the antrum (arrow) in a patient after ovarian cancer surgery. SET, subepithelial tumor; MALT, mucosa-associated lymphoid tissue; CT, computed tomography.
REFERENCES
1. Song JH, Kim SG, Chung SJ, Kang HY, Yang SY, Kim YS. Risk of progression for incidental small subepithelial tumors in the upper gastrointestinal tract. Endoscopy 2015;47:675–679.



2. Polkowski M. Endoscopic ultrasound and endoscopic ultrasound-guided fine-needle biopsy for the diagnosis of malignant submucosal tumors. Endoscopy 2005;37:635–645.


3. Kim MY, Jung HY, Choi KD, et al. Natural history of asymptomatic small gastric subepithelial tumors. J Clin Gastroenterol 2011;45:330–336.


4. Lim YJ, Son HJ, Lee JS, et al. Clinical course of subepithelial lesions detected on upper gastrointestinal endoscopy. World J Gastroenterol 2010;16:439–444.



5. Kim GH. Systematic endoscopic approach for diagnosing gastric subepithelial tumors. Gut Liver 2022;16:19–27.



6. Klöppel G, Clemens A. The biological relevance of gastric neuroendocrine tumors. Yale J Biol Med 1996;69:69–74.


8. Tada S, Iida M, Yao T, et al. Endoscopic removal of inflammatory fibroid polyps of the stomach. Am J Gastroenterol 1991;86:1247–1250.

9. Hwang JH, Saunders MD, Rulyak SJ, Shaw S, Nietsch H, Kimmey MB. A prospective study comparing endoscopy and EUS in the evaluation of GI subepithelial masses. Gastrointest Endosc 2005;62:202–208.


10. Hwang JH, Rulyak SD, Kimmey MB.; American Gastroenterological Association Institute. American Gastroenterological Association Institute technical review on the management of gastric subepithelial masses. Gastroenterology 2006;130:2217–2228.


11. Nishida T, Blay JY, Hirota S, Kitagawa Y, Kang YK. The standard diagnosis, treatment, and follow-up of gastrointestinal stromal tumors based on guidelines. Gastric Cancer 2016;19:3–14.



12. Yasuda K, Cho E, Nakajima M, Kawai K. Diagnosis of submucosal lesions of the upper gastrointestinal tract by endoscopic ultrasonography. Gastrointest Endosc 1990;36(2 Suppl): S17–S20.


13. Gress F, Schmitt C, Savides T, et al. Interobserver agreement for EUS in the evaluation and diagnosis of submucosal masses. Gastrointest Endosc 2001;53:71–76.


14. Chak A, Canto MI, Rösch T, et al. Endosonographic differentiation of benign and malignant stromal cell tumors. Gastrointest Endosc 1997;45:468–473.


15. Palazzo L, Landi B, Cellier C, Cuillerier E, Roseau G, Barbier JP. Endosonographic features predictive of benign and malignant gastrointestinal stromal cell tumours. Gut 2000;46:88–92.



-
METRICS

-
- 3 Crossref
- 5,258 View
- 180 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
Endoscopic Findings of Common Gastritis in Koreans2023 June;23(2)
Homogenous Subepithelial Esophageal Lesion2023 March;23(1)
Approach to Small Gastric Subepithelial Lesions2023 March;23(1)
The Pathologic Confirmation in Subepithelial Tumors2021 September;21(3)