 |
 |
- Search
| Korean J Helicobacter Up Gastrointest Res > Volume 22(2); 2022 > Article |
|
Abstract
Background/Aims
The eradication success rate of Helicobacter pylori (H. pylori) infection with a first-line standard triple therapy (STT) has been decreasing in Korea. However, treatment outcomes of H. pylori infection in Yeongdong, Gangwon Province have been scarcely reported. This study aimed to investigate the treatment outcomes of H. pylori infection in a single tertiary care hospital with regional characteristics.
Materials and Methods
From July 2018 to June 2019, a total of 592 patients who underwent STT consisting of a proton pump inhibitor, amoxicillin, and clarithromycin for 7 to 14 days as a first-line H. pylori eradication therapy were included. Demographic data and treatment outcomes were retrospectively reviewed using medical records.
Results
The median age of 592 patients was 58 years (range 23 to 86) and 329 patients (55.6%) were men. The indication for eradication therapy included chronic atrophic gastritis (57.9%), peptic ulcer disease (19.6%), and gastric neoplasm after endoscopic resection (5.9%). Most patients (92.2%) received a 7-day course of STT. Eradication rate of STT was 64.0% (379/592). Rescue therapy was performed in 146 patients, and the final eradication rate reached 85.6% (507/592).
헬리코박터 파일로리(Helicobacter pylori, H. pylori) 감염은 소화성 궤양, 위암, 위 점막연관 림프조직 림프종의 발생과 밀접한 연관이 있으며 치료하지 않으면 지속적으로 위 내에 존재하면서 만성 염증을 일으킨다[1]. H. pylori 감염 유병률은 감소하는 추세이나 2015~2016년 시행된 대한상부위장관·헬리코박터학회 주도 전국 규모 연구에 따르면 국내 혈청학적 유병률은 51.0%로, 특히 40대 이상에서는 50% 이상의 유병률을 보였다[2]. H. pylori 제균 치료에는 위산분비억제제와 두 가지 이상의 항생제를 조합하여 사용하며, 국내에서는 일차 치료로 clarithromycin을 포함하는 표준 삼제요법을 권고한다[3]. 그러나 H. pylori의 항생제 내성이 증가함에 따라 전 세계적으로 표준 삼제요법의 제균 치료 성적은 감소하고 있으며[4,5], 국내에서 시행된 연구 결과에서도 공통적으로 표준 삼제요법의 성공률은 점차 감소하고 있는 것으로 보고되었다[6-9].
제균 치료 성적을 극대화하기 위해서는 각 지역의 특성과 항생제 내성 현황을 반영하는 제균 치료 방법을 선택하는 것이 중요하다[10]. 국내에서도 전국 규모의 다기관 연구를 시행하는 등의 노력을 기울이고 있으나 강원 영동지역에서 시행된 제균 치료 성적 및 항생제 내성 현황에 대한 연구는 드물다[9,11,12]. 이전 연구에서 1997년 1월부터 1998년 8월 사이 강원 영동지역 단일 기관의 건강검진 센터 또는 가정의학과에 방문하여 표준 삼제요법을 7일간 시행받은 환자 132명의 제균 치료 성적을 조사하여 보고하였다[13]. 그러나 이 연구는 흡연 상태 및 흡연량이 제균 치료 결과에 미치는 영향을 알아보기 위한 목적으로 수행된 연구이며, 이후 최근까지 강원 영동지역에 국한된 제균 치료 관련 연구 결과는 보고된 바 없다. 이에 본 연구에서는 강원 영동지역의 H. pylori 일차 제균 치료에 사용된 표준 삼제요법의 제균 치료 성적을 조사하였다.
이 후향 연구는 2018년 7월부터 2019년 6월 사이 강릉아산병원에서 조직 검사(Hematoxylin and Eosin, Giemsa 염색) 또는 요소호기 검사(14C-urea breath test) 결과 H. pylori 감염을 진단받고 일차 제균 치료로 표준 삼제요법을 시행받은 환자를 대상으로 하였다. 연구 기간 중 일차 제균 치료를 받은 911명의 환자 중 위 절제술의 병력이 있거나(n=6) 표준 삼제요법 이외의 치료를 받은 경우(n=2), 치료 후 추적 검사를 시행하지 않아 치료 결과를 알 수 없는 경우(n=182), 제균 결과 확인을 위한 요소호기 검사를 시행하지 않은 경우(n=129)를 제외한 592명을 분석에 포함하였다(Fig. 1). 연구 대상 환자의 인구학적 요인, 병력, 치료와 연관된 특징 등을 의무기록을 통해 조사하였다. 이 연구는 강릉아산병원 기관생명윤리위원회로부터 심의 면제를 받았다(IRB No. 2021-11-001).
표준 삼제요법은 양성자펌프억제제(pantoprazole, lansoprazole 또는 esomeprazole 표준용량), amoxicillin 1 g, clarithromycin 500 mg을 하루 2회 7~14일간 투약하였다. 일차 제균 치료에 실패한 경우 bismuth 사제요법(양성자펌프억제제 표준용량 하루 2회, bismuth 120 mg 하루 4회, metronidazole 500 mg 하루 3회, tetracycline 500 mg 하루 4회), metronidazole 삼제요법(양성자펌프억제제 표준용량, amoxicillin 1 g, metronidazole 500 mg 하루 2회), levofloxacin 삼제요법(양성자펌프억제제 표준 용량, amoxicillin 1 g, levofloxacin 250 mg 하루 2회) 등을 구제 요법으로 시행하였다. 제균 치료 방법과 기간 및 양성자펌프억제제의 종류는 처방 의사의 선호도에 따라 결정되었다. 제균 치료 성공 여부는 제균 치료 4주 이후 시행한 요소호기 검사 결과를 바탕으로 판단하였다.
연구 기간 중 총 592명이 일차 제균 치료로 표준 삼제요법을 시행받았다. 환자 592명의 나이 중앙값은 58세(범위 23~86세)였으며 329명(55.6%)이 남성이었다(Table 1). 흡연력과 음주력은 565명에서 확인 가능하였고, 24.1%가 과거 또는 현재 흡연력을 보고하였으며 36.5%에서 음주력이 있었다. 일차 제균 치료에 성공한 군과 실패한 군을 비교하였을 때 치료에 실패한 군에서 여성의 비율이 더 많았다.
제균 치료의 적응증은 만성 위축성 위염이 57.9%로 가장 많았고 소화성 궤양(19.6%), 위 용종(8.4%), 조기위암 또는 위 선종의 내시경적 절제술 후(5.9%) 등이 포함되었다(Table 2). 제균 치료 기간은 92.2%에서 7일이었으며, 30.4%에서 제균 치료 약제에 보조적으로 점막보호제나 유산균제제가 처방되었다.
총 592명 중 379명이 표준 삼제요법에 성공하여 제균율은 64.0%였다. 약제 복용 순응도를 확인할 수 있었던 164명 중 약제의 90% 이상을 복용한 환자의 비율은 95.1%였으며 제균 치료에 실패한 군에서 순응도가 더 낮았다(P=0.021). 의무기록을 통해 이상 반응 유무를 파악할 수 있었던 162명 중 32명(19.8%)에서 이상 반응을 보고하였으며, 설사, 금속성 맛, 전신 위약감, 상복부 불편감 등이 포함되었다. 이상 반응은 대부분 경미하였으나 1명에서 일상생활에 중등도의 제한이 따르는 구토와 설사가 지속되어 약제의 85.7% 복용 후 복용을 중단하였다.
일차 제균 치료에 실패한 213명 중 146명이 이차 제균 치료를 받았으며 이 중 124명(84.9%)에서 제균 치료에 성공하였다(Fig. 1). 이차 제균 치료에는 bismuth 사제요법이 가장 흔히 사용되었으며 제균 성공률은 91.1% (102/112)로 우수하였다. 이외 metronidazole 삼제요법과 levofloxacin 삼제요법이 시행되었으며 제균 성공률은 각각 62.1% (18/29), 66.7% (2/3)이었다. 이차 치료에 실패한 환자 중 4명에서 삼차 치료로 levofloxacin 삼제요법이 시행되었고 4명 모두 제균에 성공하였다. 종합하면, 총 592명 중 507명(85.6%)이 1~3회의 제균 치료 후 제균에 성공하였다.
일차 제균 치료 실패와 관련된 인자를 확인하기 위해 회귀분석을 시행하였다(Table 3). 단변량 분석에서 여성, 음주력, 90% 미만의 순응도가 치료 실패와 연관을 보였으며, 다변량 분석 결과 90% 미만의 순응도(OR, 8.951; 95% CI, 1.058~75.743; P=0.044)가 통계적으로 유의한 인자였다. 양성자펌프억제제 종류와 치료 기간, 치료 적응증, 점막보호제 또는 유산균제제 사용은 치료 실패와 뚜렷한 연관을 보이지 않았다.
강원 영동지역 단일 기관의 표준 삼제요법 제균 치료 성적은 64.0%이며, 낮은 순응도가 치료 실패와 연관된 인자였다. 국내에서 지속적으로 보고되고 있는 표준 삼제요법의 제균율 감소와 마찬가지로, 강원 영동지역에서도 표준 삼제요법은 일차 제균 치료로 권고하기에 적합하지 않은 치료 성적을 보였다.
H. pylori 제균 치료에 적합한 치료 방법은 치료 효과가 90% 이상이면서 이상 반응 발현율이 5% 이하여야 한다[14,15]. 또한 제균 치료에는 여러 가지 항생제를 조합하여 사용하므로 치료 실패에 따른 항생제 내성 발현 가능성에 대해서도 고려해야 한다. 국내에서 1998년 처음 발표된 제균 치료 권고안에서는 치료 성적이 90% 이상이며 이상 반응이 적고 복용 방법이 간편하다는 점에 근거하여 표준 삼제요법 1주 또는 2주 투여를 일차 치료로 권고하였다[14]. 이후 현재까지 일차 치료로 권고되고 있는 것은 표준 삼제요법으로[16,17], 2020년 개정된 가이드라인에서는 clarithromycin 감수성인 경우 1주, clarithromycin 내성 여부를 알 수 없는 경우에는 2주간 치료할 것을 권고하였다[3].
표준 삼제요법의 제균율은 2000년대 초반까지는 90% 이상으로 효과적인 것으로 판단되었으나[6,18,19] 이후 제균율이 점차 감소하여 일차 제균 치료로 적합하지 않다는 우려가 계속되었다[7,9,12,20,21]. 국내 단일 기관에서 10년 이상의 기간 동안 제균율 변화 추이를 분석한 연구에서 공통적으로 의미 있는 제균율 감소 추세를 보였으며[6,8], 다기관 연구에서도 삼제요법의 제균 치료 성적은 2001~2007년 84.9~87.5%에서 2008~2010년 80.0~81.4%로 뚜렷하게 감소하였다[9]. 제균 치료 성적의 유의한 변화를 관찰할 수 없었던 다른 연구에서는 제균 치료 성적이 지속적으로 낮게 유지되어 72.5~87.2%에 머물렀다[22-25]. 최근 시행된 무작위 배정 연구에서 표준 삼제요법의 제균율은 7일 치료군에서 78.5%, 14일 치료군에서 78.6%로 치료 기간에 관계 없이 80% 미만이었다[21].
이러한 제균 치료 성적 감소의 주요한 요인은 H. pylori의 항생제 내성 증가이며, 특히 clarithromycin 내성은 표준 삼제요법 실패와 밀접한 연관이 있다[26-29]. 국내에서 시행된 H. pylori의 항생제 내성에 대한 연구 결과는 항생제 감수성 검사 방법과 연구 기관에 따라 차이가 있으나 clarithromycin에 대한 내성 빈도는 공통적으로 증가 추세를 보이고 있다[30,31]. 국내 단일 기관에서 수행된 연구에 다르면 H. pylori의 clarithromycin에 대한 내성은 2009~2010년 7.0%에서 2011~2012년 16.0%로 증가하였으며[32], 다른 연구에서도 2003~2005년 21.2%에서 2011~2012년 34.1%, 2017~2018년 45.9%로 급격히 증가하였다[33]. 대한상부위장관·헬리코박터학회 주도로 2017~2018년 시행된 전국 규모 다기관 연구에서 clarithromycin 내성은 17.8%로, 제균 치료 약제를 선택할 때 고려하는 clarithromycin 내성 기준인 15%보다 높은 것으로 나타났다[11,34]. 이러한 연구 결과는 국내에서 clarithromycin 감수성 여부를 확인하지 않고 경험적으로 표준 삼제요법을 선택하였을 때 치료에 실패할 가능성이 높음을 시사한다.
제균 치료 성적은 지역에 따라서도 다르게 보고된다. 표준 삼제요법의 제균율은 경기 서부에서는 85.5%, 광주 전남지역에서는 77.0%, 대구 경북지역에서는 86.2%, 부산에서는 84.9%로 다양하게 보고되었다[6,8,22,35]. 이러한 제균 치료 성적의 차이는 H. pylori의 항생제 내성 현황이 지역에 따라 다르기 때문이며, 따라서 제균 치료 성적을 향상시키기 위해서는 각 지역의 특성을 반영하는 항생제 내성 자료를 확보하는 것이 중요하다[10,36]. 그러나 강원 영동지역에서 시행된 표준 삼제요법의 제균 치료 성적 및 항생제 내성 현황 대한 연구는 드물다. 강원 영동지역의 H. pylori 제균 성적을 보고한 단일 기관 연구 결과에 따르면 표준 삼제요법의 제균율은 84.1% (111/132)였으며 제균 치료 시작 후 금연한 경우 제균 치료 성적이 더 높았다[13]. 그러나 이 연구는 1997~1998년에 수행된 것으로, 최근 H. pylori의 항생제 내성 증가 및 삼제요법의 제균율 감소 추세를 반영하는 자료는 부족하다. 온라인 레지스트리를 기반으로 한 전국 규모 다기관 연구에서 강원지역의 삼제요법을 포함한 일차 제균 치료 성적은 68.1%로 서울, 경기, 경상, 제주지역보다 낮았으나 영동지역의 자료는 포함되어 있지 않다[12]. H. pylori의 항생제 내성 현황을 조사한 다기관 연구에도 강원지역의 균주가 포함되었으나 영동지역의 자료는 포함되어 있지 않다[11,36]. 이에 본 연구에서는 강원 영동지역의 표준 삼제요법 치료 성적을 조사하였으며 표준 삼제요법의 제균율은 64.0%로 1999년 보고와 비교하여 크게 감소하였다. 그러나 항생제 내성, 특히 clarithromycin 내성에 대한 진단 검사는 수행되지 않아, 향후 H. pylori의 항생제 내성 현황 등 표준 삼제요법의 제균율 감소를 뒷받침하는 체계적인 자료를 구축하는 것이 중요하다. 한편, 표준 삼제요법 실패 후 bismuth 사제요법의 제균 치료 성공률은 91.1%로 우수하여 표준 삼제요법에 실패한 환자에서 효과적인 이차 치료 방법임을 확인하였다.
제균 치료 실패에 영향을 미치는 인자로 H. pylori의 항생제 내성 이외에도 성별, 흡연, CYP2C19 genetic polymorphism 등이 알려져 있다[8,29,37-39]. 음주력이 있는 환자에서 음주력이 없는 경우보다 제균 치료 성공률이 높았다는 연구 결과도 있다[40]. 이 연구에서는 낮은 순응도가 제균 치료 실패와 연관된 인자였으며, 성별, 흡연력, 양성자펌프억제제 종류 등은 유의한 연관성을 보이지 않았다.
이 연구의 제한점은 다음과 같다. 첫 번째, 단일 기관에서 시행된 연구로 전체 인구 집단의 특성을 대표하지 못할 가능성이 있다. 그러나 강릉아산병원은 강원 영동지역에 위치한 유일한 상급 종합병원으로 내원 환자의 대부분이 영동지역 주민으로 구성되어 있어 연구 결과가 지역적 특성을 반영한다고 가정할 수 있다. 두 번째, 의무기록 검토에 바탕을 둔 후향 연구로 선택 비뚤림, 보고 비뚤림과 같은 비뚤림 가능성을 배제할 수 없다. 제균 치료 성적은 객관적인 검사 결과를 기반으로 하므로 신뢰할 수 있으나 흡연력, 음주력, 순응도, 이상 반응 유무 등에 대한 자료가 상당수에서 누락되었다는 점은 중요한 제한점이다. 제균 치료 성적과 연관된 인자를 탐색하기 위해서는 병력과 항생제 내성 결과를 포함한 체계적인 자료의 수집이 필요하다.
결론적으로, 강원 영동지역에서 표준 삼제요법의 치료 성적은 70% 미만으로, 일차 제균 치료 방법으로 권고하기에 적절하지 않은 수준이다. 이 지역의 H. pylori 제균 치료 성적을 향상시키기 위해서는 항생제 감수성 검사 결과에 기반한 맞춤 치료를 포함한 다른 제균 치료 방법에 대한 모색이 필요하다.
Acknowledgements
This work was supported by the Korean College of Helicobacter and Upper Gastrointestinal Research Foundation Grant (No. KCHUGR-201902504 and KCHUGR-202002501).
Fig. 1.
Study flow and outcomes. Among the 592 patients who received standard triple therapy, 379 (64.0%) are successfully eradicated. Of the 213 patients who failed standard triple therapy, 146 received second-line eradication therapy, and the eradication rate is 84.9% (124/146). H. pylori, Helicobacter pylori; STT, standard triple therapy; UBT, urea breath test.
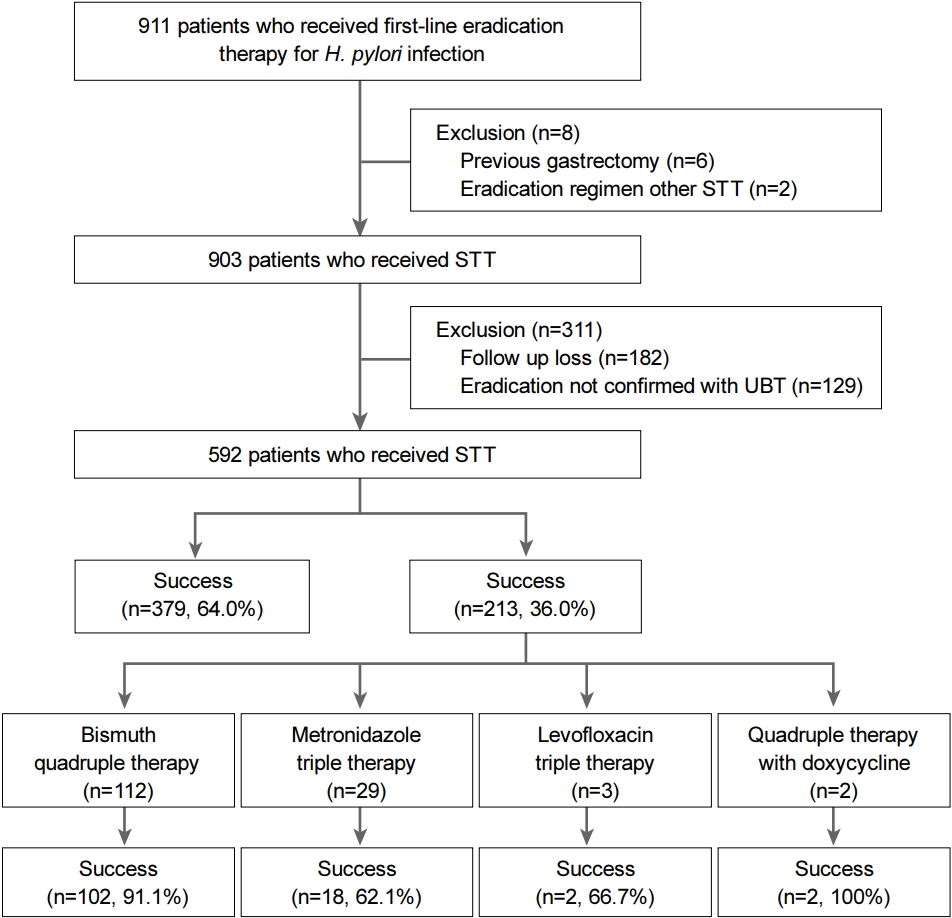
Table 1.
Demographic and Clinical Characteristics of the Study Population
Table 2.
Characteristics Associated with First-line Standard Triple Therapy
| Total (n=592) | Success (n=379) | Fail (n=13) | P-value | |
|---|---|---|---|---|
| Indication | 0.651 | |||
| Peptic ulcer disease | 116 (19.6) | 77 (20.3) | 39 (18.3) | |
| MALT lymphoma | 3 (0.5) | 3 (0.8) | 0 (0.0) | |
| Early gastric cancer | 14 (2.4) | 11 (2.9) | 3 (1.4) | |
| Atrophic gastritis | 343 (57.9) | 219 (57.8) | 124 (58.2) | |
| Dyspepsia | 25 (4.2) | 14 (3.7) | 11 (5.2) | |
| Family history of gastric cancer | 8 (1.4) | 5 (1.3) | 3 (1.4) | |
| Iron deficiency anemia | 1 (0.2) | 0 (0.0) | 1 (0.5) | |
| Gastric polyp | 50 (8.4) | 29 (7.7) | 21 (9.9) | |
| Gastric adenoma | 21 (3.5) | 15 (4.0) | 6 (2.8) | |
| Lymphofollicular gastritis | 11 (1.9) | 6 (1.6) | 5 (2.3) | |
| Proton pump inhibitors | 0.531 | |||
| Pantoprazole | 138 (23.3) | 84 (22.2) | 54 (25.4) | |
| Lansoprazole | 86 (14.5) | 53 (14.0) | 33 (15.5) | |
| Esomeprazole | 368 (62.2) | 242 (63.9) | 126 (59.2) | |
| Duration | 1.000 | |||
| 7 days | 546 (92.2) | 350 (92.3) | 196 (92.0) | |
| 10 days | 24 (4.1) | 15 (4.0) | 9 (4.2) | |
| 14 days | 22 (3.7) | 14 (3.7) | 8 (3.8) | |
| Use of supplementary agents | 0.348 | |||
| None | 412 (69.6) | 264 (69.7) | 148 (69.5) | |
| Mucoprotective agents | 111 (18.8)a | 69 (18.3) | 42 (19.7)a | |
| Probiotics | 71 (12.0)a | 46 (12.1) | 25 (11.7)a | |
| Compliance ≥90% (n=164) | 156 (95.1) | 93 (98.9) | 63 (90.0) | 0.021 |
| Adverse event (n=162) | 32 (19.8) | 15 (16.1) | 17 (24.6) | 0.231 |
Table 3.
Factors Associated with Eradication Failure after Standard Triple Therapy
REFERENCES
2. Lee JH, Choi KD, Jung HY, et al. Seroprevalence of Helicobacter pylori in Korea: a multicenter, nationwide study conducted in 2015 and 2016. Helicobacter 2018;23:e12463.




3. Jung HK, Kang SJ, Lee YC, et al. Evidence-based guidelines for the treatment of Helicobacter pylori infection in Korea: 2020 revised edition. Korean J Helicobacter Up Gastrointest Res 2020;20:261–287.


4. Thung I, Aramin H, Vavinskaya V, et al. Review article: the global emergence of Helicobacter pylori antibiotic resistance. Aliment Pharmacol Ther 2016;43:514–533.



5. Rokkas T, Gisbert JP, Malfertheiner P, et al. Comparative effectiveness of multiple different first-line treatment regimens for Helicobacter pylori infection: a network meta-analysis. Gastroenterology 2021;161:495–507; e4.


6. Song JG, Lee SW, Park JY, et al. Trend in the eradication rates of Helicobacter pylori infection in the last 11 years. Korean J Med 2009;76:303–310.
7. Gong EJ, Yun SC, Jung HY, et al. Meta-analysis of first-line triple therapy for Helicobacter pylori eradication in Korea: is it time to change? J Korean Med Sci 2014;29:704–713.




8. Kim SE, Park MI, Park SJ, et al. Trends in Helicobacter pylori eradication rates by first-line triple therapy and related factors in eradication therapy. Korean J Intern Med 2015;30:801–807.




9. Shin WG, Lee SW, Baik GH, et al. Eradication rates of Helicobacter pylori in Korea over the past 10 years and correlation of the amount of antibiotics use: nationwide survey. Helicobacter 2016;21:266–278.


10. Zamani M, Alizadeh-Tabari S, Zamani V, Shokri-Shirvani J, Derakhshan MH. Worldwide and regional efficacy estimates of first-line Helicobacter pylori treatments: a systematic review and network meta-analysis. J Clin Gastroenterol 2022;56:114–124.

11. Lee JH, Ahn JY, Choi KD, et al. Nationwide antibiotic resistance mapping of Helicobacter pylori in Korea: a prospective multicenter study. Helicobacter 2019;24:e12592.



12. Kim BJ, Yang CH, Song HJ, et al. Online registry for nationwide database of Helicobacter pylori eradication in Korea: correlation of antibiotic use density with eradication success. Helicobacter 2019;24:e12646.




13. Oh MK, Choi WS, Lee YB, Chung HR, Kang GH, Kim JS. The effect of smoking on eradication of Helicobacter pylori. J Korean Acad Fam Med 1999;20:991–999.
14. Korean H. pylori Study Group. Diagnosis and treatment of Helicobacter pylori infection in Korea. Korean J Gastroenterol 1998;32:275–289.
15. Graham DY, Lu H, Yamaoka Y. A report card to grade Helicobacter pylori therapy. Helicobacter 2007;12:275–278.


16. Kim N, Kim JJ, Choe YH, et al. Diagnosis and treatment guidelines for Helicobacter pylori infection in Korea. Korean J Gastroenterol 2009;54:269–278.


17. Kim SG, Jung HK, Lee HL, et al. Guidelines for the diagnosis and treatment of Helicobacter pylori infection in Korea, 2013 revised edition. Korean J Gastroenterol 2013;62:3–26.


18. Lee JY, Kim W, Gwak GY, et al. Reinfection rate and clinical manifestation of Helicobacter pylori-positive peptic ulcer disease after triple therapy containing clarithromycin. Korean J Gastroenterol 2002;39:93–100.
19. Kim BW, Choi MG, Choi H, et al. Pooled analysis of antibiotic therapy for Helicobacter pylori eradication in Korea. Korean J Gastroenterol 1999;34:42–49.
20. Lee SW, Kim HJ, Kim JG. Treatment of Helicobacter pylori infection in Korea: a systematic review and meta-analysis. J Korean Med Sci 2015;30:1001–1009.




21. Kim TH, Park JM, Cheung DY, Oh JH. Comparison of 7- and 14-day eradication therapy for Helicobacter pylori with firstand second-line regimen: randomized clinical trial. J Korean Med Sci 2020;35:e33.




22. Cho DK, Park SY, Kee WJ, et al. The trend of eradication rate of Helicobacter pylori infection and clinical factors that affect the eradication of first-line therapy. Korean J Gastroenterology 2010;55:368–375.

23. Na HS, Hong SJ, Yoon HJ, et al. Eradication rate of first-line and second-line therapy for Helicobacter pylori infection, and reinfection rate after successful eradication. Korean J Gastroenterol 2007;50:170–175.

24. Paek NY, Lim YJ, Lee JH, Kang JH, Park JB, Lee JH. Recent eradication rates of first-line triple regimens for H. pylori infection. Korean J Gastrointest Endosc 2010;41:5–9.
25. Yoon JH, Baik GH, Sohn KM, et al. Trends in the eradication rates of Helicobacter pylori infection for eleven years. World J Gastroenterol 2012;18:6628–6634.



26. Tshibangu-Kabamba E, Yamaoka Y. Helicobacter pylori infection and antibiotic resistance - from biology to clinical implications. Nat Rev Gastroenterol Hepatol 2021;18:613–629.



27. Lee JH, Sung IK, Kim JH, et al. Impact of clarithromycin resistance on the outcome of standard triple Helicobacter pylori eradication therapy. Korean J Helicobacter Up Gastrointest Res 2010;10:14–20.
28. Lee JY, Kim N, Kim MS, et al. Factors affecting first-line triple therapy of Helicobacter pylori including CYP2C19 genotype and antibiotic resistance. Dig Dis Sci 2014;59:1235–1243.



29. Chang YW, Ko WJ, Oh CH, et al. Clarithromycin resistance and female gender affect Helicobacter pylori eradication failure in chronic gastritis. Korean J Intern Med 2019;34:1022–1029.




30. Gong EJ, Ahn JY. Antimicrobial resistance of Helicobacter pylori isolates in Korea. Korean J Helicobacter Up Gastrointest Res 2018;18:82–88.


31. Kim JM, Kim JS, Jung HC, Kim N, Kim YJ, Song IS. Distribution of antibiotic MICs for Helicobacter pylori strains over a 16-year period in patients from Seoul, South Korea. Antimicrob Agents Chemother 2004;48:4843–4847.




32. An B, Moon BS, Kim H, et al. Antibiotic resistance in Helicobacter pylori strains and its effect on H. pylori eradication rates in a single center in Korea. Ann Lab Med 2013;33:415–419.



33. Lee JY, Kim N, Nam RH, Choi SI, Lee JW, Lee DH. Primary and secondary antibiotic resistance of Helicobacter pylori in Korea from 2003 to 2018. Helicobacter 2019;24:e12660.



34. Malfertheiner P, Megraud F, O'Morain CA, et al. Management of Helicobacter pylori infection-the maastricht v/florence consensus report. Gut 2017;66:6–30.


35. Jung YS, Lee SH, Park CS, et al. Trends in the eradication rates of Helicobacter pylori infection in Daegu and Gyeongsangbuk-do, Korea: multicenter study over 13 years. Korean J Gastroenterol 2014;63:82–89.


36. Kim JY, Kim NY, Kim SJ, et al. Regional difference of antibiotic resistance of Helicobacter pylori strains in Korea. Korean J Gastroenterol 2011;57:221–229.


37. Yu J, Yang P, Qin X, Li C, Lv Y, Wang X. Impact of smoking on the eradication of Helicobacter pylori. Helicobacter 2022;27:e12860.



38. Kang JM, Kim N, Lee DH, et al. Effect of the CYP2C19 polymorphism on the eradication rate of Helicobacter pylori infection by 7-day triple therapy with regular proton pump inhibitor dosage. J Gastroenterol Hepatol 2008;23(8 Pt 1): 1287–1291.


-
METRICS

-
- 1 Crossref
- 3,092 View
- 59 Download
- Related articles in Korean J Helicobacter Up Gastrointest Res
-
Vonoprazan-based Dual and Triple Therapy for Helicobacter pylori Eradication2023 September;23(3)
Eradication of Helicobacter pylori Infection Using 7-day PCR-based Tailored Therapy2023 June;23(2)
Endoscopic Scoring System for Predicting Helicobacter pylori Infection2022 December;22(4)






